分析方法验证(analytical method validation)的目的是证明采用建立的方法适合于相应检测要求。在建立药品质量标准、变更药品生产工艺或制剂组分、修订原分析方法时,需对分析方法进行 验证。方法验证的理由、过程和结果均应记载在药品质量标准起草说明或修订说明中。生 物制品质量控制中采用的方法包括理化分析方法和生物学测定方法,其中理化分析方法的 验证原则与化学药品基本相同,所以可参照本指导原则进行,但在进行具体验证时还需要 结合生物制品的特点考虑;相对于理化分析方法而言,生物学测定方法存在更多的影响因 素,因此本指导原则不涉及生物学测定方法验证的内容。
验证的分析项目有:鉴别试验、杂质测定(限度 或定量分析)、含量测定和特性参数(如:药物溶出度、释放度等)。
验证的指标有:专属性、准确度、精密度(包括重复性、中间精密度和重现性)、检测限、定量限、线性、范围和耐用性。在分析方法验证中,须用标准物质进行试验。 由于分析方法具有各自的特点,并随分析对象而变化,因此需要视具体情况拟订验证的指 标。表 1 中列出的分析项目和相应的验证指标可供参考。
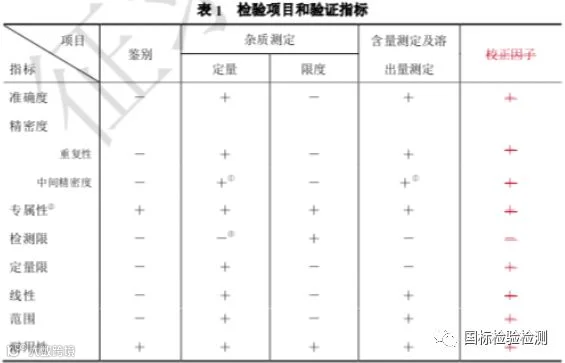
①已有重现性验证,不需验证中间精密度。
②如一种方法不够专属,可用其他分析方法予以补充。
③视具体情况予以验证。
方法验证内容如下。
一、专属性
专属性系指在其他成分(如杂质、辅料等)可能存在下,采用的分析方法 能正确测定出被测物的能力。鉴别反应、杂质检査和含量测定方法,均应考察其专属性。 如方法专属性不强,应采用多种不同原理的方法予以补充。
1. 鉴别反应
应能区分可能共存的物质或结构相似的化合物。不含被测成分的供试品,以及结构相似或组分中的有关化合物,应均呈阴性反应。
2. 含量测定和杂质测定
采用的色谱法和其他分离方法,应附代表性图谱,以说明方法的专属性,并应标明各成分在图中的位置,色谱法中的分离度应符合要求。
在杂质对照品可获得的情况下,对于含量测定,试样中可加入杂质或辅料,考察测定结果是否受干扰,并可与未加杂质或辅料的试样比较测定结果。对于杂质检查,也可向试样中加入一定量的杂质,考察各成分包括杂质之间能否得到分离。
在杂质不能获得的情况下,可将含有杂质或降解产物的试样进行测定,与另一个经验证了的方法或药典方法比较结果。也可用强光照射、高温、高湿、酸(碱)水解或氧化的方法进行加速破坏,以研究可能的降解产物和降解途径对含量测定和杂质测定的影响。含量测定方法应比对两种方法的结果,杂质检査应比对检出的杂质个数,必要时可采用光二极管阵列检测和质谱检测,进行峰纯度检查。
二、准确度
准确度系指用所建立方法测定的结果与真实值或参比值接近的程度,一般用回收 率(%)表示。准确度应在规定的线性范围内试验。准确度也可由所测定的精密度、 线性和专属性推算出来。
1. 化学药含量测定方法的准确度
原料药可用已知纯度的对照品或供试品进行测定,或用所测定结果与已知准确度的另一个方法测定的结果进行比较。制剂可在处方量空白辅料中,加入已知量被测物对照品进行测定。如不能得到制剂辅料的全部组分,可向待测制剂中加入已知量的被测物进行测定,或用所建立方法的测定结果与已知准确度的另一个方法测定结果进行比较。
2. 化学药杂质定量测定的准确度
可向原料药或制剂处方量空白辅料中加入已知量杂质对照品进行测定。如不能得到杂质对照品,可用所建立的方法测定结果与另一成熟的方法(如药典标准方法 或经过验证的方法)进行比较。在不能测得杂质的校正因子或不能测得对主成分的相对校正因子的情况下,可用主成分的校正因子计算杂质含量,并应明确表明单个杂质和杂质总量相 当于主成分的重量比(%)或面积比(%)。
3. 中药化学成分测定方法的准确度
可用已知纯度的对照品进行加样回收率测定,即向已知被测成分含量的供试品中再精 密加入一定量的已知纯度的被测成分对照品,依法测定。用实测值与供试品中含有量之差, 除以加入对照品量计算回收率。在加样回收试验中须注意对照品的加入量与供试品中被测 成分含有量之和必须在标准曲线线性范围之内;加入的对照品的量要适当,过小则引起较 大的相对误差,过大则干扰成分相对减少,真实性差。
4. 数据要求
在规定范围内,设计 3 种不同浓度,每种浓度分别制备 3 份供试品溶液进行测定,用 9 份样品的测定结果进行评价。
对于化学药,应报告已知加入量的回收率(%),或测定结果平均值与真实值之差及其相对标 准偏差或置信区间(置信度一般为 95%);对于中药,应报告供试品取样量、供试品中含有量、 对照品加入量、测定结果和回收率(%)计算值,以及回收率(%)的相对标准偏差(RSD%) 或置信区间。样品中待测定成分含 量和回收率限度关系可参考表 2。在基质复杂、组分含量低于 0.01%及多成分等分析中,回 收率限度可适当放宽。美国药典论坛 PF39(6) <1200> Requirements For Compendial Validation 中,准确度可接受标准:回收率=100%±2C-0.1505%,其中 C 为待测定成分含量。
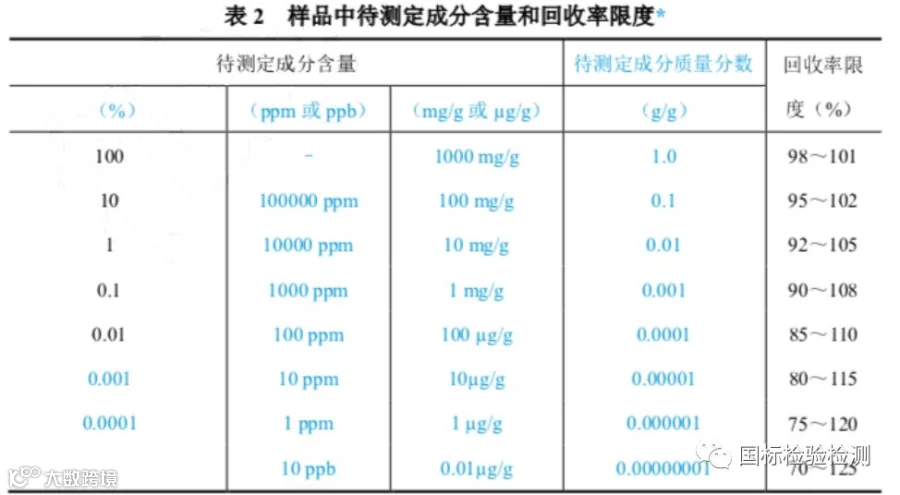
*此表源自 AOAC《Guidelines for Single Laboratory Validation of Chemical Methods for Dietary Supplements and Botanicals》
三、精密度
精密度系指在规定的条件下,同一份均匀供试品,经多次取样测定所得结果之间的接近程度。精密度一般用偏差、标准偏差或相对标准偏差表示。
在相同条件下,由同一个分析人员测定所得结果的精密度称为重复性;在同一个实验室,不同时间由不同分析人员用不同设备测定结果之间的精密度,称为中间精密度;在不同实验室由不同分析人员测定结果之间的精密度,称为重现性。
含量测定和杂质的定量测定应考察方法的精密度。
1. 重复性
在规定范围内,取同一浓度(分析方法拟定的样品测定浓度,相当于 100%浓度水平) 的供试品,用至少测定 6 份的结果进行评价;或设计 3 种不同浓度,每种浓度分别制备 3 份供试品溶液进行测定,用 9 份样品的测定结果进行评价。采用 9 份测定结果进行评价时, 浓度的设定应考虑样品的浓度范围。
2. 中间精密度
考察随机变动因素如不同日期、不同分析人员、不同仪器对精密度的影响,应设计方案进行中间精密度试验。
3. 重现性
国家药品质量标准采用的分析方法,应进行重现性试验,如通过不同实验室协同检验获得重现性结果。协同检验的目的、过程和重现性结果均应记载在起草说明中。应注意重现性试验所用样品质量的一致性及贮存运输中的环境对该一致性的影响,以免影响重现性试验结果。
4. 数据要求
均应报告偏差、标准偏差、相对标准偏差或置信区间。样品中待测定成分含量和精密 度 RSD 可接受范围参考表 3,可接受范围可在给出数值 0.5~2 倍区间。在基质复杂、组分 含量低于 0.01%及多成分等分析中,精密度限度可适当放宽。
表 3 样品中待测定成分的含量与精密度可接受范围*
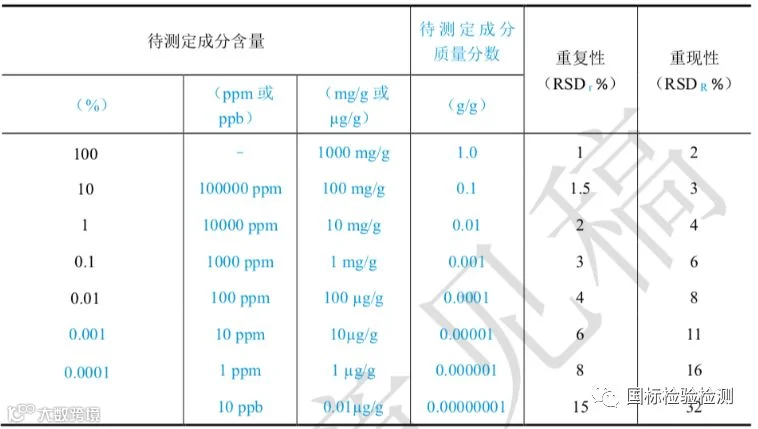
*此表源自 AOAC《Guidelines for Single Laboratory Validation of Chemical Methods for Dietary Supplements and Botanicals》
四、检测限
检测限(Limit Of Detection,LOD)系指试样中被测物能被检测出的最低量。药品的鉴 别试验和杂质检査方法,均应通过测试确定方法的检测限。检测限仅作为限度试验指标和 定性鉴别的依据,没有定量意义。常用的方法如下。
1. 直观法
用已知浓度的被测物,试验出能被可靠地检测出的最低浓度或量。
2. 信噪比法
用于能显示基线噪声的分析方法,即已知低浓度试样测出的信号与空白样品测出的信号进行比较,计算出能被可靠地检测出的被测物质最低浓度或量。一般以信噪比为 3:1 或 2:1 时相应浓度或注入仪器的量确定检测限。
3. 基于响应值标准偏差和标准曲线斜率法
按照LOD=3.3δ/S 公式计算。式中LOD:检测限;δ:响应值的偏差;S:标准曲线的斜率。
δ 可以通过下列方法测得:(1)测定空白值的标准偏差;(2)标准曲线的剩余 标准偏差或是截距的标准偏差来代替
4. 数据要求
上述计算方法获得的检测限数据须用含量相近的样品进行验证。应附测定图谱,说明试验过程和检测限结果。
五、定量限
定量限(Limit Of Quantitaion,LOQ)系指试样中被测物能被定量测定的最低量,其测 定结果应符合准确度和精密度要求。对微量或痕量药物分析、定量测定药物杂质和降解产 物时,应确定方法的定量限。常用的方法如下。
1. 直观法
用已知浓度的被测物,试验出能被可靠地定量测定的最低浓度或量。
2. 信噪比法
用于能显示基线噪声的分析方法,即把将已知低浓度试样测出的信号与空白样品测出的信号进行比较,计算出能被可靠地定量的被测物质的最低浓度或量。一般以信噪比为 10:1 时相应浓度或注入仪器的量确定定量限。
3. 基于响应值标准偏差和标准曲线斜率法
按照 LOQ = 10δ/S 公式计算。式中 LOQ:定量限;δ:响应值的偏差;S:标准曲线的 斜率。
δ 可以通过下列方法测得:1(1)测定空白值的标准偏差;2(2)采用标准曲线的 剩余标准偏差或是截距的标准偏差来代替。
4. 数据要求
上述计算方法获得的定量限数据须用含量相近的样品进行验证。应附测试图谱,说明测试过程和定量限结果,包括准确度和精密度验证数据。
六、线性
线性系指在设计的范围内,测定结果与试样中被测物浓度直接呈比例关系的程度。
应在设计的范围内测定线性关系。可用同一对照品贮备液经精密稀释,或分别精 密称取对照品,制备一系列对照品溶液的方法进行测定,至少制备 5 份不同浓度的供试样 品。以测得的响应信号作为被测物浓度的函数作图,观察是否呈线性,再用最小二乘法进行线性回归。必要时,响应信号可经数学转换,再进行线性回归计算。或者可采用描述浓 度-响应关系的非线性模型。
数据要求:应列出回归方程、相关系数和线性图(或其它数学模型)。
七、范围
范围系指分析方法能达到精密度、准确度和线性要求时的高低限浓度或量的区间。
范围应根据分析方法的具体应用及其线性、准确度、精密度结果和要求确定。原料药 和制剂含量测定,范围一般为测定浓度的 80%~120%;制剂含量均匀度检査,范围一般为 测定浓度的 70%~130%, 特殊剂型,如气雾剂和喷雾剂,范围可适当放宽;溶出度或释放 度中的溶出量测定,范围一般为限度的±30%,如规定了限度范围,则应为下限的-20%至 上限的+20%;杂质测定,范围应根据初步实际测定数据,拟订为规定限度的±20%。如果 含量测定与杂质检查同时进行,用峰面积归一化法进行计算,则线性范围应为杂质规定限 度的-20%至含量限度(或上限)的+20%。在中药分析中,对于有毒的、具特殊功效或药理作用的成分, 其验证范围应大于被限定含量的区间。
八、耐用性
耐用性系指在测定条件有小的变动时,测定结果不受影响的承受程度,为所建立的方 法用于常规检验提供依据。开始研究分析方法时,就应考虑其耐用性。如果测定试条件要 求苛刻,则应在方法中写明,并注明可以接受变动的范围,可以先采用均匀设计确定主要 影响因素,再通过单因素分析等确定变动范围。典型的变动因素有:被测溶液的稳定性、 样品的提取次数、时间等。液相色谱法中典型的变动因素有:流动相的组成和 pH 值、 不同品牌或不同批号的同类型色谱柱、柱温、流速等。气相色谱法变动因素有:不同品牌 或批号的色谱柱、固定相、不同类型的担体、载气流速、柱温、进样口和检测器温度等。
经试验,测定条件小的变动应能满足系统适用性试验要求,以确保方法的可靠性。


