一.什么是植物DNA?
DNA是一种我们在生物课上经常听到的词汇,它是指脱氧核糖核酸,是所有生物体遗传信息的载体。DNA像是一本书,里面写满了每个生物独特的“生命密码”。它决定了生物的样貌、行为以及生长方式。
植物DNA-Plant DNA Kit 简而言之是指植物中的DNA片段。自然界中热带雨林的参天大树, 农田里的玉米水稻、还是北极的冰川苔藓,所有植物都有自己独特的DNA排列。科学家可以从样本中直接提取DNA,从而对植物性状, 病虫害防止, 乃至物种演化进行研究 。

Martienssen 和McClintock,1989年在冷泉港实验室的玉米试验田
图源:Gene&Development
二.植物DNA提取应用在哪些方面?
植物DNA提取是一种重要的分子生物学技术,可应用于植物基因组研究、遗传改良、种群遗传学、病害诊断和进化生物学等方面。
植物基因组研究
通过提取植物总DNA,研究人员可以了解植物基因组的组成、结构和功能。这对于理解植物的遗传特性、进化历史以及种间亲缘关系具有重要意义
植物遗传改良
通过提取植物总DNA,可以发现植物中的有用基因或性状相关基因,并进行基因定位和序列分析这为培育具有优良性状的新品种提供了基础。
植物种群遗传学研究
研究植物种群的遗传结构和变异情况。通过分析植物总DNA中的遗传标记(如微卫星和单核苷酸多态性),可以推断不同个体和种
植物病害诊断
应用于植物病害的诊断。通过提取植物总DNA,可以检测病原体的存在和种类,从而确定植物是否感染了某种病害,进而采取相应的病害防治措施。
进化生物学研究
也在进化生物学研究中得以广泛应用。通过提取各种植物的总DNA,可以进行物种间的比较分析,了解不同物种的进化关系和演化历程。
非离子型去污剂十六烷基三甲基溴化铵(CTAB)最初被用于提取细菌基因组DNA。后来经改造用于提取植物DNA。当NaCl的浓度降到0.5 mol/L时,CTAB可以与DNA形成不溶的复合物而沉淀下来,而其他的杂质,如多糖、酚复合物则不会沉淀下来从而被除去。随后在高盐溶液中,CTAB则与DNA分离,并通过离心使DNA沉淀下来。
实验材料
2-巯基乙醇(2-ME), CTAB 抽提液,CTAB/NaCl 溶液,CTAB 沉淀液,24:1 (V/V) 氯仿/辛醇,高盐TE缓冲液,80%乙醇,TE缓冲液,异丙醇。
实验步骤
(1) 在所需量的CTAB抽提液中加入2-ME,使终浓度达2% (V/V)。将此溶液及 CTAB/NaCl溶液加热至65℃。对于每克新鲜的叶组织大约需要4 mL的2-ME/CTAB抽提液和0.4~0.5mL的CTAB/NaCl溶液。而对于干的植物组织,则2-ME/CTAB抽提液须用蒸馏水稀释一倍。
(2) 用液氮或干冰冷却匀浆器,将植物组织粉碎成为细粉,然后将其转移到一个抗有机溶剂的试管或烧杯中。
(3) 往粉碎的组织中加入65℃的2-ME/CTAB,充分混合,于65℃温育10~60min,不时混匀。
(4) 加入等体积的24:1氯仿/辛醇抽提匀浆液,颠倒使充分混合,于4℃ 7500 g离心5 min,回收水相。
(5) 在回收的水相中加入0.1体积的65℃的CTAB/NaCl溶液,颠倒混匀。
(6) 用等体积的氯仿/辛酵抽提,混匀,离心,回收上层水相。
(7) 加入等体积的CTAB沉淀液,颠倒混匀,如果沉淀不可见,则先于65 ℃温育 30 min 。
(8) 于 4℃,500 g 离心 5 min。
(9) 移出上清,但不要丢弃,用高盐的TE缓冲液溶解沉淀(每克组织0.5~lmL), 如果沉淀难于溶解,于65℃温育30 min,重复直至所有的或大部分沉淀溶解。
(10)加入0.6体积的异丙醇,充分混匀,于4℃,7500 g离心15 min。
(11)用80%乙醇洗涤沉淀物,干燥,用TE重悬(每克起始材料0.1~0.5mL)。
SDS法
这种方法的原理是采用离子去垢剂(十二烷基肌酸钠)裂解全细胞,蛋白酶K消化蛋白质。最后利用氯化铯密度梯度离心法获得基因组DNA及线粒体和叶绿体DNA。
实验材料
灭菌水,抽提缓冲液,液氮,TE溶液(PH 8.0),10% (W/V)十二烷基肌酸钠 (SDS)溶液,异丙醇,氯化铯,氯化铯饱和的异丙醇,10 mg/mL溴化乙锭,无水乙醇, 3mol/L的NaAc溶液(pH5.2),水浴锅或温箱(调至55℃)。
实验步骤
(1)剪取10~50g新鲜植物组织,并用冷的灭菌水洗涤干净,吸水纸吸干。
(2) 放入研钵中,加入适量液氮,研磨成细粉。
(3) 将细粉转移至大离心管中,加入抽提缓冲液(5-10 mL/g植物),轻轻搅拌混匀,加入1/9体积十二烷基肌酸钠溶液,使其终浓度为1%。于55℃温育2 h。
(4)于4℃ 5500 g离心10 min,将上清液转移至新离心管中。
(5) 加入0.6体积异丙醇,如无沉淀出现,则于-20℃放置30 min。于4℃ 7500g 离心15 min,弃去上清。
(6) 用9mL TE重悬沉淀,加入9.7g固体CsCl,混匀,冰上放置30min。4℃ 7500 g离心10 min,将上清转移至新离心管。
(7) 加入0.5 mL 10 mg/L的溴化乙锭,冰上放置30 min。4℃ 7500 g离心10 min, 将上清转移至两个快封(QUICK-SEAL) 5 mL超离心管中,并封口。
(8) 20℃ 525000 g离心4 h,或20℃ 300000g离心过夜,在紫外灯下用十五号针头和注射器收集DNA带。
(9) 用CsCl饱和的异丙醇重复抽提DNA以除去溴化乙锭。
(10)加入2体积水和6体积100%乙醇,混匀。-20℃放置1 h,4℃ 7500 g离心10min。
(11)沉淀用TE缓冲液重悬,加入1/10体积的3mol/L乙酸钠和2体积的100%乙醇重新离心,沉淀晾干后用0.5~2mL TE缓冲液重悬。
关键因素
(1) 取组织前将植物置于阴暗处1~2日,并且尽量选用较幼嫩的植物组织,以减少淀粉含量。
(2) 研磨时要不时加入液氮,保持低温,防止DNA降解。研磨要尽量充分。
(3) 组织的细粉应当在抽提缓冲液中充分悬浮均匀后才加入十二烷基肌酸钠。
(4) 第6步用9mLTE溶解DNA时可以于55℃放置不超过2h帮助溶解。离心后液体表面可能出现单独的一层,为残余的十二烷基肌酸钠,吸去即可。
(5) EB有强诱变性,操作时应注意防护及污染问题。
(6) 整个过程中的操作,如振荡混匀等,动作应当轻柔,不要剧烈地摇晃倒置等, 防止DNA断裂。
高盐低pH法是指以无机盐和异丙烯为提纯试剂提取DNA的方法。通常采用的无机盐为低pH的醋酸钾,用来沉淀蛋白质。该方法方便省时,所需样品量少。
实验材料
灭菌水,提取缓冲液,液氮,PVP 1.5ml离心管, 2.5mo l/L KAC (pH 4.8),异丙醇,T E 缓冲液,水浴锅或温箱 冰箱。
实验步骤
(1)高盐低 pH 值法 ①取 0.05g 新鲜叶片(豆 荚)置液态氮中研磨成粉(加入少量 PVP),或取 1 粒 大豆干燥种子置研钵中研成干粉后分装于 2 支 1.5mL 离心管中(加入少量 PVP)。
(2) 迅速加入预热 至 65 ℃的 1mL 的提取缓冲液[ 100mmol/ L NaAC , 50mmol/ L EDTA 、500mmol/L N aCl 、2.5 %PV P 、 3 %SDS 、1 %β-巯基乙醇, pH5.5] , 于 65 ℃的恒温振 荡器 温 育 30min 。
(3) 10 000r/min 离 心 10min 。
(4) 吸取上清液加入 2/3 倍体积的 2.5mo l/L KAC (pH 4.8), 0 ℃下放置 30min , 10000r/min 离 心 10min 。
(5) 吸上清液移入另一支离心管中, 加入等 体积的氯仿/异戊醇(24 ∶1)反复颠倒混匀, 10000 r/min 离心 10min 反复抽提至中间无白色沉淀 。
(6) 上清液加入 0.6 倍体积-20 ℃异丙醇, 轻轻混匀 置-20 ℃沉淀 1h 。
(7) 8000r/min 离心 15min ,所得沉 淀用 70 %乙醇洗 2 ~ 3 次, 待残留的乙醇挥发后, 将 DNA 溶于 20μL T E 缓冲液中, 置-20 ℃冰箱中保存 备用 。
实验材料
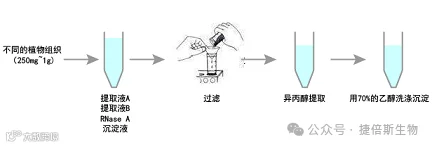
新鲜或干燥的植物提取样品,液氮,异丙醇,无水乙醇,磁力架,涡旋仪,研磨珠。
手 工 提 取 流 程
1.样品的处理:
●新鲜样品:
液氮研磨:新鲜样品可以用液氮研磨成粉末。研磨完成后,取小于100mg新鲜样品或者小于20mg干燥样品,加入600μl Buffer FPL与4μl RNase A涡旋混匀。(Buffer FPL与RNase A可以根据样品量预先混匀)。
珠磨仪:在2ml的离心管中加入1颗4mm的不锈钢珠(需单独购买)、600μl BufferFPL与4μl RNase A。加入小于100mg新鲜样品或者小于20mg干燥样品,叶片等易磨样品按65Hz,90s研磨一次。豆粒等难磨样品按65Hz,120s研磨2次。豆粒等要预先捣碎,直径不超3mm研磨效果更佳。
●干燥样品:用研钵或研磨研杵研磨成粉末。小于20mg干燥样品,加入600μl Buffer FPL与4μl RNase A涡旋混匀。
2.65℃水浴10分钟。孵育过程中短暂涡旋管子几次。
注意:珠磨仪研磨的样品,可以不用水浴直接进下下一步操作。
3.14,000×g下离心5-10min。
4.转移300µl上清到新的离心管中加入600 µl Buffer MB(第一次使用前加入异丙醇)和20µl MagIso Beads,混匀。静置2-4分钟。
5.将离心管放置于磁力架上静置1-2min,待磁珠完全吸附时小心去除液体。
6.加入600μl Buffer MW1(第一次使用前加入无水乙醇),盖上离心管涡旋15s,放回磁力架,离心管与磁力架一起颠倒3-4次,磁吸1min,吸弃所有液体(包括管盖中残留的)。
7.加入600μl Wash Buffer(第一次使用前加入无水乙醇),盖上离心管涡旋15s,放回磁力架,离心管与磁力架一起颠倒3-4次,磁吸1min,吸弃所有液体(包括管盖中残留的)。
8.重复上一步操作步一次。
9.空气干燥2-5分钟。 干燥不能太长时间,否则会影响洗脱。
10.加50~100µl 预热至55oC的Buffer TE或灭菌水等缓冲液,涡旋打散磁珠。静置3~5分钟,其间轻轻振荡1~2次加速DNA溶解。
11.转移至磁力架上,静置1-2分钟。转移DNA溶液至新的1.5ml离心管中。
| 货号 | 产品名称 |
|---|---|
|
|
|
|
|
Hpure Plant DNA Kit Hpure植物DNA提取试剂盒 |
|
|
|
|
|
Fast MagIso Plant DNA Isolation Kit 磁珠法快速植物DNA提取试剂盒 |
产品介绍:
https://www.gbcbio.cn/Product/M4105-50.html
https://www.gbcbio.cn/Product/D5105.html
https://www.gbcbio.cn/Product/M8105-50.html
https://www.gbcbio.cn/Product/M8115-50.html
四种植物DNA提取方法对比
| 方法 | 提取原理 | 适用范围 |
|
|---|---|---|---|
|
|
以CTAB为去污剂,并加提取缓冲液中β-巯基来控制酚类物质的氧化褐变及DNA的降解。增加氯仿/异戊醇除蛋白质,最后用乙醇沉淀DNA,以除去CTAB
|
适用范围广,适合绝大多数植物DNA的提取。尤其适用于含酚类及糖类物质较高植物材料。是目前最为常用的提取方法 |
|
|
|
使用SDS作为去污剂,并且用氯仿等有机溶剂去抽提蛋白质和糖类,最后用乙醇或异丙醇来沉淀DNA | 适用的范围较为广泛,适合小量植物DNA的提取,为较为常用的植物DNA提取方法 |
|
|
|
|
|
|
|
|
|
|
|
品牌优势
捷倍斯生物可以提供专业和完善的核酸分离纯化解决方案,有硅胶柱法、磁珠法与溶液直接法的核酸纯化产品,在二代测序的样品前处理方面有着专业的技术与积累,有完善的针对唾液、血液与血浆等样品的保存、运输与高通量核酸纯化等整套的解决方案。 在诊断试剂原料方面,捷倍斯生物可以提供生物染色剂、高端的表面活性剂、显色底物、生物缓冲剂以及酶制剂与其稳定剂等系列产品。

做值交往的人|做值得信赖的产品



