游离DNA(Circulating free DNA or Cell free DNA,cfDNA),循环游离DNA或者细胞游离DNA,是释放到血浆中的降解的DNA片段。cfDNA存在于人体的各种体液中,随组织损伤、癌症和炎症反应等发生浓度变化。母亲和胎儿-胎盘单位都会产生cfDNA,正常人体的cfDNA主要通过细胞凋亡过程中产生的小而均匀的185~200 bp小片段DNA。而肿瘤坏死的组织细胞由于非正常的凋亡过程,导致产生大小不同且大于200 bp的大片段DNA。循环中的cfDNA分子被迅速清除,半衰期为1小时或更短。
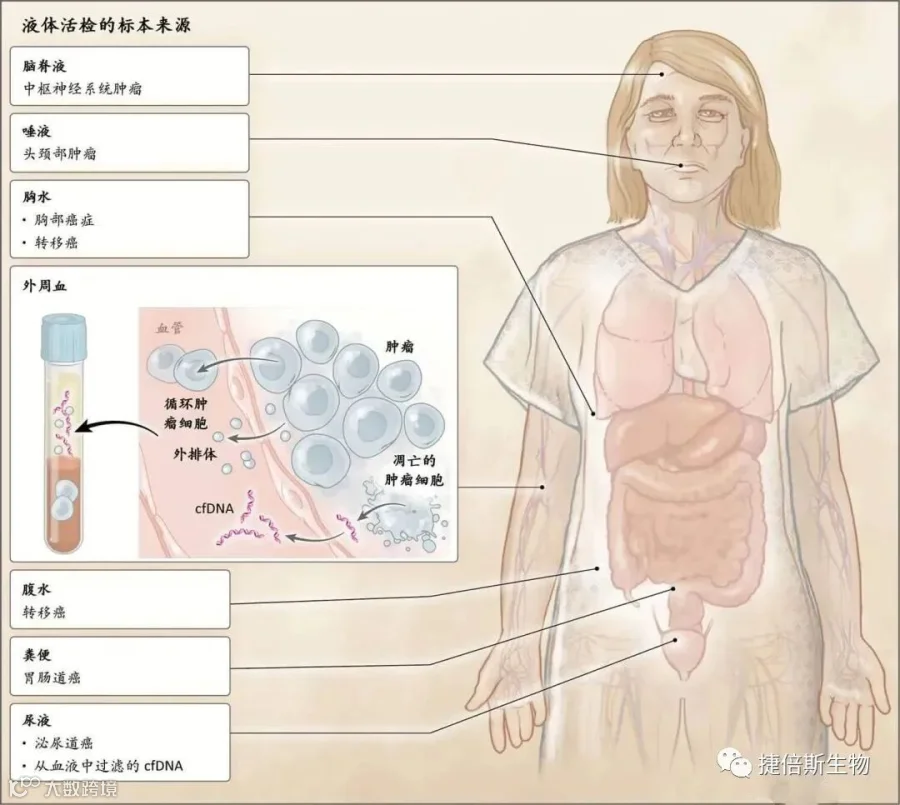 游离核酸的来源
游离核酸的来源
1947年,Mandel和Metais首次报道了外周血中存在cfDNA。生理情况下,血液中的cfDNA主要来源于白细胞的坏死和凋亡,在某些疾病和特殊状态下,其他细胞也会释放游离DNA入血,包括来源于肿瘤细胞的循环肿瘤DNA(ctDNA)和来源于胎儿的cfDNA等。血液不是可用于液体活检的唯一体液,例如尿液、粪便、脑脊液(CSF)、唾液、胸水和腹水都是潜在来源,可从中获得肿瘤来源的物质(包括cfDNA)。
cfDNA的生物学特点:
ctDNA检测是目前市场上最常见的液体活检形式,它在具备巨大潜力的同时,在检测开发和临床应用的推广方面也面对着一系列挑战。目前,血浆cfDNA的产生机制尚不明确。cfDNA多以DNA和蛋白质结合的复合物形式存在,仅极少数为游离的DNA片段。cfDNA在血浆和血清中都有存在,健康人外周血中cfDNA浓度大都小于100 ng/ml,平均值约为30 ng/ml。而在肿瘤患者体内,外周血cfDNA浓度可高达到1 000 ng/ml,平均值约为180 ng/ml。在其他的一些疾病,包括术后、寄生虫病、心血管疾病等也可见cfDNA水平的升高。
目前普遍认为细胞发生凋亡或者坏死释放的DNA片段是cfDNA的主要来源,但是不同疾病发生的病理生理进程不同,致病机制和疾病微环境也不同,因此不同疾病导致产生cfDNA的过程极为复杂,单一机制不能充分的阐明cfDNA产生的来源,往往是同时存在这两种产生机制。
cfDNA的主要作用:
胎儿的DNA会游离到孕妇的血液中,怀男孩的孕妇血液可以检测到Y染色体,还可用于产前检测,21和18三体;
器官移植免疫排斥产生的细胞死亡,DNA会释放到血液中,因此用于器官移植状态的监控;
cfDNA浓度与外伤、烧伤的损伤水平有关;
高浓度cfDNA也用于ICU死亡的预测,也可用于预测脓毒症和脓毒性休克,无菌性炎症,心肌梗死和无影像学结果的中风患者患病情况;
肿瘤来源的cfDNA,可以发现肿瘤相关的突变、杂合子缺失(LOH)、基因扩增、癌病毒DNA、抑癌基因启动子区的超甲基化,因此可以实现在无创条件下研究肿瘤DNA;
核小体在TSS区是否占据,影响cfDNA的深度,因此可以用来推测基因的表达情况;
目前cfDNA检验应用于临床常规的瓶颈主要集中于方法学和样本的质量上,由于血浆中存在的靶cfDNA微乎其微,标本的采集、抗凝剂使用和保存的不当都会影响检测的质量,造成假阳性或假阴性的结果。随着cfDNA分析技术迅速发展,在肿瘤学中具有许多有希望的临床应用。如果要实现cfDNA分析的有效临床整合,需要仔细了解这种方法的优点和局限性,以正确解释结果,用于指导临床决策。
柱式法提取步骤(参考)
1.转移 30µl Proteinase K 至 2.0ml 离心管中。
2.转移 0.6ml 血浆或其它液体样品至装有 Proteinase K 离心管中。
3.加入 0.6ml Buffer ACL 和(可选)5µl Carrier RNA 至样品中,涡旋混匀 15 秒。60℃水浴
4.加入 0.3ml 异丙醇至样品中,涡旋混匀 15 秒。室温放置 3 分钟。
5.把 HiPure Viral Mini Column 装在 2ml 收集管中。转移一半体积(750µl)混合液至柱子中。
6.倒弃滤液,把柱子装回收集管中。转移剩余混合液至柱子中。13,000 x g 离心 1 分
7.把柱子装在新的收集管中。加入 500µl Buffer GW1(已用乙醇稀释)至柱子上。13,000
8.倒弃滤液,把柱子装回收集管中。加入 500µl Buffer GW2(已用乙醇稀释)至柱子中。
9.倒弃滤液,把柱子装回收集管中。加入 500µl Buffer GW2(已用乙醇稀释)至柱子中。
10. 倒弃滤液,把柱子装回收集管中。13,000 × g 离心 2 分钟。
11. 将柱子装在新的 1.5ml 离心管中。60℃进一步干燥柱子 5 分钟。
12. 将柱子装在新的 1.5ml 离心管中。加入 30~50µl Buffer AE 或灭菌水至柱子的膜中央。
放置 3 分钟,13,000 × g 离心 1 分钟。
13. 丢弃 DNA 结合柱,把 DNA 保存于 2~8℃,长期保存需保存于-20℃。
磁珠法提取步骤(参考)
1. 在2.0ml离心管中,加入30µl Proteinase K和525µl MagIso Beads.
2. 转移600µl血浆至含蛋白酶K的离心管中。振荡混匀5秒。
3. 加入900µl Buffer ML至样品中,涡旋混匀15秒。室温或至55度放置10分钟,其间颠倒混匀次数。
4. 转移至磁力架上,静置3~5分钟吸附磁珠。小心吸弃所有溶液。
5. 加入600ul Buffer MW1,涡旋混匀15秒。
6. 转移至磁力架上,静置2分钟吸附磁珠。小心吸弃所有溶液。
7. 加入600ul 75%乙醇,涡旋混匀15秒。
8. 转移至磁力架上,静置2分钟吸附磁珠。小心吸弃所有溶液。
9. 重复第7-8步一次。
10. 空气干燥7~10分钟。
11. 加30~50µl 预热至55oC的Elution Buffer或灭菌水等缓冲液,涡旋打散磁珠。静置3~5分钟,其间轻轻振荡1~2次加速DNA溶解。
12. 转移至磁力架上,静置3分钟。转移DNA溶液至新的1.5ml离心管中。
| 货号 |
试剂名称-(GBCBIO) |
| D3206 |
无细胞游离DNA提取试剂盒 |
| M2105 |
磁珠法游离DNA提取试剂盒 |
1.Snyder M W, Kircher M, Hill A J, et al. Cell-free DNA comprises an in vivo nucleosome footprint that informs its tissues-of-origin[J]. Cell, 2016, 164(1-2):57.
2.捷倍斯生物官网
品牌优势
GBCBIO
--自主品牌--物美价廉--
服务优质
广州捷倍斯生物科技有限公司(GBCBIO Technologies)专注于生物试剂与诊断原料的研发、生产与销售,致力于提高国产生物试剂的竞争力。自主品牌----GBCBIO®牌核酸纯化试剂盒、ECL发光液、蛋白定量试剂盒与高端的表面活性剂等已为广大的科研与工业用户所使用,产品达到同类进口品牌的品质,具有物美价廉的特点!
捷倍斯生物可以提供专业和完善的核酸分离纯化解决方案,有硅胶柱法、磁珠法与溶液直接法的核酸纯化产品,在二代测序的样品前处理方面有着专业的技术与积累,有完善的针对唾液、血液与血浆等样品的保存、运输与高通量核酸纯化等整套的解决方案。 在诊断试剂原料方面,捷倍斯生物可以提供生物染色剂、高端的表面活性剂、显色底物、生物缓冲剂以及酶制剂与其稳定剂等系列产品。
视质量如生命的我们,以“做值得交往的人,做值得信赖的产品”为信念,期望通过我们努力的能够为您提供优质的产品与贴心的服
务。
公司官网:
http://www.gbcbio.cn/
服务热线:
020-82160415
公司邮箱:
genebase@vip.163.com
地 址:
广州市番禺区石楼镇清华科技园A4栋502
 游离核酸的来源
游离核酸的来源




