聚-γ-谷氨酸(γ-PGA)是一种生物衍生的水溶性、可食用、保湿、非免疫原性聚合物。枯草芽孢杆菌纳豆菌是一种野生型γ-PGA生产者,最初从日本发酵纳豆中分离出来,其活性已被证明通过染色体外DNA维持机制的离子特异性激活而增强。根据循环经济原则,可扩展的大型藻类生物质已被评估为γ-PGA的基质,在产量和材料成分方面都显示出巨大的潜力。通过马蒂亚·帕拉蒂、凯瑟琳·菲利普、芭芭拉·门德雷克、大卫·汤罗、易卜拉欣·哈利勒、菲德琳·楚恩布-马加亚等学者研究发现,使用机械方法对冻干海藻进行全细胞预处理,灭菌,随后接种枯草芽孢杆菌纳豆菌。高剪切混合被认为是最合适的预处理技术。补充的 L. digitata (9.1 g/L)、S. latissima (10.2 g/L)、A. esculenta (13 g/L) 显示出与标准 GS 培养基 (14.4 g/L) 相当的 γ-PGA 产量。6月份,L. digitata的纯γ-PGA产量最高(平均4.76 g/L),与GS培养基相当。此外,预处理的 S. latissima 和 L. digitata 复合物培养基能够分别以 8.6 和 8.7 g/L 的速度进行高摩尔质量 γ-PGA 生物合成。与标准GS培养基相比,藻类衍生的γ-PGA显示出显著更高的摩尔质量。

γ-聚谷氨酸是什么?
γ-聚谷氨酸(γ-PGA)是一种蛋白质样化合物,由通常被认为是安全的微生物自然产生,其显示出生物相容性和可控的化学变异性。从工业角度来看,γ聚谷氨酸具有化学多功能性、水溶性和非免疫原性使这种生物材料特别适合生物修复等。
芽孢杆菌可以生产γ-PGA
通过酶决定的γ-PGA聚合,所有野生型生产者都可以根据环境队列定制材料的特性(图1)。迄今为止,许多芽孢杆菌家族已被证明可以产生大量具有不同摩尔质量和立体化学性质的γ-PGA。聚谷氨酸合酶 (pgs) 膜间酶复合物负责 D/L-谷氨酸外消旋混合物的聚合。与其他酶类似,不同离子的存在会极大地影响pgs复合物中一种或多种生物催化组分的活性,从而导致γ-PGA性质的显着变化。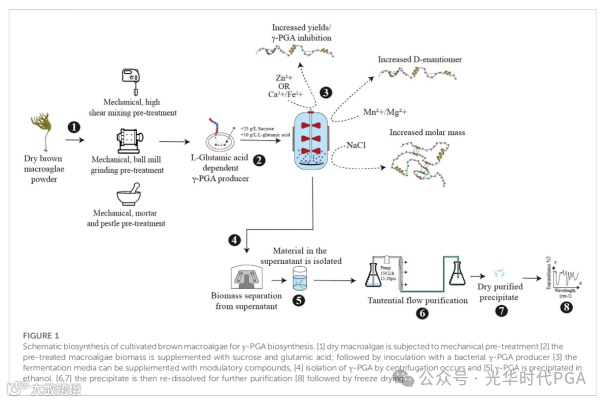
众所周知,海藻是碳水化合物、蛋白质、抗氧化剂和纤维物质的绝佳来源;英国海岸特有的海带、Saccharina latissima 和 Alaria esculenta 是三种全年生长的大型藻类物种(图 2),虽然它们都是棕色海藻家族的一部分,但在碳、抗氧化剂、蛋白质物质和灰分/成分方面都表现出很大差异。为此,我们评估了不同藻类对枯草芽孢杆菌纳豆菌γ-PGA产量和化学成分的影响。还评估了栽培期间(4月至8月)发生的聚合物生化变异对枯草芽孢杆菌纳豆菌γ-PGA生物合成的影响。 
试验设计
1.1微生物的处理设计
从国家工业和海洋细菌收集获得的枯草芽孢杆菌纳豆菌被冷冻干燥并保持在 -20°C。使用前,将培养物复苏并在 37°C 下在胰蛋白胨大豆琼脂上生长过夜。选择高度粘液类菌落,并在含有 100 mL 胰蛋白胨大豆肉汤培养基的摇瓶中在 37°C 下有氧生长 24 小时。
所有大型藻类复合物培养基均由 40 g/L 海藻(表 1 中指定的来源)组成,并辅以 10 g/L L-谷氨酸盐和 25 g/L 蔗糖。使用从购买的NaOH将所有培养基的pH值调节至6.8。
所有复杂培养基均使用去离子水制备,并在115°C下高压灭菌15分钟。将蔗糖溶液单独过滤灭菌,并单独加入培养基中。
1.2栽培参数的设计
在 250 mL 摇瓶中进行批量培养。通过在37°C浴中解冻冷冻细胞接种培养物,并将5%的接种物添加到培养基中。生长温度保持在37°C,在培养期的96 h内将搅拌设置为150 rpm。在工作体积为 4 L 的 7 L 发酵罐中进行中等规模的间歇培养。培养基以 5%接种,发酵剂培养 24 小时。培养温度保持在37°C,培养物的pH值保持在6.8,发酵开始时,搅拌速度和风量分别设置为150 rpm和2.0 L/分钟。在枯草芽孢杆菌纳豆菌栽培过程中,发酵培养基的粘度显著增加,搅拌速度和气流均应调整,以保持氧气供应保持在40%以上。为此,搅拌速度提高到250 rpm,空气流速提高到3 L/分钟。
通过无菌除去 0.5 mL 等分试样并在四分之一强度的 Ringer 溶液中依次稀释它们,定期监测菌落形成单位。对于每个样品,将 0.5 mL 以 10 倍的步长连续稀释至 10–7.通过将 1 片溶解在 1 L 烧瓶中的 500 mL 去离子水中来制备林格溶液。通过连续稀释到含有营养琼脂的培养皿上来测定细胞活力。按照Miles和Misra方法接种每种稀释液,并使用每种稀释液20μL。在37°C下孵育过夜后计数菌落,生物体浓度表示为Log10[CFU/毫升]。

1.3γ-PGA的分离和纯化
为了进行物质分离,将培养液从发酵容器中取出,并使用离心机以17,000×g离心30分钟以除去细胞。将上清液倒入3体积的冷乙醇中,在5°C下静置过夜,在静态条件下沉淀。通过0.22μm纸过滤器过滤收集所得沉淀物。随后将沉淀物冻干,运行 36 小时。将白色/绿色/棕色干粉在室温下储存在干燥器中,直至进一步使用。为了进一步纯化,将获得的干粉重新溶解到去离子水中,并从Repligen截断30 KDa的20 cm MidiKros色谱柱。将纯化的溶液用3体积的冷乙醇重新沉淀,并在5°C下放置过夜。沉淀后,收集聚合物并冻干。

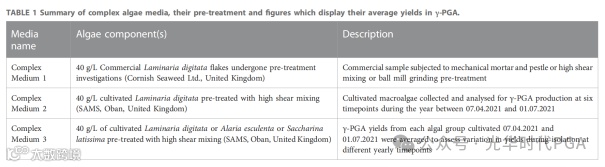
1.4枯草芽孢杆菌纳豆菌在标准培养基上的生长
枯草芽孢杆菌纳豆菌在标准培养基上的生长情况总结在图3中。图 3 中显示的生长曲线表明,高浓度的 NaCl (50 g/L) 导致 t = 72 和 t = 96 小时之间的细胞活力降低。我们的数据表明,在0 g/L和25 g/L的NaCl之间,定义培养基的生长没有显着差异(p > 0.05)。此外,添加2.78 mMol MnSO4与 0 g/L 和 25 g/L NaCl 浓度相比,似乎具有相似的细胞增殖和活力。
在放大阶段,培养体积从250 mL增加到4,000 mL似乎对枯草芽孢杆菌纳豆菌细胞生长或活力没有显着影响(p > 0.05)(图4)。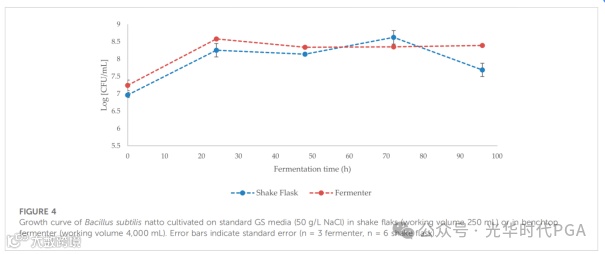
1.5复杂藻类介质的粒径
分析藻类组分的初始和机械处理后的粒径,以评估培养过程中养分可用性的潜在变化。不同颗粒的直径已在图5、图6中显示。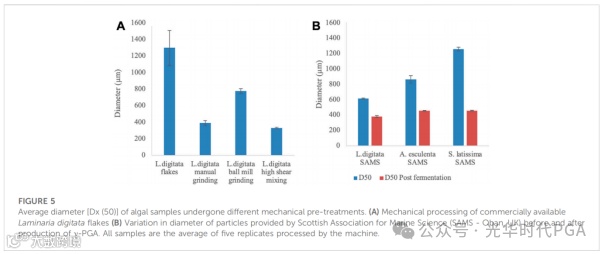
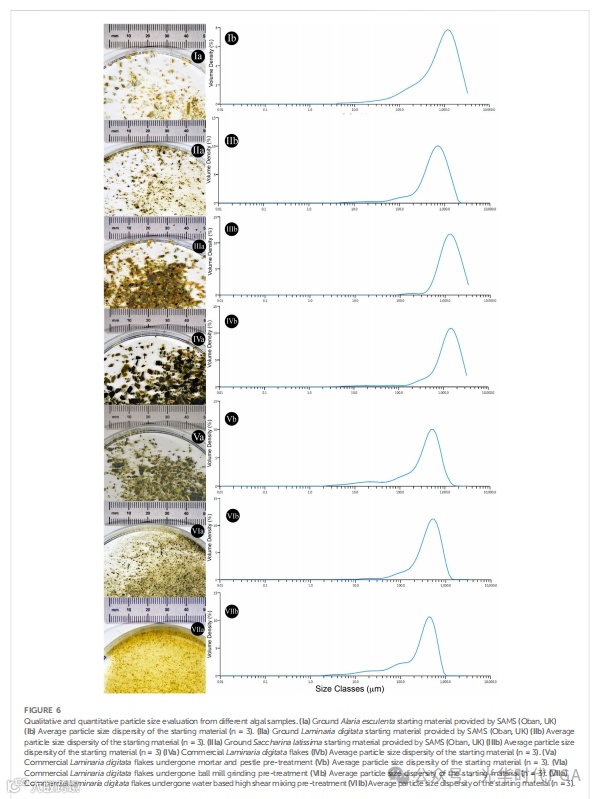
图6.对不同藻类样品进行定性和定量粒度评估。(一)SAMS提供的磨碎的 Alaria esculenta 起始材料 (Ib) 起始材料的平均粒径分散度 (n = 3)。(二一)SAMS提供的地面海带起始材料 (IIb) 起始材料的平均粒径分散度 (n = 3)。(三一)SAMS提供的磨碎的 Saccharina latissima 起始材料 (IIIb) 起始材料的平均粒径分散度 (n = 3) (IVa) 商业海带片 (IVb) 起始材料的平均粒径分散度 (n = 3)。经过研钵和研杵预处理(Vb)的市商业海带片起始材料的平均粒径分散度(n = 3)。(VIa)经过球磨机研磨预处理(VIb)的商用海带片 起始材料的平均粒径分散度(n = 3)。(七)商业海带片经过水基高剪切混合预处理(VIIb)起始材料的平均粒径分散(n = 3)。
当采用不同的机械预处理方法时,观察到粒径的显着变化(p < 0.0001)(图5A)。在预处理方法中,在手动研磨和高剪切混合之间似乎没有观察到粒径的显着变化(p > 0.99)。图5A还表明,与球磨机磨削相比,手动研磨获得的粒径更低;然而,与目视观察相比,这些结果似乎有所不同(见图6V-VI)。图5B表明,三种物种的初始藻类粒径存在显着差异(p < 0.0001),在高剪切混合和γ-PGA生产后的结果相似(p < 0.0001)。
1.6枯草芽孢杆菌纳豆菌在复杂藻类培养基上的生长
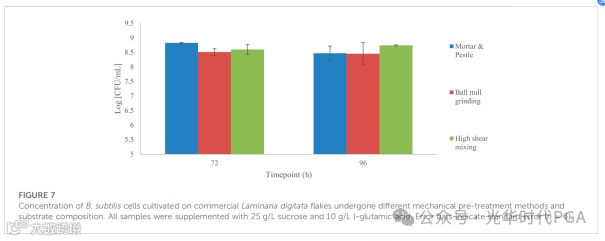
在基质优化研究期间,评估了不同的海藻预处理。研究了三种机械预处理技术:球磨机研磨、研钵和研杵以及高剪切混合。图7总结了这项调查的结果。枯草芽孢杆菌在不同时间点的生长差异有统计学意义(p < 0.01)。此外,枯草芽孢杆菌纳豆菌在仅添加 7 g/L L-谷氨酸的商业海带片状培养基(无预处理)上的生长,三个重复中只有一个在所有时间间隔内显示生长,终浓度为 6.43 CFU/mL;该数据集使我们能够了解,尽管藻片的潜在良好营养来源,但藻片的预处理和补充都更可取,以获得高浓度的枯草芽孢杆菌纳豆菌。
1.7γ-PGA的鉴定
借助傅里叶变换红外分析技术研究了γ-PGA的化学成分。图8表明,γ-PGA实际上是生产的。然而,令人惊讶的是,与切向流过滤后的 γ-PGA 商业样品相比,复杂的藻类废物介质的纯度似乎没有显着变化。

γ-PGA的额外纯化是通过切向流过滤实现的,其中肽和其他小杂质杂质通过30,000个Da孔;γ-PGA保持在截留物内。总体而言,摇瓶和 4L 发酵罐均表明原始产量和切向后流产率均存在显着差异。图 8 表明,对于标准 GS 培养基 4L 发酵,使用 MnSO 可获得最高的 γ-PGA 产量,补充 25 g/L NaCl 培养基。这在摇瓶实验中正好相反(见图9)。然而,GS培养基25 g/L NaCl和25 g/L NaCl + MnSO的收率没有显著差异。在摇瓶或 4L 发酵罐中,0 和 50 g/L NaCl 培养基的产量没有显着差异(图 9)。不同的是,与0或50 g/L NaCl相比,使用25 g/L NaCl的培养与0 g/L NaCl的培养之间存在显着差异(p < 0.0025)。总体而言,在摇瓶或4L发酵罐中培养的原始产量没有显著差异(p = 0.27)。
当材料进一步纯化时,与从4L发酵罐中获得的产量相比,从摇瓶中获得的产量显着不同(更高)。总体而言,在摇瓶的0 g/L NaCl培养基中获得的纯γ-PGA产量最高,而在4L发酵罐的0 g/L NaCl培养基中获得纯-PGA的产量最高。与4L发酵罐相比,从摇瓶中获得的纯材料产量总体更高。
3.6 γ-PGA不同机械预处理的产率
图 10 中总结的数据表明,原始和切向后流动处理样品之间的 γ-PGA 产量存在显著差异 (p = 0.0001)。此外,数据表明,预处理显着影响原始产量和PTF γ-PGA产量。正如预期的那样,切向流处理后的γ-PGA百分比在预处理方法之间从37.5增加到59.6再到75.2。

3.7 不同栽培时间海带复合物培养基的γ-PGA产量
图11评估了藻类养殖年时间点对γ-PGA产量的影响,对于标准培养基培养,未加工沉淀和纯化沉淀物之间的产量存在显著差异(p < 0.0001)。不同的是,原始或纯化的γ-PGA产量的年度时间点收集之间没有显著差异(分别为p = 0.41和p = 0.46)。

3.8 不同年点Alaria esculenta、Laminaria digitata和Saccharina latissima复合培养基γ-PGA产量变化
培养了由Alaria esculenta或Laminaria digitata或Saccharina latissima组成的培养基,用于γ-PGA生物合成。尽管γ-PGA产量的变化很明显(参见图12中的标准差条),但统计分析表明,三种大型藻类之间的γ-PGA产量没有显著差异(p = 0.11)。如之前的图10所示,γ-PGA产量在年度时间点上没有显著差异。

3.9 γ-PGA的物理性质
尽管聚合物产量对工艺的总成本有很大影响,但决定材料价值的主要方面之一是其性能。为此,在表2中分析和总结了材料的物理化学性质。

结论
1. 在三种常见的预处理方法中,高剪切混合最适合γ-PGA合成。
2. 数据表明,当分别在7月和4月的相反培养时间点分离时,L. digitata和S. latissima都能够支持高摩尔质量无定形γ-PGA(4,500 kDa)的合成。
3. 在 5 月份收集时,这三种大型藻类的 γ-PGA 产量最高。
4. 从标准GS培养基中,枯草芽孢杆菌纳豆可以在渗透压具有挑战性的条件下生长,暗示了能量优势,非无菌,嗜盐γ-PGA的产生。
5. 在锥形瓶中,25 g/L NaCl GS培养基补充有2.48 mM MnSO4导致γ-PGA的产量最高。
6. 在4-L发酵罐中,存在Mn离子可能对高γ-PGA生物合成具有抑制活性,这与先前观察到的一致。

引用
Acircular bioprocess application of algal-based substrate for Bacillus subtilis natto production of γ-PGA.


微信号|GH-PGA
官网|www.ghpga.com



