



英文标题:Targeting SPHK1 in Macrophages Remodels the Tumor Microenvironment and Enhances Anti-PD-1 Immunotherapy Efficacy in Colorectal Cancer Liver Metastasis
中文标题:巨噬细胞靶向SPHK1重塑肿瘤微环境,增强抗PD-1免疫治疗结直肠癌肝转移的疗效
发表刊物:Cancer Communications
影响因子:24.9/Q1(2025 IF)
发表时间:2025年7月
通讯作者:方媛、沈智勇
作者单位:广州南方医科大学南方医院放射肿瘤科、广东省胃肠道肿瘤精准医学重点实验室等
涉及多因子检测:AAM-INF-1(小鼠40个炎症因子抗体芯片)
详情:https://www.raybiotech.com/mouse-inflammation-array-c1-aam-inf-1


英文标题:Targeting SPHK1 in Macrophages Remodels the Tumor Microenvironment and Enhances Anti-PD-1 Immunotherapy Efficacy in Colorectal Cancer Liver Metastasis
中文标题:巨噬细胞靶向SPHK1重塑肿瘤微环境,增强抗PD-1免疫治疗结直肠癌肝转移的疗效
发表刊物:Cancer Communications
影响因子:24.9/Q1(2025 IF)
发表时间:2025年7月
通讯作者:方媛、沈智勇
作者单位:广州南方医科大学南方医院放射肿瘤科、广东省胃肠道肿瘤精准医学重点实验室等
涉及多因子检测:AAM-INF-1(小鼠40个炎症因子抗体芯片)
详情:https://www.raybiotech.com/mouse-inflammation-array-c1-aam-inf-1
英文标题:Targeting SPHK1 in Macrophages Remodels the Tumor Microenvironment and Enhances Anti-PD-1 Immunotherapy Efficacy in Colorectal Cancer Liver Metastasis
中文标题:巨噬细胞靶向SPHK1重塑肿瘤微环境,增强抗PD-1免疫治疗结直肠癌肝转移的疗效
发表刊物:Cancer Communications
影响因子:24.9/Q1(2025 IF)
发表时间:2025年7月
通讯作者:方媛、沈智勇
作者单位:广州南方医科大学南方医院放射肿瘤科、广东省胃肠道肿瘤精准医学重点实验室等
涉及多因子检测:AAM-INF-1(小鼠40个炎症因子抗体芯片)
详情:https://www.raybiotech.com/mouse-inflammation-array-c1-aam-inf-1

涉及其它技术:单细胞RNA测序(scRNA-seq)、转录组测序(RNA-Seq)、质谱流式(CyTOF)等
检测样本:肿瘤、细胞培养上清
全文下载:https://doi.org/10.1002/cac2.70047

SPHK1在CRLM的TAMs中高表达且与不良预后相关
通过单细胞RNA测序(scRNA-seq)和免疫荧光分析,发现SPHK1在CRLM组织的TAMs中显著高表达(图1A-D)。
临床数据分析显示,SPHK1高表达的CRC患者总体生存率较低,尤其在CD68高表达的亚组中预后更差(图1E-G)。
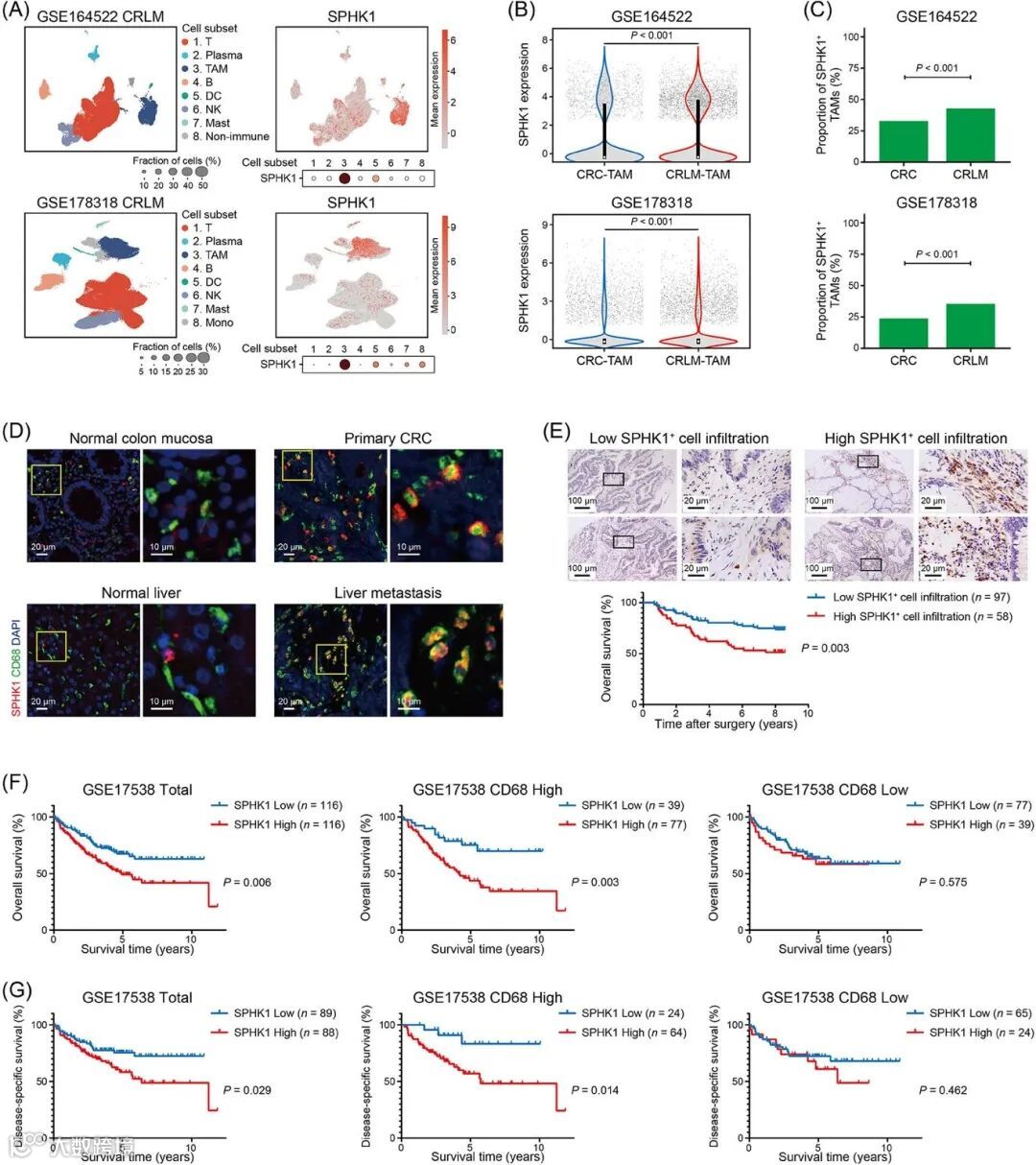
图1
抑制SPHK1可减少肝转移并改善免疫微环境
在CRLM小鼠模型中,SPHK1抑制剂(PF543、SKI II)或基因敲除(SPHK1−/−)显著减少肝转移灶数量和体积,延长生存期(图2A-J)。
质谱流式(CyTOF)和流式分析显示,SPHK1缺失导致TAMs减少,CD8+ T细胞浸润增加,且CD8+ T细胞耗竭标志物(PD-1、TIM3)下调,效应分子(IFN-γ、GZMB)上调(图3A-H)。

图2

图3
SPHK1通过S1P-S1PR2轴激活NLRP3炎症小体
利用AAM-INF-1炎症多因子检测及RNA测序分析表明,SPHK1缺失或抑制降低NLRP3和IL-1β的表达(图4A-D)。
S1P通过结合S1PR2激活NF-κB和HIF-1α信号通路,促进NLRP3炎症小体组装和IL-1β分泌(图5A-K)。

图4

图5
IL-1β通过ADAM17介导CD8+ T细胞功能障碍
利用AAM-INF-1炎症多因子检测IL-1β刺激的CRC细胞高表达单核细胞趋化因子(CCL2、CCL7)和ADAM17,促进TAM招募并诱导CD8+ T细胞表面CD62L丢失,加剧耗竭(图6A-H)。
临床样本中,SPHK1与ADAM17表达呈正相关,且双高表达患者预后最差(图6H)。

图6
靶向SPHK1增强抗PD-1疗效
联合SPHK1抑制剂与抗PD-1治疗显著抑制肝转移,延长生存期,并增加CD8+ T细胞活性(图7A-G)。
在放疗联合免疫治疗模型中,SPHK1抑制剂进一步改善疗效并减轻肝损伤(图7H-J)。
临床数据分析显示,SPHK1高表达与ICI治疗耐药相关(图7K-N)。

图7



专题集锦 | 信号通路、蛋白翻译后修饰(PTMs)、肿瘤癌症、肺癌、胃癌、肝癌、胰腺癌、乳腺癌、甲状腺癌、鼻咽癌、结直肠癌、巨噬细胞、自噬、泛素、凋亡、焦亡、铁死亡、免疫、炎症、脓毒症、衰老、阿尔茨海默病、肥胖、糖尿病、肾病、血管生成、心脑血管、肝病、呼吸、结核病、皮肤、眼科、妇科、干细胞、外泌体、类器官、组织工程、骨科、新药研发、中医药、多糖、神奇动物、病毒、麻醉……

请点击以上链接查阅详情,或私信、电话 020-3160 8909 与我们联系…

请点击以上链接查阅详情,或私信、电话 020-3160 8909 与我们联系…









