

2023年3月16日,斯微(上海)生物科技股份有限公司非复制mRNA瘤内注射药剂SW0715获得IND申请(CDE受理号:CXSL2300196)。SW0715是国内首个First in class级别的DDS核酸抗肿瘤创新药。采用纳米脂质体技术递送人源化细胞因子IL-12诱导辅助性T细胞(Th)分化成Th1极性细胞。Th1细胞通过T细胞分泌IFN-γ,激活细胞伤害型CD8+T细胞,实现杀伤肿瘤细胞的目标。拟用于晚期且无有效治疗手段的实体瘤(如黑色素瘤、乳腺癌、小细胞肺癌、胃癌、结直肠癌等)的治疗。
药物递送系统简称DDS(Drug Delivery System)作为靶向治疗的核心技术,在恰当的时机“时间”将适量/提供治疗需求的最小剂量“小剂量”的药物递送到正确的位置“空间”(别称“时间/空间”双靶向治疗模式)。因为减少了使用药物的剂量,增加药物有效利用率,提高疗效,实现降低成本,减少毒副作用的目的。

回顾DDS近70年的演化进程,自1950年代起,不同形式的制剂如:片剂、胶囊、软膏和液体制剂(含生物制剂)等都基于四种机制:即扩散、溶解、渗透和离子交换控制药物释放。与传统的速释制剂相对应,第一代DDS制剂的主要目标在于给药后尽可能延长药物在体内“持续”的时间,“延长”释放周期。第一代DDS系统的“里程碑”包括 Spansule[1]12小时缓释;血药浓度检测等技术(图1:第一代DDS试剂缓释型与药物浓度调控型)。是目前批准上市的原型药或仿制药剂型,数量,技术成熟度最高[2]。
80年代,伴随大/小分子药物、蛋白与蛋白工程、基因工程、核酸药物、IT以及影像学等多学科交叉技术的发展与应用,通过对药物或药物载体等进行改性、修饰,改变药物载体的形态结构,甚至采用适当的释放机制如细胞载体、病毒载体、纳米胶囊等技术的成熟,正式迈入第二代DDS给药系统。
1952年发布的Spansule®技术开启了12小时持续DDS的篇章。该技术通过药物表面构建的涂层屏障来限制进入胃肠道的药物核心的溶解速率(如:Dexedrin(递送硫酸右旋苯丙胺),Contac 600(递送苯丙醇胺盐酸盐和马来酸氯苯那敏)。四年后,加压计量吸入技术(MDI)的问世,开启了吸入型DDS的历史[3]。1969年,干粉吸入型DDS获批[4]。1979年,Transdermal Scop®的批准使市场上有了透皮型DDS制剂[5]。在1950年代至1980年代伴随药物释放的数学模型得到开发,持续释放口服或透皮药物的时间也从最初的12小时延长到了24小时。以Spansule®技术为“里程碑”,口服与透皮制剂为代表的第一代DDS制剂趋向成熟。

每天多次(MDI)或连续皮下注射胰岛素(CSII),控制血液中葡萄糖浓度接近正常血糖水平,已经成为1型糖尿病(T1DM)患者的常识。早期的胰岛素泵,例如1975年第一台胰岛素泵Biostator;1978年首批商用胰岛素泵Autosyringe通过计算血糖数据,控制胰岛素的输注。基于性能(如体积大,输液速度不易调节)和稳定性困扰(频繁更换电池、易脱针、注射器和管路堵塞等),仅限于在餐前以特定的速度连续注射胰岛素,尚无法实现调制释放(在正确的时间输送需要量的胰岛素)。(图2.胰岛素输送系统的进步与市场主要上市产品(数据源自公开信息派思维新整理)
初代DDS技术的关键点是,控释制剂几乎专用于 12 小时或 24 小时递送的口服制剂,并在某种程度上用于透皮制剂。对于口服制剂,体外药物释放曲线通常与体内药代动力学(PK)相关。因此,需要调整制剂配方,药物结构,给药微环境修饰DDS的药物类型,芯片与智能化技术,实现输送系统的自动化、功能化、实用化、舒适化等需求。2010年美敦力发布的胰岛素输送系统,包含葡萄糖传感器、驱动器和控制胰岛素释放的反馈系统等功能,为用户使用提供了便利性与舒适性。目前该市场以约50%的年增长率快速成长[6]。


第二代(1980-2017)DDS(例如,脂质体、纳米颗粒、微球和基因传递)纳米药物和智能化输送系统得到了更多关注。1995年,脂质体Doxil®成为第一个上市的纳米药物(治疗HIV相关的卡波氏肉瘤和多发性骨髓瘤)[7]。2005年上市的 Abraxane®是第一个基于纳米技术的靶向DDS制剂(用于局部晚期或转移性三阴性乳腺癌)。2015年,Spritam®是第一个基于3D打印技术的DDS新药(适用于局部性癫痫)。2017年,FDA批准第一个基因治疗DDS药物Kymriah®的上市(CAR-T细胞疗法)[8],同年FDA获批了全球首款数字药物Abilify MyCite®(在抗精神病药物Abilify内部植入盐粒大小的微芯片)。服用药物的同时,借助通讯设备帮助医护人员跟踪患者的服药情况。2018年,FDA批准首个非病毒给药系统的基因治疗药物 Onpattro®(适应症为遗传性转甲状腺素蛋白淀粉样变性)。2019年,首个口服胰高血糖素样肽-1(GLP-1)受体激动剂药物获得FDA批准上市(治疗2型糖尿病)。2021年,FDA批准了首个新冠疫苗Comirnaty®(COVID-19 mRNA疫苗)[9]。
DDS制剂包含溶液、混悬液、乳剂、散剂、颗粒剂、胶囊剂到片剂等所有剂型,第二代DDS给药系统采用胶束、脂质体、乳剂、微球、胶囊等多种药物包被与修饰技术改变药物载体的形态结构学可以改善难溶性药物的溶解度,或者在药物表面构建一个保护屏障,保护药物在递送过程中的非特异性清除或各类消化酶降解,提高药物的稳定性,调控代谢速率。随着治疗方式从小分子扩展到蛋白质和多肽、抗体、核酸以及细胞(活细胞)载体等各种独特的药物递送技术也随之而来,以应对出现的挑战[10]。


DDS药物递送系统发展至今,无论是为持续药物输送而开发的第一代DDS Spansule技术,还是包括小分子、蛋白质和肽、单克隆抗体(mAb)、抗体毒素共聚物(ADC)、核酸和活细胞在内的第二代DDS提供的新的治疗功能,1)对药物本身的结构改造;2)药物微环境的修饰;3)药物输送系统的设计,通过控制药物与其微环境之间的相互作用来促进药物递送。以其实现增加药物有效利用率,减少药物使用剂量,提高疗效降低治疗成本与减少毒副作用的目的。
派思维新及其所属团队创建了一种基于吞噬细胞的智能化载药纳米微粒靶向递药系统,为基于活细胞的高效递药系统的研发提供新的技术平台。简而言之:采用AI(人工智能模拟)技术与PBMD数据库,构建世界上首个M1/M2极性吞噬细胞的环状RNA(CirRNA)数据库,用于高通量筛选候选药物。团队首创的双环状核酸药物结构可将环状RNA(CirRNA)包埋在甘露糖-3/5(mannose3or5)修饰的载药磁性纳米微粒中,到达胞内ROI区域后,通过设定的程序将包埋的核酸药物提示给幼稚吞噬细胞。载药磁性纳米微粒在胞内降解后,CirRNA通过幼稚吞噬细胞以及抗原提示细胞的分解,合成与表达,有望攻克尚无药物治疗的疾病包括遗传疾病和其他难治疾病[11]。


1.通过人工智能模式(AI)高通量筛选治疗靶点,构建世界上首个M1/M2极性吞噬细胞的环状RNA(CirRNA)数据库。诱导M1/M2极性吞噬细胞的CirRNA,其治疗靶点及其作用机制
2.通过甘露糖-3/5(mannose)修饰载药磁性纳米材料,递送和富集到骨损伤部位的巨噬细胞内,改变巨噬细胞胞内特定类型的circRNA丰度,降低其功能,或者诱导naive巨噬细胞为M1/M2表型的作用机制与靶点信息
3.以naive巨噬细胞为靶细胞,通过M1/M2极化吞噬细胞的免疫调节可能拓展的新技术,新应用领域的研究
1.肿瘤研究平台:包括肿瘤药理平台如传统肿瘤平台(CDX PDX,同源小鼠模型,原位肿瘤药效模型等);特色药理平台如人源化小鼠模型,肿瘤耐药体内模型,基于小动物成像系统的模型,类器官相关模型,基因编辑小鼠模型等相关模型。
2.体外研究平台:体外药物筛选平台可实现包括肿瘤靶点验证技术及多种肿瘤免疫体外分析技术。2D/3D细胞培养,体外和体内药物靶点抑制及下游信号通路分析等。
3.炎症免疫疾病药效评价模型平台:如类风湿性关节炎(RA, rheumatoid arthritis),过敏性脑脊髓炎模型((EAE, experimental allergic encephalomyelitis),银屑病((Psoriasis),特应性皮炎及湿疹(AD, atopic dermatiti$),炎症性肠病(IBD, Infectious Bursal Disease)等相关疾病结肠炎(colonists),其他常规炎症(others inflammatory disease model)。
4.药代动力学平台:提供药物的体内药代动力学,毒代动力学数据以及药物发现阶段及Pre-IND阶段的开发筛选,测试化合物包括小/大分子药物,蛋白和多肽,抗体以及ADC药物等。
公司拥有3000平、上下六层的办公室一级动物房、实验室,配备有FACS流式平台、多因子检测平台(MSD S600)、小动物活体成像平台、小动物手术平台(麻醉机&小动物脑定位仪),Countstar细胞分析仪,SCIEX Triple Quad 5500+质谱仪、QX100 Droplet Digital PCR仪、MD M5多功能酶标仪、PE多功能荧光分析仪,临床中心实验室配备有全自动智能染色机,病理平台配备有组织自动脱水机、组织包埋机、组织切片机、组织摊烤片机。
上海派思维新生物为全内资公司,并有中国人类遗传资源国际合作临床试验备案。临床前实验室为P2实验室,临床中心实验室遵循CAP认证国际质量管理标准,实验动物中心为SPF级动物房,可以饲养超3000笼位的小动物。
套用禅宗提出的三重境界「看山是山,看山不是山,看山还是山」。DDS的发展进程从初代的持续缓慢释放,以Spansule 12小时释放技术为“里程碑”,实现了第一重境界。80年代至今的二代DDS。随着小分子药物、蛋白质和肽、抗体、核酸和细胞载体/细胞治疗等技术发展,以及AI、芯片为代表的人工智能技术的应用,通过药物表面修饰,给药微环境调节各种治疗方案的递送系统,在疾病的预防与治疗过程中备受关注。展望未来,伴随智能与信息化的进一步推进,第三代DDS系统可能延续三重境界的最后一重,为越来越多的药物提供更好更多的DDS递送系统,以适应多器官、多疾病等多种不同的给药需求。
Novopathway

2023
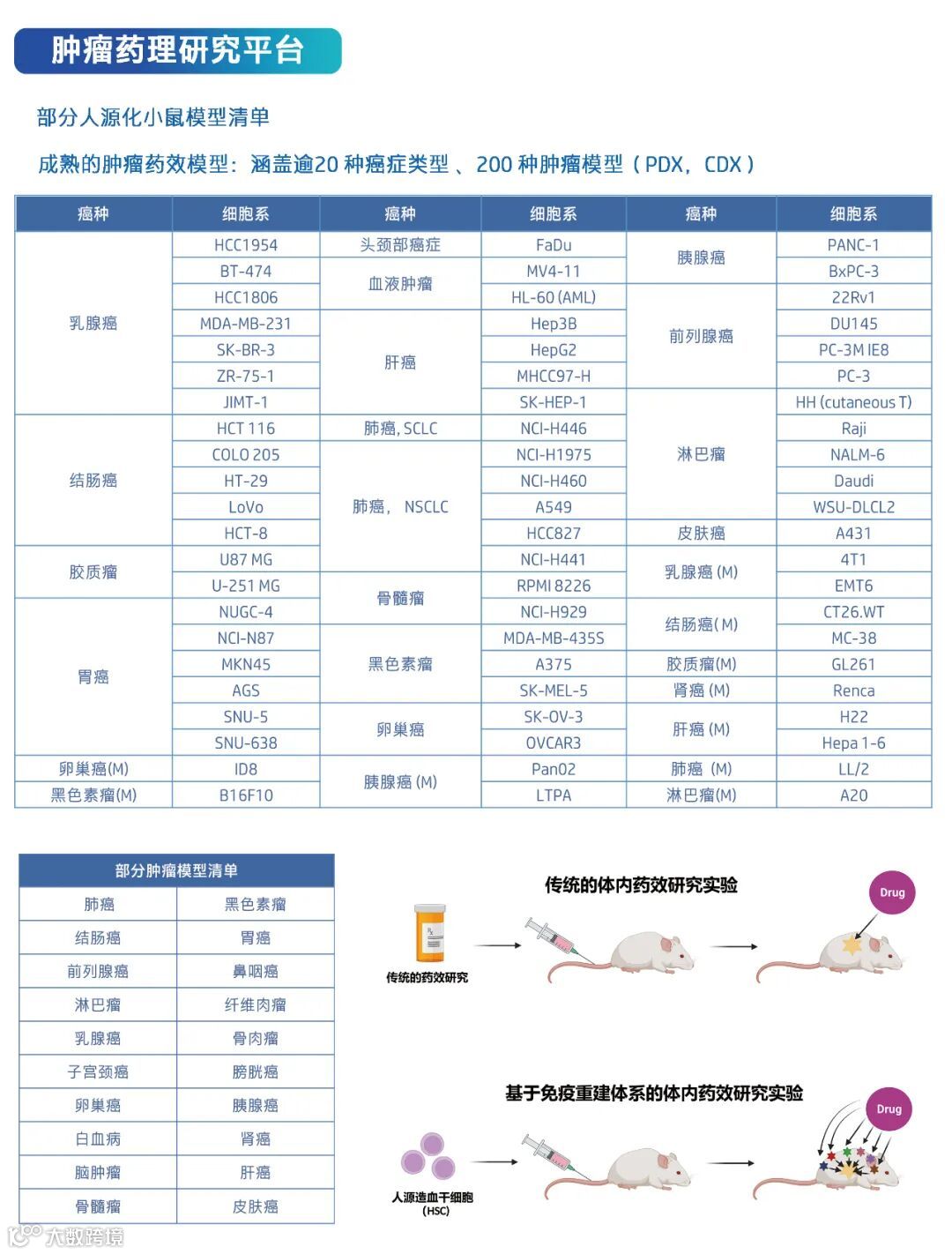
派思维新现有模型清单

更多信息
请登录派思维新官方网站
www.novopathway.com


- 上下滑动查看参考资料 -
[1]Berkowitz D., The effect of a long-acting preparation (spansule) of belladonna alkaloids on gastric secretion of patients with peptic ulcer., Gastroenterology. 1956 Apr;30(4):608-12.
[2]Haesun Park, Andrew Otte, Kinam Park.,Evolution of Drug Delivery Systems: From 1950 to 2020 and Beyond.,J Control Release. 2022 February ; 342: 53–65. doi:10.1016/j.jconrel.2021.12.030
[3]Hardwell A, Barber V, Hargadon T, et al. Technique training does not improve the ability of most patients to use pressurised metered-dose inhalers (pMDIs). Prim Care Respir J. 2011. March; 20 (1):92–6. doi: 10.4104/pcrj.2010.00088.
[4]Chang RYK, Chow MYT, Khanal D, Chen D, Chan HK. Dry powder pharmaceutical biologics for inhalation therapy.; Adv Drug Deliv Rev. 2021 May;172:64-79. doi: 10.1016/j.addr.2021.02.017. Epub 2021 Mar 8.
[5]Mazzo DJ, Fong EK, Biffar SE., A comparison of test methods for determining in vitro drug release from transdermal delivery dosage forms.J Pharm Biomed Anal. 1986;4(5):601-7. doi: 10.1016/0731-7085(86)80006-1
[6]Lal R, Leelarathna L., Insulin Delivery Hardware: Pumps and Pens. Diabetes Technol Ther. 2022 Mar;24(S1):S21-S34. doi: 10.1089/dia.2022.2502.
[7]Porche DJ., Liposomal doxorubicin (Doxil).J Assoc Nurses AIDS Care. 1996 Mar-Apr;7(2):55-9. doi: 10.1016/S1055-3290(96)80016-1
[8]Brudno JN, Kochenderfer JN., Recent advances in CAR T-cell toxicity: Mechanisms, manifestations and management.Blood Rev. 2019 Mar;34:45-55. doi: 10.1016/j.blre.2018.11.002. Epub 2018 Nov 14.
[9]Skowronski DM, De Serres G.,Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med. 2021 Apr 22;384(16):1576-1577. doi: 10.1056/NEJMc2036242. Epub 2021 Feb 17.
[10]Vargason AM, Anselmo AC, Mitragotri S. ,The evolution of commercial drug delivery technologies., Nat Biomed Eng. 2021 Sep;5(9):951-967. doi: 10.1038/s41551-021-00698-w. Epub 2021 Apr 1
[11]Ikehara Y, Niwa T, Biao L, Kojima N, et al.. A carbohydrate recognition-based drug delivery and controlled release system using intraperitoneal macrophages as a cellular vehicle., Cancer Res. 2006 Sep 1;66(17):8740-8. doi: 10.1158/0008-5472.CAN-06-0470
图文信息均汇总于专业期刊,如有错误欢迎指正!
往期推荐

2023-03-24

2023-02-15

2023-01-31
期待您的
分享
点赞
在看











