

骨质疏松症模型及其应用
现代医学将骨质疏松症(Osteoporosis,下文简称OP)分为原发性、继发性和特发性三大类。第一类原发性骨质疏松症(primary osteoporosis,POP),因增龄所致的体内性激素突然减少及生理性退行性改变所致,包括Ⅰ型绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)和Ⅱ型老年性骨质疏松症。第二类为继发性骨质疏松症,由疾病或药物因素诱发,如内分泌代谢病(糖尿病、甲状腺功能亢进症等)、肾脏疾病、肝脏疾病等。药物诱发如长期大剂量糖皮质激素的应用、肝素、免疫抑制剂等的应用。第三类为特发性骨质疏松症,多见于青少年,一般伴有遗传疾病史,女性多见,妇女哺乳期和妊娠期的骨质疏松症也往往列入此类。
由于骨质流失是隐匿的,骨质疏松症最初是无症状的,通常只有在第一次临床骨折发生后才能被诊断出来。其最常见的症状是疼痛,以腰背痛最为多见,其次是身长缩短、驼背,严重者可见骨折,常见部位为髋部、脊柱、腕部和肋骨。
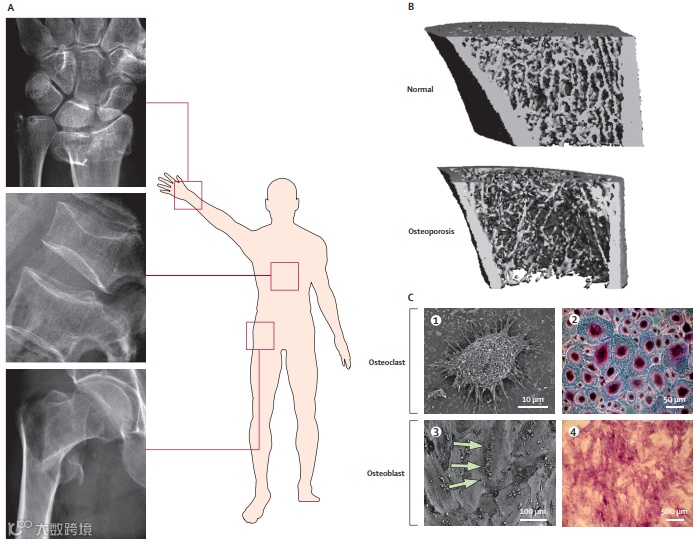
DOI:10.1016/s0140-6736(10)62349-5
OP发生机制主要是增龄(衰老)、体内性激素减少、药物和某些疾病等因素导致骨吸收与骨形成失调,骨矿物质和有机质等比例丢失,导致骨量减少和骨质疏松,进而易发生骨折。机体的骨量多少是由成骨细胞和破骨细胞功能的平衡决定的,成骨细胞形成新骨,破骨细胞造成骨吸收。当成骨细胞活性大于破骨细胞活性时,新骨形成大于骨吸收,骨量增加,反之骨量减少。OP形成的机制即破骨细胞活性相对增加,导致形成骨吸收大于骨形成的负平衡状态,从而使机体骨量减少、骨小梁结构破坏,骨组织生物力学性能减低、易于发生骨折。

骨质疏松症的病因和发病机制复杂,至今尚未完全明了,根据已了解的病因和发病机制,建立合适的、能反映疾病病理特征的动物模型,是研究不同途径药物抗OP药效学的关键。人类骨质疏松症是由于衰老进程(妇女绝经、老年退行性病变)及内分泌紊乱、营养不良、疾病及药物诱发等因素引起,针对以上因素,研究人员成功构建多种经典的、受到广泛认可的OP动物模型。目前常用来诱导OP的动物有大鼠、小鼠、 兔、羊、猪、狗和非人类灵长类动物以及斑马鱼等,造模方法有去势法(双侧卵巢切除、双侧睾丸切除等)、药物致骨质疏松法(糖皮质激素、维甲酸诱导等)、营养法(低钙饮食、低钠诱导等)、失用法(机械固定法,悬吊法等),以及一些特殊类型的造模方法如基因法(α,β-雌激素受体或芳香酶基因敲除)、脑源性造模法(破坏大鼠下丘脑弓状核)等,有的用单一种方法,有的两种或多种方法联合使用(去卵巢联合糖皮质激素、糖皮质激素法联合低钙饮食等)。
首次运用手术去势法可追溯到1969年,国外学者Saville采用手术方式摘除大鼠的双侧卵巢(OVX)后成功诱导OP症状,至此手术去势法构建PMOP动物模型得到广泛的认可及推广。目前去卵巢造模方法被广泛认为是绝经后骨质疏松症造模的金标准,也是FDA和WHO推荐的研究绝经后骨质疏松症模型。
造模方法:手术切除大鼠双侧卵巢,大鼠切除卵巢后14 d 胫骨近心端骨量丢失最明显,30 d 时股骨颈骨骨量丧失最多,60 d时腰椎椎骨骨量丢失达到高峰。切除雌性大鼠双侧卵巢造成雌激素水平急剧下降、骨量大量丢失而建立OP模型,具有建模因素单一、建模成功率高、可重复性好、可信度高和能够很好地体现雌激素水平下降这一重要病理生理现象等优点。

老年性骨质疏松症是由于年龄的老化引起的骨质疏松症。因此,可根据实验动物的寿命,采用自然衰老动物、快速老化模型小鼠(senescence -accelerated mouse,SAM)模拟老年性骨质疏松模型。快速老化模型小鼠SAMP6为自发老年性骨质疏松症模型,它是目前仅有的一种能证明增龄性骨脆性骨折的动物。SAMP6在4月龄时骨量达到峰值,之后骨量逐渐丢失,骨强度降低,硬度加大,抗变形能力及抗骨折能力差,与老年性骨质疏松症患者的病理变化相似。
药物致骨质疏松模型中糖皮质激素(Glucocorticoids,GCs)应用最广泛,使用糖皮质激素引起的骨质疏松症发病率仅次于绝经后骨质疏松和老年性骨质疏松,已被列为导致骨质疏松症的三大诱因之一。GCs是治疗炎症性和风湿性疾病广泛使用的药物,在临床上,患者使用GCs后,会发生一定几率的骨质疏松症。一般认为其病理机制主要在于GCs能通过氧化还原的途径影响破骨细胞和成骨细胞的分化和寿命,激活RANKL/RANK和WNT/-β Catenin途径,从而抑制成骨细胞的增殖和分化、促进骨吸收和局部细胞凋亡,增加骨脆性和骨折的概率,导致继发性骨质疏松甚至骨坏死。因此,GCs诱导法建立的OP模型对研究人类骨质疏松症意义重大,最常用的糖皮质激素有地塞米松、氢化可的松和泼尼松龙。
造模方法:在大鼠身上使用超生理剂量的皮质类固醇激素,如大鼠灌胃醋酸泼尼松龙(2.7 mg/kg/d)4周,即可使骨代谢处于负平衡状态,即骨吸收大于骨形成,骨量不断丢失,进而成功构建骨质疏松动物模型。

Doi:10.1172/JCI28551.
(2)维甲酸诱导的继发性骨质疏松模型:
维甲酸是治疗恶性肿瘤的药物,其副作用是引起骨量流失,诱发骨质疏松。研究发现维甲酸连续注射两周,动物即可出现严重的骨质疏松表现,骨量丢失,骨生物力学性能下降等。一般认为其作用机理主要是过激活体内的维甲酸受体相关的孤儿受体(ROR)进而影响骨代谢,使骨重建处于骨吸收大于骨形成的负平衡状态,从而诱发骨质疏松。
造模方法:大鼠维甲酸(80 mg/kg/d)连续灌胃14~21 d,观察4周,取大鼠股骨测得骨密度、骨组织形态计量均显著降低,血清钙、磷、碱性磷酸盐、抗酒石酸碱性磷酸盐均显著增高。
环磷酰胺是一种广谱抗肿瘤药,在骨代谢方面能够抑制骨形成,导致骨微结构退化,进而诱导骨质疏松症的发生发展。
造模方法:大鼠环磷酰胺(4.5 mg/kg/d)连续灌胃15 d即可诱导骨质疏松症。
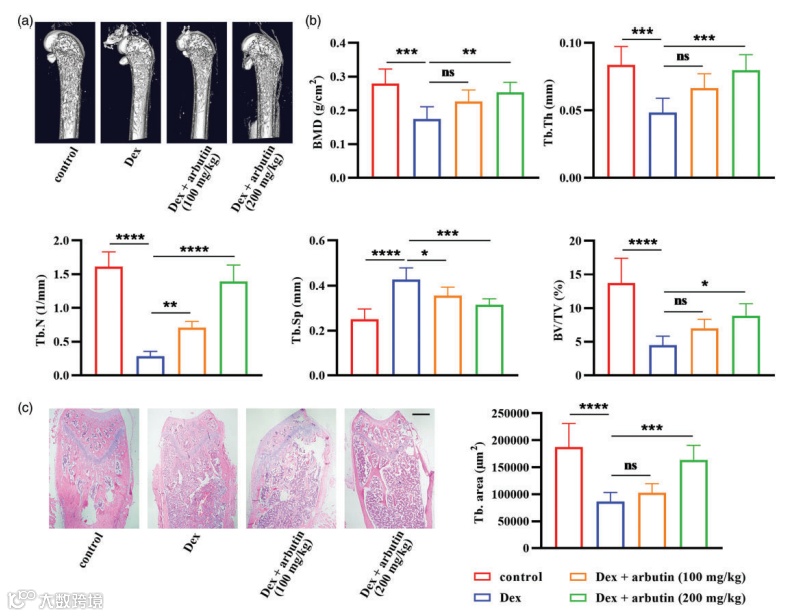
DOI: 10.1177/15353702211002136
4、营养缺陷诱导骨质疏松模型
营养是影响骨密度的众多因素之一,通过限制饮食中的钙、维生素D、蛋白质等的摄入可以成功建立营养缺乏型骨质疏松模型,该模型对研究因营养缺陷引起的OP有重要意义。但由于饲料配方复杂,且影响因素较多,普及推广困难。同时,因为单独应用营养法建模耗时长且成功率低,故常作为一种辅助方法。
造模方法:通过给大鼠饲喂低钙饮食造成骨吸收大于骨形成,从而得到低钙饮食诱导的OP模型或每天通过等渗泵皮下滴注去氨加压素(5 ng/h),同时每天给予70 mL/d(1.0 kcal/mL)的溶液和去离子水,连续3个月,使大鼠骨密度降低、骨小梁和皮质骨下降,得到低钠诱导的OP模型。
用去势法联合其他造模方法共同构建骨质疏松模型的方法亦是目前研究的热点,可以有效缩短造模时间。如去势联合糖皮质激素,去势联合低钙饮食,去势、低钙饮食、糖皮质激素三者联合等,且研究发现三联法较两联法对骨骼的影响更加明显。联合造模虽能加速造模,但干扰因素较多且复杂。
骨质疏松模型是否复制成功,需要用客观的指标来评价,骨质疏松的动物模型和造模方法众多,但评价指标是一致的,主要有骨密度测定、骨组织形态计量学、生化检测分析、骨生物力学测试、体质量、性腺形态等,其中最主要的是骨量与骨组织病理学变化这两项指标。
动物模型的骨密度(BMD)是诊断骨质疏松、预测骨质疏松骨折风险及评估药物治疗效果的重要指标,骨密度指骨骼单位面积中矿物质的含量,骨质疏松的发生与骨密度下降有关。骨密度检测方法有多种,有双能X线吸收检测法(DXA)、显微CT检测法、定量超声检测法(QUS)等,其中DXA测定是目前公认的诊断骨质疏松症的金标准。DXA是依据X射线衰减原理,组织越致密,所含的电子就越多,光子衰减也越大,采用X线管球作为射线源,产生两种不同能量的射线,在低能量下,骨骼的衰减比软组织的衰减程度要大,而在高能量下,骨骼衰减和软组织的衰减是相当的,可以区分两种组织,探测骨密度丢失情况。
骨组织形态计量学(bone histomorphometry)主要研究对象是二维骨组织切片显微图像,以生理学和骨组织学为依据,通过分析并处理显微图像,获得骨组织结构的计量参数。骨计量学能对骨结构与骨质量相关指标进行定性、定量的客观评价,能从动态和静态两个方面反映骨新陈代谢过程,能准确地分析骨结构和骨脆性,以及破骨细胞和成骨细胞的数目,骨小梁的厚度和数目等。
骨质疏松生化指标检测主要有骨代谢激素和骨转换相关指标的检测:
骨生物力学检测可反映骨质疏松骨组织结构和骨宏观力学效应如强度、硬度、韧性等情况,骨力学特性可间接反映骨矿盐分布、骨小梁空间结构等特性,可据此评价发生骨折的风险。常用的测量指标有骨干中段 3 点弯曲最大载荷、4点弯曲、抗扭转强度、轴向压缩实验、疲劳实验、椎体骨的抗压强度及破坏荷载等。
派思维新现有模型清单


专题回顾:
往期精彩:
翻滚吧肿瘤君丨世界淋巴瘤日
一场漫长的遗忘丨世界阿尔兹海默症日








