在肿瘤研究中,人源肿瘤组织异种移植(PDX)小鼠模型是现在被公认的优秀动物模型,然而PDX模型存在建模时间长,成本高,建模成功率低,难以满足高通量药物筛选等问题。而其他肿瘤研究模型如:细胞系来源的异体移植肿瘤模型(CDX),基因工程小鼠肿瘤模型,诱发性肿瘤小鼠模型,因为小鼠和人,细胞系与原发肿瘤存在很大差异,使得以这些模型所得到的基础研究成果进行临床的转化效率极低。
当前以患者来源的肿瘤类器官表现出同PDX模型一样,除了能维持患者肿瘤细胞的高度异质性,遵循人类原发性肿瘤中发现的耐药途径与肿瘤微环境对药物的影响,保持了患者的表观遗传特性等优势,还具备制备速度快,可进行药物高通量筛选,保持长期扩增,冷冻保存及基因改造等优势。已经成为肿瘤基础和临床研究中的重要工具,尤其在结合基因修饰技术后,对肿瘤精准研究意义重大。
2009 年,荷兰的 Hans Clevers 验室通过将小鼠单个 LGR5+的小肠干细胞种植在含有 ENR细胞因子组合 ( 表皮生长因子、Noggin、R-spondin)的三维基质胶培养体系中,发现干细胞通过增殖分化形成了包含具有增殖功能的隐窝和高分化绒毛的小肠结构,且该结构中仍有LGR5+的干细胞,高效模拟了小肠形态结构及功能[1]。类器官培养技术由此兴起并迅速拓展,人们成功建立了包括大脑、胃肠、肝肾、肺等机体正常组织的类器官模型。
类器官是在体外培育出与体内组织高度相似的空间结构,类器官不仅保留了与体内高度相似的组织学、遗传学特点,同时形成的组织有干细胞增殖与分化潜能。类器官可以进行稳定传代和冻存。
2014 年,BOJ 等[2]成功在体外培育出小鼠的胰腺肿瘤类器官,并在此基础上优化培养体系成功建立人胰腺导管癌类器官,通过对比原位肿瘤的基因测序发现包括 Kras 在内的基因突变都保持一致,这是肿瘤类器官的首次成功建立。随后人们又成功构建了结直肠癌、胃癌、前列腺癌、膀胱肿瘤、食道癌和子宫内膜癌等肿瘤类器官模型。与传统肿瘤研究模型相比,肿瘤类器官可以最大程度地模拟肿瘤在体内的结构和功能,既能直观展现肿瘤生长的过程,又能反映患者个体差异,是一种直观、可靠、高效和避免伦理争议的器官水平研究体系,与传统的2D模型相比更适合体外肿瘤生物学和癌症相关的研究。
Figture 1:提供PDOs模型定制和研发服务。
构建患者来源的肿瘤类器官(patient-derived organoids ,PDOs),肿瘤细胞的获取途径主要包括肿瘤组织来源、液体活检来源和肿瘤干细胞来源。肿瘤组织组织主要是通过手术、组织活检等途径获得。通过物理剪碎、胶原酶消化等处理分离纯化获得肿瘤细胞的小团块,将其接种在基底膜提取物上,含有各类生长因子的改良型培养基传代培养。类器官培养基中的主要成分为(ADMEM)/F12,盘尼西林/链霉素,primocin,GlutaMAX, HEPES,B27,N2,EGF,FGF10,FGF7,肝细胞生长因子(HGF),Wnt3A,Noggin,R-spondin-1,胃泌素,prostaglandin E2,烟酰胺,神经调节蛋白1,N -乙酰半胱氨酸,Y27632(Rho激酶抑制剂),A-83-01(转化生长因子- β抑制剂),以及SB202190(p38抑制剂)[3]。
肿瘤微环境的体外重现是肿瘤类器官形成高度模拟体内组织的关键。主要的培养条件要素包括细胞因子和生物学材料,其中细胞因子可以促进肿瘤细胞的增殖、分化,而生物学材料模拟细胞外基质、提供生物力学等支撑。
类器官培养基是培养环境中最重要的组成部分,它为细胞生长提供必要的营养、生长因子和激素,还可以调节培养环境的 pH 值和渗透压。而肿瘤类器官的培养除了基本培养基外,还需要加入包括相关通路激活剂或抑制剂和激素等不同类型的细胞因子来保障肿瘤细胞的生长。
表皮生长因子和成纤维细胞生长因子等属于所需的基本细胞因子促进肿瘤细胞的增殖;在肝癌类器官培养中需要在正常肝类器官培养方案中去除R-Spondin1、Noggin和Wnt3a,并加入地塞米松和Rho激酶抑制剂;肿瘤干细胞的活性依赖Wnt通路和Notch通路的持续激活,而R-Spondin1作为Wnt 信号通路的激动剂,不仅可以促进肿瘤细胞的增殖还可以控制分泌细胞的分化,在乳腺癌、结直肠癌等肿瘤类器官培养中是必要的细胞因子之一;为了抑制细胞发生上皮间质转化的分化,在前列腺癌等类器官中需要加入转化生长因子β信号通路的抑制剂A83-01。除了这些基本因子外,不同肿瘤还需要一些关键因子:乳腺癌类器官的培养需要补充神经调节蛋白1,它是人表皮生长因子受体(Her)3和4的配体;肝癌类器官的培养中,需要加入肝细胞生长因子(HGF)特异性地促进肝癌细胞的增殖;恶性卵巢肿瘤主要驱动因素是P53的突变,因此在恶性卵巢癌类器官培养基中可添加Nutlin-3a。此外还需要一些小分子物质,前列腺癌类器官需要加入雄激素,肝癌和胰腺肿瘤类器官中需要添加胃泌素,一些无机物质也作为营养辅助成分添加,如维生素C、烟酰胺等。这些因子的加入不仅利于培养出肿瘤类器官,且培养体系更加接近体内的肿瘤微环境,从而保证了体外培养的肿瘤类器官与原发灶肿瘤的基本特质的一致性[4]。
PDOs的培养中常用到的生物学材料是一类以基底膜提取物、基质胶为主的天然材料。基质胶是从EHS小鼠肉瘤中提取的可溶和无菌的基底膜蛋白,主要成分包括生长因子、层粘连蛋白、Ⅳ型胶原、巢蛋白及细胞因子等,其组成成分及其比例与人体基底膜相同。有研究表明基质胶可以促进乳腺上皮细胞生长并形成管样结构、 还可以促进唾液腺细胞形成腺体。正是因为基质胶可以模拟体内肿瘤生长的局部环境促进肿瘤类器官增殖和腺体分化的优点,所以被广泛用于多种肿瘤类器官培养。
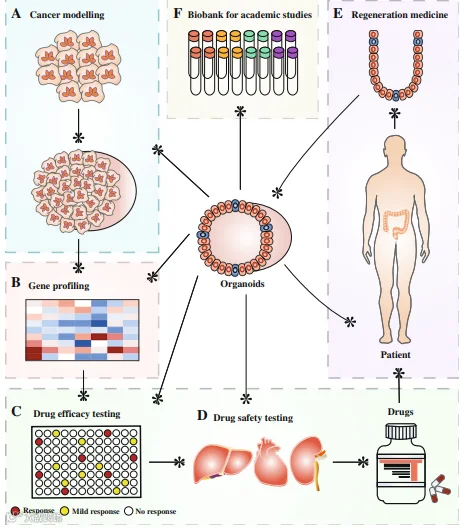
Figture 2:PDO 类器官模型的应用示意图
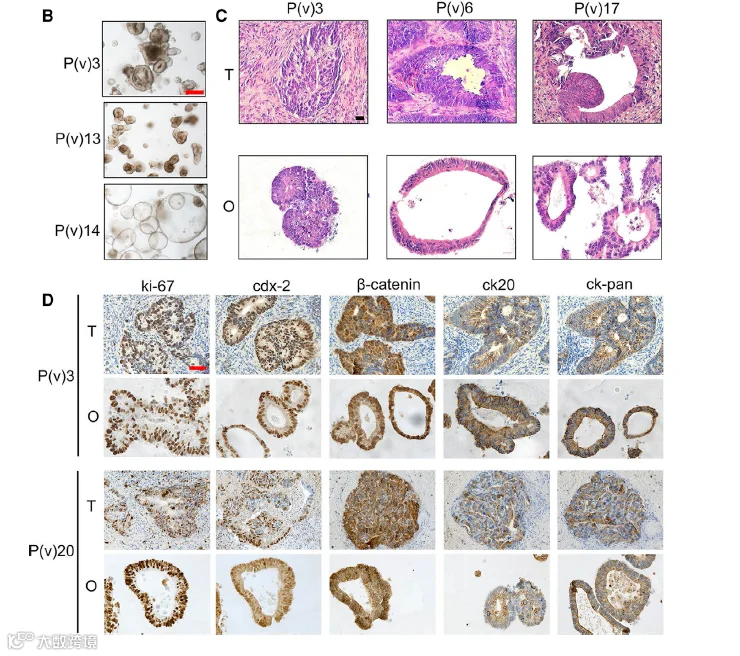
PDOs与肿瘤组织固定稍有区别。肿瘤组织固定在4%新鲜制备的多聚甲醛中4℃,16-18小时,脱水后埋于石蜡块中。类器官去除培养基后加入预热4%新鲜制备的多聚甲醛中在37℃固定30分钟,然后将基质胶完整转移后再进行后续操作。以肠癌PDOs为例,HE染色用苏木精和伊红染色,选择ki-67、CDX2、ß-catenin、CK20、CK-pan进行免疫组化染色[6]。
Figture3:肿瘤-PDOs的相关模型特定化表型坚定。已建了80例结肠癌患者活检来源的肠癌类器官生物库,对患者原发组织和对应PDOs分别从组织病理学进行形态结构观察,肿瘤标志物的染色鉴定,基因表达变化及基因突变分析。(B)是肠癌类器官三种表型的明场图像,比例尺:200um。(C)是患者原发组织和对应的肿瘤类器官HE染色,比例尺:200um(T,原发肿瘤;O,对应PDO)(D)免疫组织化学染色结果。
虽然肠癌类器官在形态和生长速率个体间表现出差异,但是从类器官和对应肿瘤的HE染色来看都呈现出患者的特异性异质形态,不管是薄壁囊状,实心或是质密的结构。免疫组化染色分析也表明肿瘤和对应PDOs的染色结果相似。这些数据表明,PDOs再现了原始肿瘤组织的组织学特征和肿瘤标志物表达。
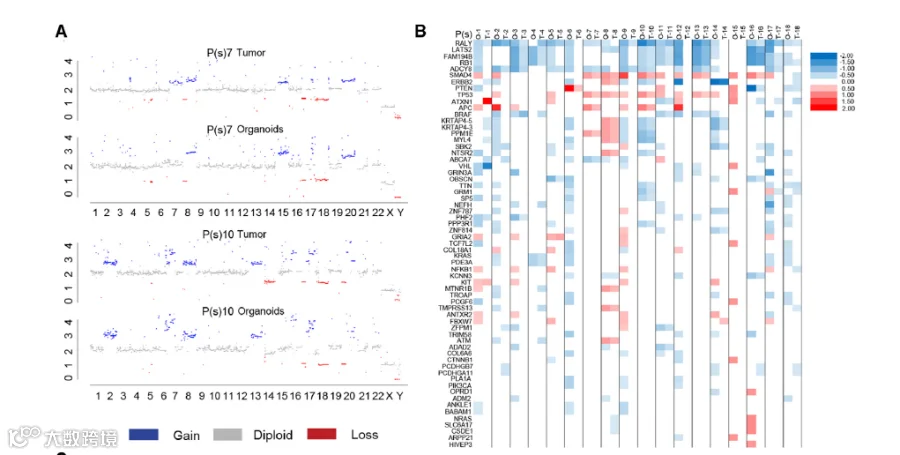
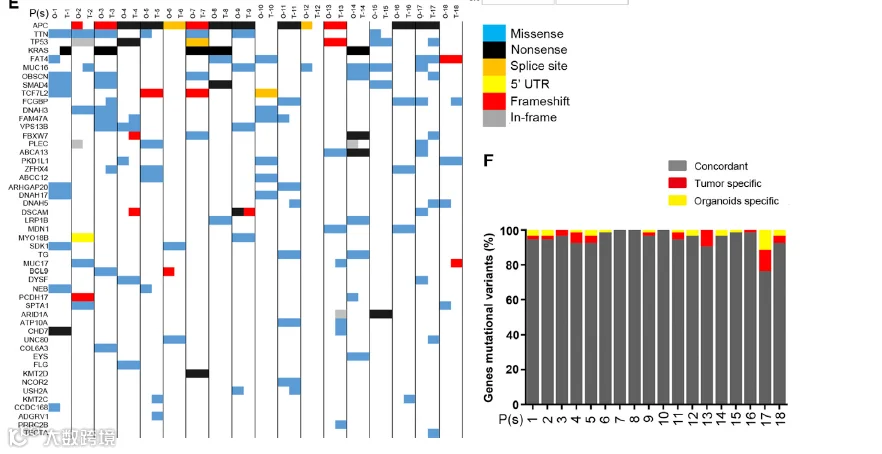
Figture4:(A)PDOs和成对原发肿瘤的全基因组基因拷贝数变异(CNVs)(蓝色,增加;红色,缺失;灰色,二倍体)。(B)肠癌驱动基因CNVs热图。基因拷贝数转换为每个基因的log2比率(蓝色,增加;红色,缺失)。(E)肠癌最常突变基因的基因突变变异(单核苷酸变异[SNVs])热图。(F)显示肠癌肿瘤类器官与相应原发肿瘤之间SNV的一致性(百分比)的直方图。
该图系统比较了类器官与对应肿瘤全基因组的CNV,发现DNA拷贝数的缺失和增加在整个基因组中都保留了。在18例病例中,有12例PDOs培养重现了在患者中发现的肠癌驱动基因中CNVs的特征,尽管在原发肿瘤样本中,读取数量通常较低。PDOs保留了在肠癌中最常突变的成对肿瘤基因超过94.4%。WNT信号通路基因的突变率为88.9%(18例中有16例);其中包括APC, FBXW7,TCF7L2、ARID1A、LRP5和SOX9突变。APC发生突变18例PDOs中有13例(72.2%),而18例类器官中有5例野生型APC。预期的Wnt通路激活突变在PDO培养中观察到。
在类器官培养过程中需要很多因子的支持,但如果细胞存在特定的基因突变,就会失去对对特定细胞因子的依赖性,或者拥有对特定的信号通路抑制剂产生抗性,因此通过在类器官培养基中,通过去掉特定的细胞因子,或者联合添加信号通路抑制剂,便可以将带有特定突变的肿瘤类器官筛选鉴定出来(条件培养)。携带特定基因突变的类器官,尤其是肿瘤驱动基因突变的类器官,在研究肿瘤发生,发展,转移上是非常有用的工具。
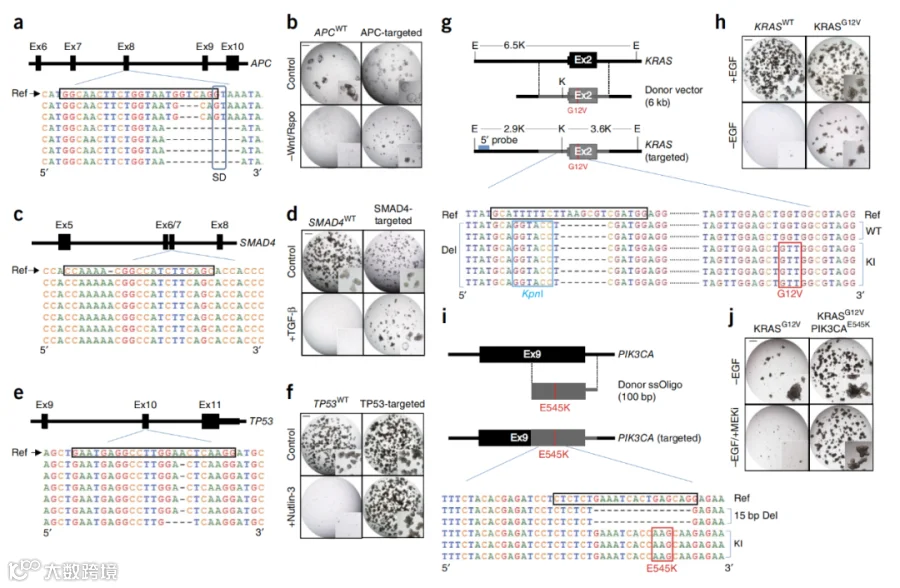
以2015年Nat Med期刊的文献:“Modeling colorectal cancer using CRISPR-Cas9-mediated engineering of human intestinal organoids”为例:作者通过CRISPR-Cas9基因编辑技术,将影响肿瘤发生发展的关键性驱动基因APC,TP53,KRAS,SMAD4进行了突变或者敲除,再通过条件培养筛选出来了同时携带多种驱动基因突变的,由正常结直肠来源的类器官。
Figture 5:先确定单驱动基因突变的类器官所需要的培养条件,以上图为例APC基因突变的类器官获得了Wnt信号通路激活剂依赖性的丢失,而TP53突变则让类器官获得了对Nutlin-3抑制剂的抗性。

Figture 6:联合各突变驱动基因的条件培养,成功获得了携带5种驱动基因突变的,正常结直肠来源的类器官。

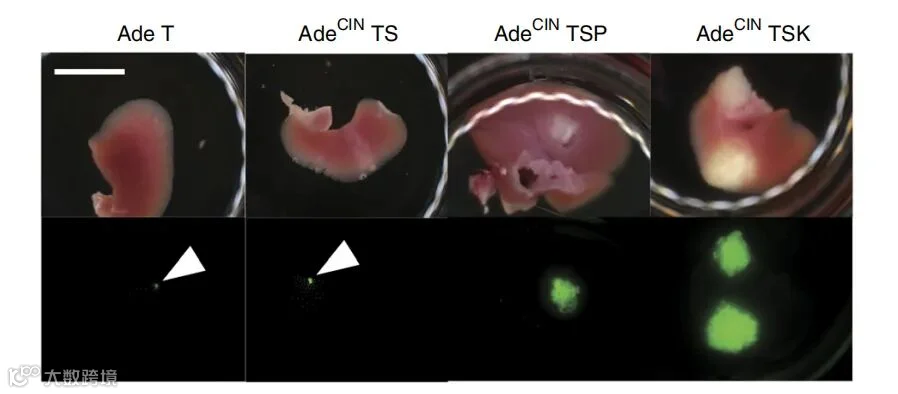
Figture 7:将获得的携带5种驱动基因突变,正常结直肠来源的类器官注射到NSG小鼠体内,通过左图注射部位的荧光成像我们可以看到:相比于阳性对照组(CRC组),携带5种驱动基因突变,正常结直肠来源的类器官同样可以在注射部位成瘤,而右图小鼠肝的荧光成像,则表明相比于阳性对照组(CRC组),携带5种驱动基因突变,正常结直肠来源的类器官还无法发生肝转移。当将模型从结肠类器官,换成携带染色体不稳定的腺癌,重复上述实验,肿瘤则获得了很好的转移能力。表明肿瘤转移与染色体的不稳定状态有密切关联。
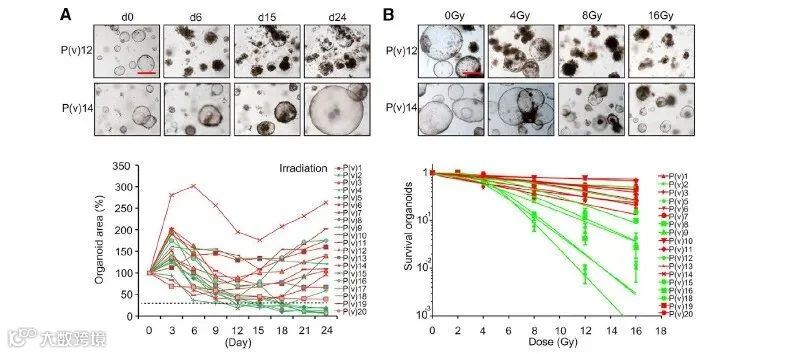
个性化医疗又称为精准医疗,文章对选取的80例肠癌PDOs开展同步治疗对照研究,检测类器官的大小变化,持续追踪患者临床新辅助治疗效果进行对比。
Figture 8:(A)8 Gy照射后类器官大小的变化(上图为两个选定病例中8 Gy照射后具有代表性的类器官明场图像;20例PDOs 经8 Gy辐照后面积变化曲线)。(B)类器官对照射的剂量反应(上图为两个选定病例照射后第15天具有代表性的类器官明场图像;下面是20例照射后第15天剂量-存活率曲线)。红色曲线,临床反应差的患者(trg2或3);绿色曲线,临床反应良好的患者(TRG 0或1或cCR)。
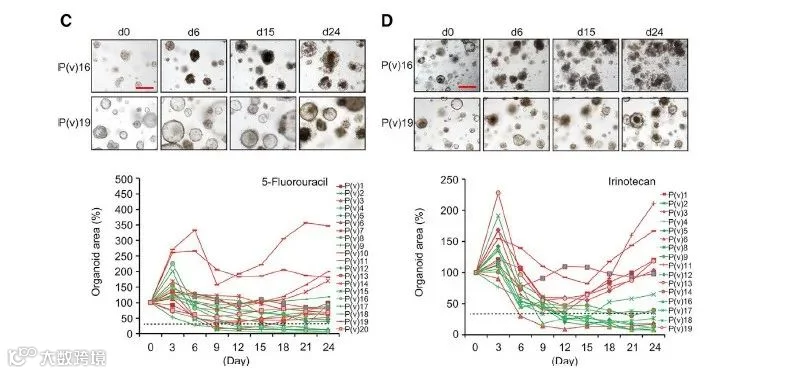
Figture 8:(C)10 uM 5-Fu处理后类器官大小的变化(上图为两例5-Fu处理后具有代表性的类器官明场图像;下面是 20例5-Fu治疗后类器官大小变化曲线)。(D)10 uM CPT-11处理后类器官大小的变化(上图为两个选定病例CPT-11处理后具有代表性的类器官明场图像;下为19例CPT-11治疗后类器官大小变化曲线)。
虚线表示类器官大小变化截点(36.42%)。比例尺:200um
Figture 9:(A)在六个选定病例中,每个患者对辅射、5-Fu和CPT-11的类器官反应和相关患者的临床结果(上面是经8 Gy照射或药物治疗后第24天的类器官明场图像;下为8 Gy照射及药物处理后类器官大小变化曲线)。虚线表示类器官大小变化的截止点(36.42%)。比例尺:200 um。

Figture 9:(B)患者临床结果的评估(上面是新辅助放化疗前后的MRI图像;下为术后残留肿瘤的H&E图像)。白色箭头表示直肠癌肿瘤,红色箭头表示腺癌腺体,绿色箭头表示正常大肠上皮腺体。
在80例PDOs中有68个PDOs的敏感性数据与患者的临床结果匹配,12个PDOs不匹配。整体匹配率为85.0%(68/80)。由此可见,合并后的PDO数据与患者的临床表现高度相关,AUC为88.20%(95%CI,76.46%-98.67%),84.43%的准确率(95%CI,72.40%~93.75%),78.01%的灵敏度(95%CI,55.56%~95.00%),91.97%的特异性(95%CI,77.78%-100.00%),Cohen 's kappa=0.69(95%CI,0.46- -0.88)。
因此,PDO数据可能可以用于调整新辅助治疗方法,使用适当的药物进行化疗或者放疗,以改善临床效果降低LARC对患者的毒性。
类器官技术拥有巨大的潜力去准确模拟人类肿瘤,利用这些令人惊叹的3D培养可以显著促进药物筛选和个性化医学研究去更好地预测药物反应和指导优化个体化治疗方案。未来继续努力,类器官技术会更接近临床实践。
Figture 10:派思维新人结肠癌类器官培养成果展示
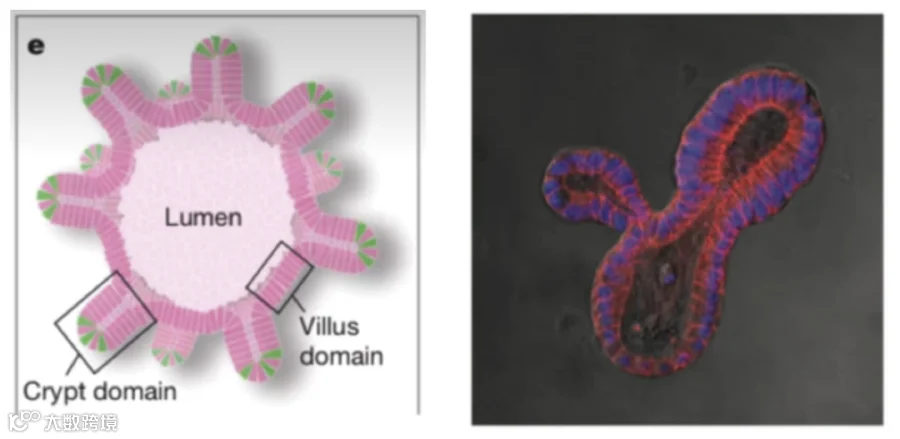
派思维新在结肠癌类器官培养上现可实现稳定扩增,已经达到结肠类器官的典型结构:以单层细胞为主的组织结构,具备扩增分化的能力的干细胞存在于“凸起”的顶端,中间为lumen,如Figture 11所指示。
结肠癌类器官在指导结肠药物研发和临床治疗上运用有丰富的运用:Vlachogiannis等[8]构建了转移性耐药结直肠癌患者类器官模型(PDO),在预测患者对靶向药物或化疗效果方面,达到了100%敏感性、93%特异性、88%阳性预测值和100%的阴性预测值(P<0.000 1),发现BRAF抑制剂威罗菲尼(vemurafenib)可抑制BRAFV600E突变的PDO生长,但未能诱导细胞凋亡,这与单药BRAF抑制剂在转移性结直肠癌中缺乏疗效一致,而包含KRASG12D和BRAFV600E突变的2例PDO对西妥昔单抗无应答,也与这两种药的临床耐药一致。根据这些结果,避免了无效治疗。另外Dijkstra等[7]构建了13例dMMR患者结直肠癌类器官与自身外周血淋巴细胞共培养,其中4例(31%)在IL-2、IFN-γ刺激下诱导产生肿瘤反应性T细胞杀伤肿瘤类器官,同时对自身正常类器官没有杀伤作用。此项研究提供了一种体外检测结直肠癌患者免疫治疗敏感性的方法,也可用于过继性免疫细胞治疗。
在动物模型方面,Vlachogiannis等[8]建立人结直肠癌类器官原位异种移植模型,来自瑞戈非尼(regorafenib)敏感患者的肿瘤类器官PDX中,肿瘤在其作用下微血管明显减少(P=0.03,P<0.05),而来自瑞戈非尼耐药患者的PDO移植模型无明显变化。国内学者利用结直肠癌类器官构建小鼠PDX模型探究10-羟基喜树碱、丝裂霉素、阿霉素及紫杉醇的药物敏感性,用于筛选药物[9]


更多信息
请登录派思维新官方网站
www.novopathway.com
[1]SATO T, VRIES RG, SNIPPERT HJ, et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 2009;459:262-265.
[2]BOJ SF, HWANG CI, BAKER LA, et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. 2015;160:324-338.
[3]冯紫伊,梁珊珊,于炜婷,王若雨.患者来源肿瘤类器官的培养与研究及应用[J].中国组织工程研究,2021,25(25):4082-4088.
[4]Xu, H., Lyu, X., Yi, M., Zhao, W., Song, Y., & Wu, K. (2018). Organoid technology and applications in cancer research. Journal of Hematology & Oncology, 11(1). doi:10.1186/s13045-018-0662-9 .
[5]Matano M, Date S, Shimokawa M, Takano A, Fujii M, Ohta Y, Watanabe T, Kanai T, Sato T. Modeling colorectal cancer using CRISPR-Cas9-mediated engineering of human intestinal organoids. Nat Med. 2015 Mar;21(3):256-62.
[6] Patient-Derived Organoids Predict Chemoradiation Responses of Locally Advanced Rectal Cancer .Yao, Ye et al.Cell Stem Cell, Volume 26, Issue 1, 17 - 26.e6.
[7] DijkstraKK,CattaneoCM,WeeberF, et al.Generation of tumor-reactive T cells by co-culture of peripheral blood lymphocytes and tumor organoids[J]. Cell, 2018, 174(6): 1586-1598.e12. DOI:10.1016/j.cell.2018.07.009.
[8] VlachogiannisG,HedayatS,VatsiouA, et al.Patient-derived organoids model treatment response of metastatic gastrointestinal cancers[J].Science, 2018, 359(6378): 920-926.DOI: 10.1126/science.aao2774.
[9] XieBY,WuAW. Organoid culture of isolated cells from patient-derived tissues with colorectal cancer[J].Chin Med J, 2016, 129 (20):2469-2475. DOI: 10.4103/0366-6999.191782.
[10] 路小欢, 徐鲁明, 王星月,等. 结直肠癌类器官的构建与应用进展[J]. 中华医学杂志, 2019, 99(36):3.