

基于UPLC-Q-TOF/MS的黑灵芝多糖对大鼠急性肠道炎症作用机制研究
——南昌大学李文娟教授课题组


研究背景


近年来,随着现代社会生活方式、饮食结构及运动量减少等的改变,肠道疾病的发病率逐年增加,且具有年轻化的趋势,严重影响人们的生活质量。有研究指出炎症是许多肠道疾病的发病诱因和病理基础,如炎性肠病、肠易激综合征、结直肠癌等。肠道在消化吸收营养物质的,同时也极易受到饮食和微生物因素的影响进而引发肠道炎症。当肠道发生炎症时,肠道的蠕动往往会减缓,有害细菌繁殖,过量脂多糖( lipopolysaccharide, LPS)累积,肠道机械屏障受损、通透性增加,有害物质被吸收、移位至循环和淋巴系统,激活炎症信号通路释放IL-1β、IL-6及TNF-ɑ等多种炎症介质,形成级联放大作用,炎症因子过度激活,进而导致其他器官功能发生障碍。因此,维护机体内炎症因子的平衡状态,阻断级联放大的失控性炎症反应是防治肠道疾病的重要策略。
黑灵芝(Ganoderma atrum)作为一种著名的药食同源的天然真菌,含有多种活性物质如多糖、三萜类化合物、氨基酸多肽类等。近年来,Chen Yi等对江西赣州的黑灵芝开展了大量的研究工作,分离提取了一种水溶性黑灵芝多糖(Ganoderma atrum polysaccharides, PSG)。前期研究发现,PSG具有降血糖、抗氧化、抗肿瘤、抗衰老及调节免疫等生物活性,其中免疫调节是PSG发挥多种生物学功能的基础。帅小雪等研究表明PSG可显著升高LPS所致小鼠腹腔巨噬细胞炎症模型中IL-10的水平,和抑制细胞中IL-1β、TNF-α水平,降低机体的炎症水平。Zhang shen shen等研究发现PSG可与TLR4和甘露糖受体结合,激活NF-κB信号通路来减少LPS所诱导的炎症水平。同时,赵明明等报道了PSG能够有效地改善免疫抑制小鼠肠道绒毛断裂、缩短及隐窝深度的降低等损伤,增强机体的免疫功能,来发挥肠道保护作用。基于以上研究,PSG已初步被证实具有抗炎作用且对肠道具有一定的保护作用。但目前国内关于PSG对于LPS所致急性肠道炎症的保护作用研究鲜有报道。
代谢组学是通过色谱、质谱及其联用等技术对特定条件下生物体内源性代谢产物的种类、数量及变化规律进行定量或定性分析,为探究生物化学与细胞表型之间的机制提供了良好的平台。近年来,代谢组学在食品、营养和医药等领域得到广泛的运用,为功能性食品和药物的开发和利用提供科学的理论基础。因此,李文娟团队运用UPLC-Q-TOF/MS技术分析急性肠道炎症大鼠盲肠内容物中小分子代谢产物,寻找PSG干预急性肠道炎症大鼠盲肠内容物的生物标志物及相关代谢通路,为PSG后期的资源开发和利用提供科学依据。


1 PSG对LPS诱导大鼠急性肠道炎症中肠道组织形态学的影响

肠道对于机体而言不仅是消化吸收营养物质的器官,也是表面积最大的免疫器官。因此,肠道的完整性和功能性对机体的健康至关重要。唐煌尧等人指出当肠道的机械屏障受到破坏时,细菌或者毒素则会侵入肠道细胞并诱发多种炎症因子的合成与分泌,进而造成肠道炎症的发生。在本实验中,对空肠组织进行HE染色。如图1所示,Con组大鼠的空肠黏膜上皮正常,绒毛无明显断裂充血等症状。与Con组大鼠相比,LPS组大鼠空肠黏膜上皮糜烂缺失,绒毛明显断裂充血等,且隐窝深度也有明显降低。与LPS组相比,PSG低、中剂量组空肠绒毛明显增长,黏膜得到一定的恢复。而PSG高剂量组和DEX组大鼠空肠组织损伤明显改善,黏膜、绒毛和隐窝均恢复至正常水平,表明PSG在一定浓度下对LPS诱导肠道组织损伤有一定的保护作用。
2 PSG对LPS诱导大鼠急性肠道炎症中IL-1β、IL-10因子含量的影响
肠道组织病理切片的结果表明,LPS可诱导肠道的损伤,诱发大量的炎症细胞聚集和浸润。在急性肠道炎症病理状态下,炎症介质IL-1β由激活的抗原呈递细胞(如巨噬细胞)分泌,并通过自分泌或旁分泌的方式诱导TNF-α、IL-6等因子产生而进一步增加组织损伤,因此IL-1β被认为在急性肠道炎症的炎症反应中扮演了重要的始动作用。本实验发现在腹腔注射LPS后大鼠小肠组织匀浆中IL-1β含量明显增加(p < 0.05,表2)。而PSG剂量组和DEX组小肠匀浆中IL-1β含量均有不同程度的下降,其中PSG高剂量组IL-1β含量有显著性差异(p < 0.05)与LPS组相比较,说明PSG可以减少体内LPS诱导产生的IL-1β。
LPS进入机体后,抗炎因子的产生往往伴随着促炎因子的产生。众所周知,IL-10作为Th2细胞源性抗炎因子,在平衡机体炎症反应中扮演着关键性的作用,可以有效减缓炎症反应所诱导的损伤。IL-10可通过抑制NF-κB的激活来减少免疫细胞分泌促炎因子,平衡体内炎症反应[17]。研究表明,急慢性炎症均与IL-10水平的上升相关,这可能与机体发生的代偿性抗炎反应有关,会进一步地造成多器官障碍。在黄小流等[18]人研究中发现LPS处理大鼠空肠组织中的IL-10含量显著增加。因此,平衡机体内促炎因子和抗炎因子的状态及阻断级联放大的失控性炎症反应是防治急性肠道炎症的重要策略。与Con组相比,LPS组大鼠小肠组织匀浆中的IL-10含量显著增加(p<0.05,见表2)。与LPS组相比,PSG低、中剂量组小肠组织匀浆中IL-10含量有所降低而PSG高剂量组IL-10含量显著增加(P<0.05),这与金鹏峰[19]等人研究结果类似。有研究指出,IL-10浓度的增加与急性肠道炎症减缓有关[20]。DEX组小肠匀浆中IL-10含量也增加,但无统计学意义。综上所述,一定浓度的PSG对LPS诱导ALI大鼠小肠组织中 IL-10释放有明显的促进作用。

3 PSG对LPS诱导大鼠急性肠道炎症中盲肠内容物代谢的影响
3.1 多元统计数据分析
将盲肠内容物预处理好的代谢组学数据导入SIMCA-P软件中进行PCA分析,结果发现盲肠内容物样本在负离子模式下Con组、LPS组、PSG组和DEX组基本完全分离,在正负离子模式下四组样品没有完全分开,但是通过二维图可知,Con组和LPS组明显分离且相隔较远,表明这两组之间的差异是最大的(图2A)。为了进一步分析Con组、PSG组、DEX组与LPS组盲肠内容物样品之间的代谢谱差异,本实验也建立OPLS-DA分析模型。参数R2和Q2分别表示模型的可解释性和预测能力,越接近1越好。在本实验中,正离子模式下R2和Q2分别为0.934和0.711,负离子模式下R2和Q2分别为0.950和0.776,说明OPLS-DA模型是可靠的。此外,200次响应排序检验结果发现OPLS-DA模型中所有排序检验后的R2和Q2值均低于原始值,且Q2值小于零,说明此OPLS-DA模型不存在过度拟合,模型有效。如图2B所示,四组样本在OPLS-DA得分图中均显著分离,Con组与LPS组相隔较远,PSG组远离LPS组且接近Con组,DEX组也远离LPS组,这与Li等研究中血常规、炎性细胞因子的数据结果相一致,表明PSG可调节LPS所致大鼠急性肠道炎症盲肠内容物中代谢物的组分与含量。

3.2 盲肠内容物中代谢差异物鉴定
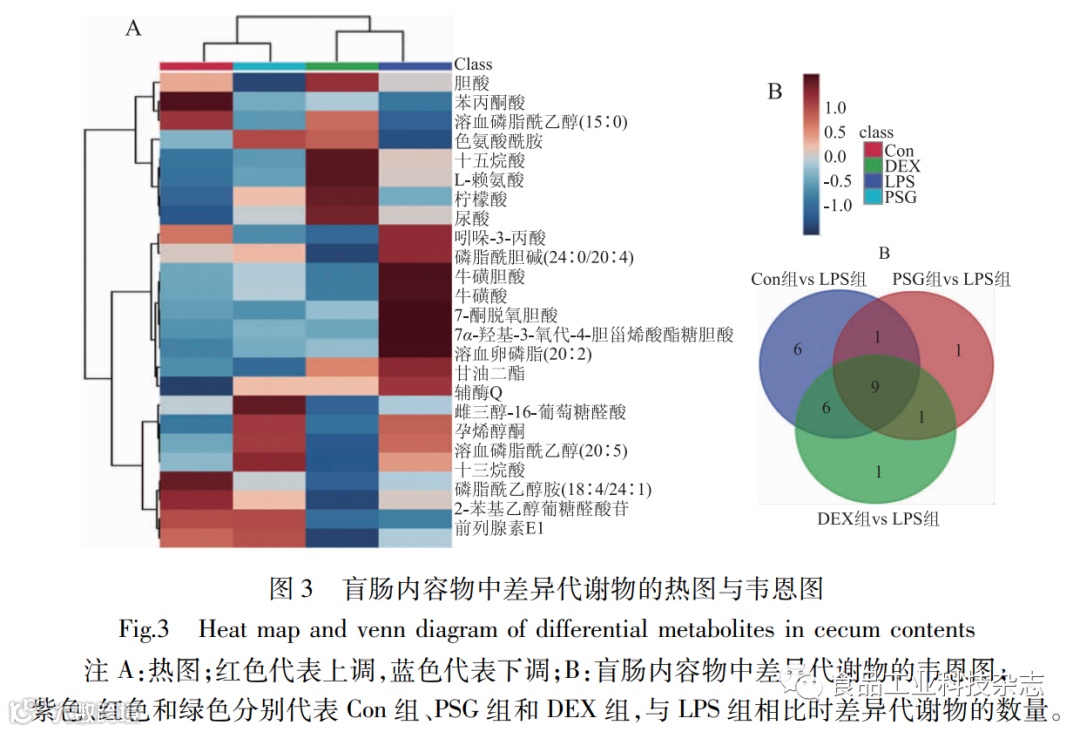
从OPLS-DA模型中得到VIP >1的差异质荷比,并通过相对峰面积进行定量分析。同时,采用独立t检验对差异质荷比的含量进行显著性分析,设定阈值为p<0.05,筛选出差异质荷比。最后,将差异质荷比的二级碎片离子与METLIN、KEGG、HMDB和Pub Chem数据库中二级的碎片离子相匹配,鉴定出差异代谢物,最终筛选鉴定出25种差异代谢物,见表3。与Con组相比,LPS组大鼠盲肠内容物中找到了22种差异代谢物,与LPS组相比,PSG组和DEX组中分别找到了12和17种差异代谢物。通过Venn图可知,LPS 组与PSG 组中差异代谢物共有10个差异代谢物,LPS 组与DEX组中共有10种差异代谢物。同时热图(图3)也揭示了,与Con组相比,LPS组盲肠内容物中有17种代谢差异物显著增加,有5种差异代谢物显著减少。而PSG组盲肠内容物中有10种代谢差异物明显被改善。

3.3 代谢通路分析

表4 盲肠内容物中差异物代谢通路的分析结果
Table 4 Result from pathway analysis ofdifferential metabolites in cecum contents
代谢通路 |
匹配数量 /总数量 |
原始 p值 |
-log (p) |
影响值 |
匹配的代谢物 |
GPI锚定生物合成 |
1/14 |
0.155 |
1.8626 |
0.125 |
PE (18:4/24:1) |
甘油磷脂代谢 |
3/36 |
0.008 |
4.8335 |
0.2115 |
Lyso PC(20:2), PE(18:4/24:1), PC(24:0/20:4) |
亚油酸代谢 |
1/5 |
0.058 |
2.842 |
0.25 |
PC(24:0/20:4) |
α-亚麻酸代谢 |
1/13 |
0.145 |
1.9312 |
0.125 |
|
花生四烯酸代谢 |
1/36 |
0.354 |
1.0381 |
0.0278 |
|
苯丙氨酸,酪氨酸和色氨酸的生物合成 |
1/4 |
0.047 |
3.0595 |
0.25 |
Phenylpyruvic acid |
苯丙氨酸代谢 |
1/12 |
0.135 |
2.0056 |
0.3 |
|
初级胆汁酸的生物合成 |
4/46 |
0.002 |
6.3812 |
0.0213 |
Cholic acid, 7α-Hydroxy-3-oxo-4-cholestenoate, Glycocholic Acid, Taurocholic acid |
牛磺酸和亚牛磺酸的代谢 |
1/8 |
0.092 |
2.3888 |
0 |
Taurocholic acid |
生物素代谢 |
1/10 |
0.113 |
2.1768 |
0 |
L-Lysine |
赖氨酸降解 |
1/25 |
0.261 |
1.3433 |
0.05 |
|
氨酰基-tRNA的生物合成 |
1/48 |
0.443 |
0.8141 |
0.0345 |
|
类固醇激素的合成 |
2/77 |
0.233 |
1.4563 |
0.0581 |
Pregnenolone,16-Glucuronide-estriol |
嘌呤代谢 |
1/66 |
0.555 |
0.5888 |
0.0114 |
Uric acid |
3.3.1 盲肠内容物中苯丙氨酸代谢通路与急性肠道炎症关系
3.3.2 盲肠内容物中甘油磷脂代谢通路与急性肠道炎症关系
4 结论
通讯作者简介

李文娟 副教授
南昌大学食品学院
李文娟,2004年毕业于南昌大学大学医学院药学专业,2007年获得南昌大学医学院药理学专业硕士学位,同年考取南昌大学食品学院食品科学与工程攻读博士学位,并于2011年博士毕业留校任教;攻读博士期间曾多次获得研究生特等奖学金“中兴发展”奖学金、“益海嘉里”奖学金、“大盈”奖学金、“王氏”奖学金与三好学生等荣誉。博士期间研究成果获2009年度第二届中国食品科学技术学会科技创新奖----优秀论文奖----“二等奖,2011年获南昌大学优秀博士毕业生。博士论文获2012年度获江西省优秀博士学位论文。本人于2011年7月就职于南昌大学食品学院,从事教学与科研工作,研究方向为食品安全与分子营养学、食源性活性组分结构鉴定与活性功能作用机理等;2013年12月晋升副教授。近年来一直围绕多糖类复杂碳水化合物和多酚开展研究,基于创新性成果,第一作者或通讯作者发表论文近50篇(其中20篇被SCI收录),研究成果获2015年度江西省自然科学奖一等奖。主讲本科生课程多门,本科课程《食品安全风险评估》教学获江西省高等学校教学改革项目1项(No:JXJG),参编著作1部;2017年作为第一指导老师带领本科生参加第十五届“挑战杯”全国大学生课外学术科技作品竞赛《甘露糖受体介导黑灵芝多糖调控巨噬细胞极化模式研究》获江西赛区“特等奖”。此外,积极参加江西省科技特派团婺源茶叶团(No:0210208651),与企业合作,积极推动产学研相关研究。

代表性成果:
(1)Effect of Ganoderma atrum polysaccharide against pancreatic damage instreptozotocin-induced diabetic mice[J].Function food,2019,DOI:10.1039/C9FO01990A.(SCI一区,IF:3.289) (2)Ganoderma atrum polysaccharide improves doxorubicin-induced cardiotoxicity in mice by regulation of apoptotic pathway in mitochondria[J].Carbohydratepolymers,2018,202:581-590.(SCI一区,IF:6.044) (3)Mannosereceptormediatestheimmuneresponseto Ganoderma atrum polysaccharides inmacrophages[J].Journal of Agricultural and Food Chemistry.2017,65,348−357.(SCI一区,IF:2.857)


版权声明
本公众号推送文章仅为学术交流使用,‘原创’为原创编译之标记,不表示本平台对文本主张版权。作者团队或单位如需使用编译文本,可联系编辑开放白名单。凡是注明“转载”的稿件,均已注明直接来源,如需使用,请联系版权人。如有侵权,请联系我们,我们会尽快删除。





