



图片来源于图司机
南昌大学食品学院陈军副院长等以乳清分离蛋白和甜菜首为研究对象,明确乳清分离蛋白对甜菜香热稳定的影响以及甜菜昔对蛋白内源荧光表面疏水性、二级结构的影响,并采用多光谱学结合分子模拟的方法探究乳清分离蛋白与甜菜昔的相互作用机制,为色素稳定的研究及功能性蛋白色素复合物的应用开发提供理论基础。
通过使用紫外可见光谱法测量浊度来验证WPI-Betanin 复合物的形成。当由光波的散射而形成胶体粒子时,溶液的浊度会增加。浊度增加的幅度取决于颗粒的数量、大小和折射率对比度等。因此, 浊度的测量可以快速指示胶态颗粒的形成。图 1 显示了乳清分离蛋白:甜菜苷质量比对乳清分离蛋 白-甜菜苷溶液的外观和浊度的影响。当乳清分离蛋白与甜菜苷的比例从 16:0 增加至 16:8 时,浊度从0.290 显著提高至 0.306 cm−1(P<0.05),从外观上看,溶液变得越来越混浊,但在室温下储存一天之后,也并没有沉淀迹象。这些结果表明乳清分离蛋白与甜 菜苷形成了相对较小的胶体复合物,具有较强的抗重力沉淀能力。

蛋白质分子微环境中芳香族氨基酸残基的变化可能会导致蛋白质的紫外吸收发生变化,因此可以应用蛋白质的紫外光谱来分析蛋白质的结构变化。紫外光谱可反映乳清分离蛋白与甜菜苷间的相互作用,表现为紫外光谱峰值的蓝移或红移、信号的增强或减弱。图2中显示乳清分离蛋白在 280 nm 处有最大吸收峰,此处的吸收可能是由于色氨酸(Trp)和酪氨酸(Tyr)存在 C=O 键的紫外吸收。乳清分离蛋白的紫外吸收随着甜菜苷浓度的增加而增加,进一步证明乳清分离蛋白与甜菜苷发生了相互作用,改变了色氨酸和酪氨酸的微环境。吴云雪等观察到了类似的现象,表没食子儿茶素没食子酸酯(EGCG)与乳清分离蛋白发生相互作用,蛋白的紫外吸收随着EGCG 含量的增加而增加。

于 280 nm 的激发波长,测定了 0.6~1.2 mg/mL 乳清分离蛋白的内源荧光强度。从图 3A 可得知,乳清分离蛋白在 0.6~1.2 mg/mL 的浓度范围内蛋白的荧光强度随其浓度呈现先增后减的关系,且分为两段线性关系, 最大值位于 0.9 mg/mL, 因此选择了0.8 mg/mL 的蛋白浓度进行内源荧光实验,该浓度可以避免蛋白浓度过高而引起的内滤效应,提高实验精度。图 3B~D 显示了在 298、304、310 K 温度下,不同浓度甜菜苷对乳清分离蛋白内源荧光的猝灭效果。乳清分离蛋白的色氨酸在 280 nm 的激发波长下在 332 nm 处有最大的荧光发射峰,荧光强度随着甜菜苷浓度的增加而不断下降,表明甜菜苷对乳清分离蛋白有荧光猝灭效果。此外,由图 2 中可知,甜菜苷在 0.2 mg/mL 浓度下,其紫外吸收非常低,(A280+ A332)/2<0.1,这表明甜菜苷对乳清分离蛋白几乎不产生内滤效应,这个荧光强度的下降可能是由于甜菜苷与乳清分离蛋白发生了相互作用并形成复合物,改变了乳清分离蛋白中酪氨酸和色氨酸的微环境。类似的现象也出现在一些多酚与乳清分离蛋白的相互作用中,咖啡酸(CA)、表没食子儿茶素没食子酸酯(EGCG)与乳清分离蛋白通过非共价相互作用结合,猝灭了乳清分离蛋白的内源荧光。

如图4 所示,在298、304、310 K 温度下,Stern-Vo- lmer 方程具有良好的拟合性,表明甜菜苷猝灭为动态或静态单一猝灭类型。由表 1 可知,在 298、304、310 K 温度下,WPI-Betanin 的猝灭常数分别为 2.06×102·mol−1、2.26×102·mol−1 和 2.58×102·mol−1。最小的猝灭速率常数Kq (Kq=KSV/τ0)为 3.32×1010 L·mol−1·s−1明显大于各类猝灭剂对生物大分子的最大动态猝灭速率 2.0×1010 L· mol−1·s−1,表明甜菜苷猝灭乳清分离蛋白内源荧光的机制为静态猝灭过程。对于静态猝灭过程,可以采用双对数方程(2)计算乳清分离蛋白与甜菜苷之间的结合常数和结合位点数。从表1中可知,在不同温度下甜菜苷与乳清分离蛋白的结合常数分别为 1783.16 L/mol (298 K)、672.59 L/mol(304 K)、259.81 L/mol(310 K),结合常数随温度的升高而明显降低,说明温度对乳清分离蛋白-甜菜苷相互作用的影响比较大,温度较低时结合得越紧密, 这可能是因为活性小分子甜菜苷对高温较敏感。温度对结合位点数几乎没有影响,三种温度下的结合位点数均接近 1,表明乳清分离蛋白与甜菜苷以 1:1 的比例复合。


相互作用的 Van’t Hoff 方程为 Y=14827.67X− 42.27(R2=0.99),热力学参数 ΔH 和 ΔS 可由方程的斜率和截距得出。蛋白质与活性小分子之间常常通过静电作用力、疏水作用力、氢键和范德华力等非共价相互作用结合成复合物。根据热力学参数的不同,可判断二者结合的作用力类型。蛋白质与小分子结合时,若 ΔH>0 及 ΔS>0 时,主要表现为疏水作用;若 ΔH<0 及 ΔS>0,主要表现为静电作用;ΔH<0 及ΔS<0,主要表现为氢键或范德华力作用。由表1可知,ΔG 为负值表明 WPI-Betanin 复合物为自发结合的过程,ΔH 和 ΔS 均为负值表明 WPI-Betanin 复合物的形成为焓驱动反应,且主要相互作用为范德华力和氢键相互作用。
疏水基团指示着蛋白质的三级结构,利用ANS 荧光探针探究乳清分离蛋白与不同浓度甜菜苷结合后表面疏水性的变化。由图5 所示,乳清分离蛋白的表面疏水性随着甜菜苷含量的增加而逐渐降低。表面疏水性的降低可能是由于从甜菜苷引入了极性 基团(羧基和羟基)所致。此外,甜菜苷与蛋白质表面上的疏水性氨基酸侧链基团(尤其是芳香环)结合导致荧光探针 ANS 可检测的表面疏水性基团减少, 这两个因素都会导致疏水性降低。表没食子儿茶素没食子酸酯(EGCG)也被观察到能使乳清蛋白的表面疏水性降低,并在 240 μmol/g 的 EGCG 浓度下降低 50%。

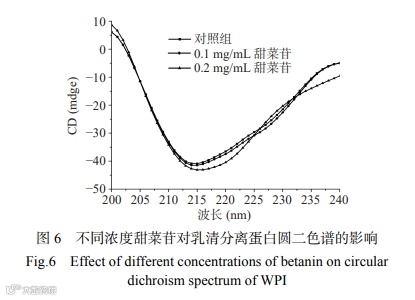
圆二色谱主要反映蛋白质二级结构的变化。图 6 显示,乳清分离蛋白的圆二色谱在 216 nm 附近显示了一个负峰,这是二级结构 β-折叠的特征峰。如表 2 所示,在不存在甜菜苷的情况下,乳清分离蛋白含有 12.5% 的 α-螺旋,31.1% 的 β-折叠,24.4% 的β-转角和 31.9% 的无规则卷曲,随着甜菜苷浓度的增加, α-螺旋含量和 β-转角含量分别降至 10.1% 和 23.8%,而 β-折叠含量增加至 34.2%。由此可推断出,乳清分离蛋白与甜菜苷之间的相互作用可能导致了蛋白质多肽链的部分解折叠,并破坏了用于稳定螺旋结构的氢键,使得蛋白质的结构变得更加松散。花青素与乳清蛋白相互作用也有类似的现象,乳清蛋白与紫薯粉花青素结合后,α-螺旋含量从20.8% 下降到 13.4%,花青素分子在乳清蛋白的 α- 螺旋区域结合,破坏了稳定螺旋结构的氢键。

为了进一步研究乳清分离蛋白与甜菜苷之间相互作用的位置,采用 CDOCHER 分子对接可视化地进行对接模拟。如图7所示,甜菜苷分别与乳清分离蛋白的主要成分 α-乳白蛋白(1NFZ)、牛血清蛋白(3VO3)、乳铁蛋白(1BLF)和 β-乳球蛋白(3NPO)对接,甜菜苷被 WPI 包裹在内部。α-乳白蛋白(1HFZ)的 His 107、 Asn 102、 He 101、 Asp 97 与甜菜苷通过氢键相互作用结合,且 Asn 102 与甜菜苷形成了多个氢键(2.22 Å、5.73 Å、2.32 Å),Lys 108 与甜菜苷有静电相互作用;牛血清蛋白(3V03)与甜菜苷主要通过氢键相互作用结合(Arg 435、Glu 186、 Lys 431、 Arg 144、Leu 112、 Asp 111);乳铁蛋白(1BLF)的 Ser 185、 His 253、Glu 187、Pro 188 与甜菜苷形成 氢键,Asp 197、 Glu 15、 Lys 197 通过静电相互作用与甜菜苷结合;β-乳球蛋白(3NPO)主要通过氢键(Gln 120、Pro 38)和静电相互作用(Phe 105)与甜菜苷结合。总体而言,四种蛋白质与甜菜苷结合以氢键相互作用为主,与圆二色谱数据结合,可推断甜菜苷被包裹在蛋白质中,与乳清分离蛋白中 α-螺旋结构中的氨基酸发生了大量的氢键相互作用,从而破坏了蛋白质 α-螺旋中原有的氢键,降低了 α-螺旋的含量。





食品科学家论文汇总
(点击专家姓名,查看论文)













《食品工业科技》特邀主编专栏征稿
《食品工业科技》青年编委专栏征稿:AI for Food Industry:人工智能在食品工业中的应用 ☚
《食品工业科技》青年编委专栏征稿:组学分析技术在食品品质研究中的应用 ☚
群聊:食品工业科技作者群

温
馨
提
示

我刊正式组建微信作者群,为作者提供更多的学术与论文资讯,如需进群,请联系刘老师(微信:上方二维码,电话:87244117-8062)。

版权声明














