

撰稿|由课题组供稿
等离激元超构表面凭借免标记、高灵敏等优势有望被广泛应用在生物传感和医学检测等领域。与传统的金、银等贵金属等离激元材料相比,铝具有储量丰富、工作波段范围广以及自由电子密度高等优点,但是其传感应用常受到紫外光工作波段和表面氧化的限制。近日,厦门大学朱锦锋教授团队联合杨志林教授团队,开发一种晶圆级铝基等离激元超构表面的高灵敏生物分子传感方法,在牛血清蛋白抗体的免疫检测中获得了1 pg / mL的检测极限(Limit of Detection,LOD),比相同结构金超构表面的灵敏度提高两个数量级,展现了铝基超构表面优越的生物分子免疫检测能力和临床应用潜力。相关成果以“Wafer-Scale Flexible Plasmonic Metasurface with Passivated Aluminum Nanopillars for High-Sensitivity Immunosensors”为题发表在国际期刊Sensors and Actuators B上。
传统的等离激元超构表面对金、银等贵金属材料的使用具有强烈的依赖性,这在成本上很大程度限制了便携式生物医学检测系统的发展。铝作为一种具有高自由电子密度特性的金属材料在该领域具有很大的应用潜力。但是其等离激元模式常作用于紫外光波段,较大的介电常数虚部和较长的光场衰减长度制约了其在可见光波段的传感能力;另一方面,铝作为一种活泼金属,表面极易氧化,这也极大影响铝纳米材料的等离激元特性和表面生物分子传感性能。此项工作实现了铝基超构表面诱导的可见光波段等离激元共振模式,综合运用纳米压印、氧等离子体刻蚀、金属薄膜沉积、氧等离子体钝化等工艺,在柔性聚合物衬底上制备2英寸铝基纳米柱超构表面圆片(如图1所示),所制备的铝基超构表面具有晶圆级的纳米结构均匀性,柔软轻薄,适合大规模、大面积加工制造,有望很好地应用于柔性可穿戴便携式生物传感器件与系统的开发。

图1:铝基等离激元超构表面的制备工艺、实物照片以及不同氧等离子体刻蚀条件下的扫描电镜图
通过对比研究(如图2a所示),相同阵列结构的金超构表面和铝基超构表面体灵敏度分别为428 nm / RIU 和553 nm / RIU,因此铝基超构表面的体灵敏度是金的1.3倍。为了进一步分析两者表面灵敏度性能,该研究分别采用沉积共形的氧化铝薄膜和自组装聚电解质双分子层进行光谱测量和分析。图2b的结果表明,在沉积20 nm 氧化铝薄膜的情况下,金超构表面的波长仅红移5.2 nm,而铝基超构表面的波长则红移9.25 nm。图2d的表面沉积聚电解质双分子层实验结果表明,随着双分子层数的不断增加,金超构表面在沉积10对双分子层后就达到了波长红移的饱和,总偏移量为14.46 nm,而铝基超构表面沉积15对双分子层后才达到波长红移的饱和,总偏移量高达49.69 nm。这些实验结果体现了铝基纳米柱超构表面具有较强的近场传感性能,与相同结构的金超构表面相比具有更优越的表面灵敏度。
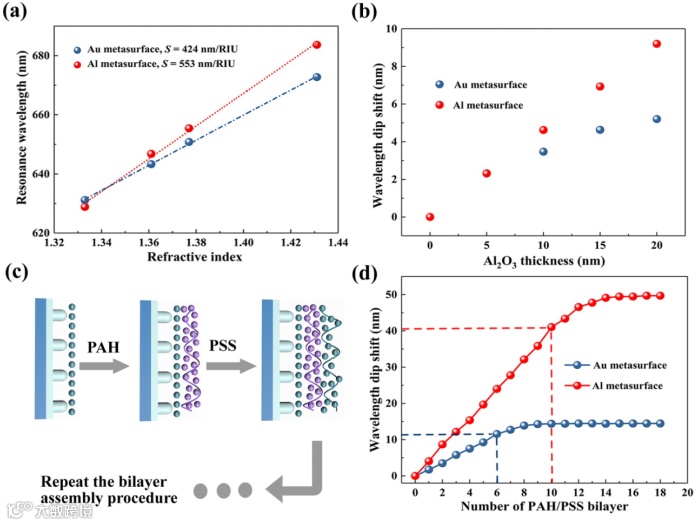
图2:铝基超构表面与金超构表面的表面传感性能比较
为了进一步测试铝基超构表面在生物检测中的应用,该研究还采用了牛血清蛋白的抗原/抗体的免疫功能化检测方法(如图3a所示)来评价其生物分子传感性能。如图3d所示,该研究对不同浓度牛血清蛋白抗体传感的波长偏移量采用希尔函数和最小二乘法进行拟合,结果表明氧等离子体表面钝化的铝基超构表面最大波长偏移量高达6.43nm,是金超构表面的2.38倍,传感线性区所体现的灵敏性能也大大高于金超构表面。免疫检测结果还表明铝基超构表面的牛血清蛋白抗体LOD低至1 pg/mL,远小于金超构表面(~100 pg/mL)。综上所述,该研究所开发的柔性衬底铝基超构表面具有很好的免疫特异性结合传感性能,在生物分子的医学检测上具有广阔的应用前景。

图3:铝基超构表面的免疫分子传感检测性能及其与金超构表面的比较
以上研究成果将晶圆级铝基等离激元超构表面应用于高灵敏生物分子传感,克服了铝基等离激元超构表面在生物医学检测上的工程应用难题,为铝基超构表面后续在肿瘤标志物、新型冠状病毒抗原抗体等检测上的应用确立了较好的科研基础,具有很好的创新性和产业推广价值。该工作得到国家自然科学基金、国家科技部基金项目、福建省杰出青年科学基金等研究经费的支持。

https://www.sciencedirect.com/science/article/pii/S0925400521007395

免责声明:本文旨在传递更多科研资讯及分享,所有其他媒、网来源均注明出处,如涉及版权问题,请作者第一时间后台联系,我们将协调进行处理,所有来稿文责自负,两江仅作分享平台。转载请注明出处,如原创内容转载需授权,请联系下方微信号。




