

撰稿|由课题组供稿
利用飞秒激光双光子聚合技术构建微结构用于特定功能应用,已成为微纳制造领域的研究热点。而如何改进现有激光直写工艺,开发一种灵活简便、减少对设备需求的新型加工策略,对双光子聚合技术和微器件制备的发展具有重要意义。近日,中国科学技术大学吴东教授团队利用全息调制的飞秒激光动态三维多焦点加工策略,在无需外部移动台扫描运动的前提下实现了3D可变形功能微结构的灵活快速制备,并展示了在微粒子捕获、细胞培养等方面的应用。相关成果以“Functional Shape-Morphing Microarchitectures Fabricated by Dynamic Holographically Shifted Femtosecond Multifoci”为题发表于《Nano Letters》期刊。
飞秒激光双光子聚合技术由于具有极高的加工精度和真三维加工能力,在微纳制造领域占有着越来越重要的地位。但是,传统的激光单点直写存在效率低的问题,目前的主流加工策略是利用高频工作的转镜控制焦点高速扫描,或采用空间光调制器(SLM)等器件将光束调制成多焦点或特定光场来进行并行扫描加工。这两种方法都极大地提高了激光直写的效率,但加工过程都依靠位移台、转镜等机械部件,这既增加了对硬件设备的需求,也需要复杂的控制软件来协同机械部件的高精度运动。
近年来,研究者们将飞秒激光双光子聚合技术与具有刺激响应能力和良好生物兼容性的智能水凝胶材料结合,构建出可调谐功能性微结构并应用于微型粒子和细胞的操纵,在生物医学等领域展现了广阔的发展前景。然而,现有双光子聚合打印水凝胶的方法局限于传统的转镜扫描,还有待开发对设备需求低、操作更简便的新型水凝胶加工策略。
针对上述挑战,研究团队提出了基于新型的SLM光场调制技术,也就是通过在全息图上叠加透镜因子来控制多焦点在样品中的三维扫描加工,整个加工过程无需任何位移台。首先,采用加权Gerchberg-Saxton(GSW)算法由目标点阵分布获得相应的全息图,加载到SLM上,可在加工系统焦面上得到xy平面内的任意焦点分布。然后,在全息图上叠加特定的透镜相位因子,可控制焦平面沿轴向的偏移量,从而调控焦点阵列在z方向上的位置,如图1a,b所示。基于这种全息图设计原理,将一系列预先计算好的全息图依次在SLM上播放,再现的多焦点就能按设计的3D轨迹运动。通过协调各焦点的运动,可实现复杂3D结构的灵活快速构建,如图1c所示。这种加工策略仅利用单个SLM即可控制焦点的3D扫描,在加工过程中不需要依赖外部运动,可省去现有双光子聚合加工必需的压电台、转镜等机械设备,降低了对加工设备的控制、维护需求。同时,之前报道的多焦点加工策略大多局限于单一焦点阵列的扫描,只适用于固定结构阵列的构建,而本方法能够控制多焦点沿各自独立的路径运动,具有更高的灵活性,使更复杂多样化结构的制备成为可能。

图1.(a)SLM动态三维多焦点加工光路;(b)叠加透镜因子控制多焦点在3D空间中的位置分布;(c)动态多焦点构建3D微结构过程
可调谐微结构在诸多领域具有重要的应用价值,因此研究团队选用一种丙烯酸基水凝胶作为加工材料,用该方法在其中构建了一系列多样化3D结构,如图2a所示。得益于水凝胶的pH响应特性,可通过切换周围溶液的酸碱性来调控微结构的收缩与膨胀(见图2b,c)。研究团队设计了一种微笼结构以展示所构建水凝胶器件的功能性应用。如图3a所示,在膨胀状态下微颗粒可自由进入微笼,在收缩状态下微笼能将微颗粒限制在内部。利用动态多焦点快速制备大面积微笼阵列,可实现大数量微粒的高效捕获。研究团队又进一步制备了六边形支架阵列,可支持HeLa细胞的3D生长、增殖、迁移(见图3b)。除此之外,由于水凝胶的大孔隙率,支架结构可通过简单的浸泡装载抗癌药物,并缓慢释放作用于支架中的HeLa细胞。如图3c所示,装载不同浓度药物的支架阵列对癌细胞生长表现出不同的抑制效果,为医学研究提供了一种潜在的药效筛选手段。

图2.(a)动态全息三维多焦点在水凝胶中构建的多样化结构SEM图;(b)水凝胶微结构pH响应示意图;(c)水凝胶微结构的pH调节收缩与膨胀显微照片
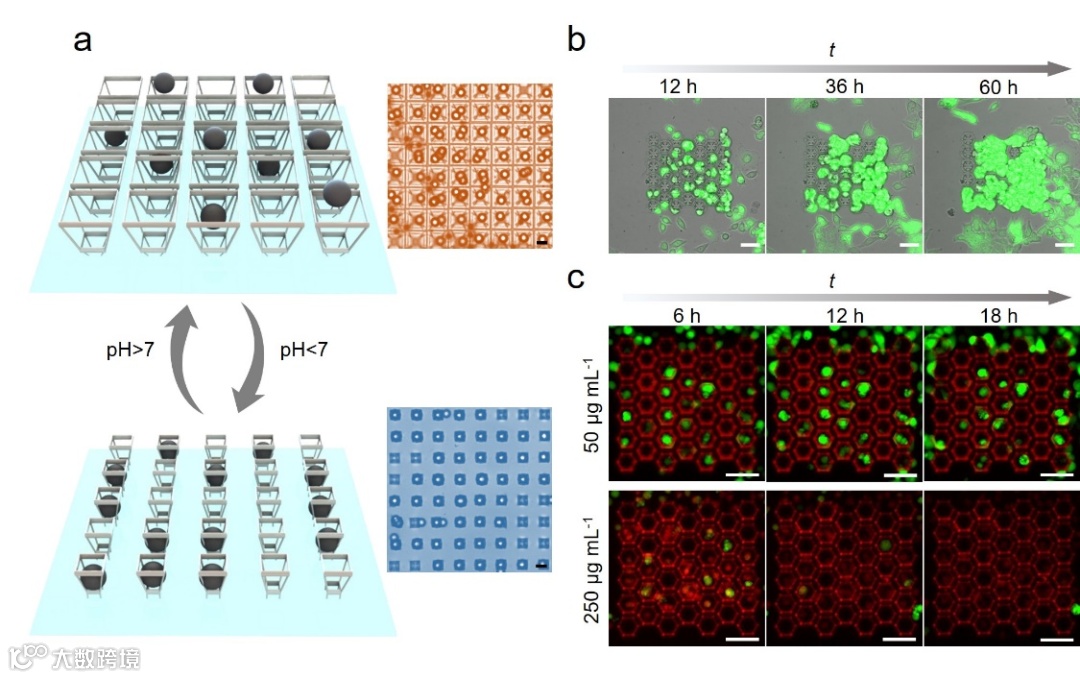
图3.(a)水凝胶微笼阵列pH响应捕获微粒;(b)微支架阵列用于培养HeLa细胞;(c)微支架阵列装载不同浓度药物测试癌细胞抑制效果
本工作提出的三维动态全息多焦点加工方法无需任何机械移动部件就能实现复杂3D结构的制备,简化了双光子聚合加工工艺的设备需求。该方法在水凝胶中构建pH响应微结构,为智能响应性材料的双光子聚合打印提供了一种灵活简便的替代途径。通过与更高分辨率的双光子聚合技术和更多样的新型智能响应材料结合,这一加工方法在将来有望为生物医学等领域提供高性能的功能器件。
中国科学技术大学博士生张乐然、博士后刘炳瑞为本文第一作者,汪超炜特任副研究员、吴东教授为通讯作者。这项工作得到基金委重大仪器、科技部重点研发计划、中国博士后科学基金等项目的资助。

文章链接:
https://pubs.acs.org/doi/10.1021/acs.nanolett.2c01178
免责声明:本文旨在传递更多科研资讯及分享,所有其他媒、网来源均注明出处,如涉及版权问题,请作者第一时间后台联系,我们将协调进行处理,所有来稿文责自负,两江仅作分享平台。转载请注明出处,如原创内容转载需授权,请联系下方微信号。




