


图1 本研究设计的示意图
基因工程已经彻底改变了现代生物学和医学,其中一个核心能力是精确地操纵DNA序列,以发现遗传学的奥秘,纠正遗传疾病,并推进医学治疗。DNA序列中目标位点的精确性可以被编辑是至关重要的,因为它支配着遗传信息的完整性,并影响着许多生物和医学应用的发展。近年来,基因工程领域取得了突破性的进展,最显著的是集群规则间隔短回文重复序列(CRISPR)和相关蛋白系统(CRISPR-Cas)的出现,已经具有空前的特异性和多功能性启动了基因编辑。
然而,像CRISPR这样的酶基基因编辑工具也面临着挑战。虽然基于酶的基因编辑方法提供了前所未有的精度,但它们对生物机制的依赖带来了固有的局限性,包括对某些反应条件的严格要求,包括离子浓度、温度、PH值等,这样的局限性强调了创新的DNA切割方法的重要性。该课题组提出了一种创新的纳米剪刀系统,称之为“TADPOLE(蝌蚪)(Targeted DNA Precision Oriented Laser Excision靶向DNA精确定向激光切除)”。利用飞秒激光照射下由多光子吸收(MPA)激发的黑磷量子点(BPQDs)产生的活性氧(ROS)来进行定点核酸片段切割。在本研究中,采用互补RNA序列的整合有助于高效的站点选择性DNA切割,除了利用量子点靶向任意DNA序列的精度外,蝌蚪还利用了BPQDs独特的多光子吸收特性,使在未来适合在体内应用的低能量光源进行激发。此外,这种创新的剪切方法集成了引导RNA和超快激光技术,以提供对局部ROS产生和最小热产生的精确控制。这保证了位点特异性DNA的切割,同时降低了对非靶向序列造成的损伤风险。重要的是,研究证明了蝌蚪对环境因素的优越耐力,包括温度波动、变化的离子浓度(Na+和Mg2+)和pH值,优于传统的酶,如CRISPR。
在图1中,我们展示了DNA链(“尾巴”)引导的黑磷量子点(“头部”)系统的功能,精确捕获任意序列的反向互补DNA链,由800 nm激光触发切割。
方法机理:超快激光通过BPQD的MPA激发ROS
在研究中介绍了活性氧的产生机理及其与超快激光和多光子吸收的相互作用。
活性氧的产生机理:
少层黑磷(BP)的带隙因其厚度而变化,从0.3 eV(bulk BP)到2eV(单层BP)。BPQDs具有量子尺寸效应,表现出更宽的带隙。当暴露在光子能量等于或大于其带隙的可见光下时,BPQDs会经历从价带到导带的电子激发,产生电子-空穴对。这些载流子可以迁移到BPQDs的表面。电子被转移到被吸附的上,导致形成高活性的过氧物质 。同时,价带上的光生孔穴被表面吸附的羟基和水分子捕获,从而在BPQD表面产生
。同时,价带上的光生孔穴被表面吸附的羟基和水分子捕获,从而在BPQD表面产生 自由基。这种定位的
自由基。这种定位的 生产使在BPQDs附近精确的DNA裂解。采用了脉冲持续时间约为100 fs的超快激光器,以确保位点选择性DNA切割的准确性和有效性。这种方法对目标纳米材料提供了高选择性,同时保留了非靶向DNA序列。切割效率受“尾”RNA与目标DNA序列和目标DNA序列相互作用的影响。高温会导致DNA-RNA杂交体的解离,即使碱基配对是正确的。超快激光器主要提高BPQD附近的温度,保持“尾巴”RNA的结合能力。超快激光烧蚀的特点是由于多光子吸收而在焦体积外的热扩散有限,使其成为通过多光子吸收激发ROS的理想方法。在本研究中,其独特的MPA特性的无数优势有助于实现精确的定点DNA切割。此外,这些特性为蝌蚪系统在生物体中的未来应用奠定了基础。通过最小化意外损伤的风险,并确保有效的组织渗透。
生产使在BPQDs附近精确的DNA裂解。采用了脉冲持续时间约为100 fs的超快激光器,以确保位点选择性DNA切割的准确性和有效性。这种方法对目标纳米材料提供了高选择性,同时保留了非靶向DNA序列。切割效率受“尾”RNA与目标DNA序列和目标DNA序列相互作用的影响。高温会导致DNA-RNA杂交体的解离,即使碱基配对是正确的。超快激光器主要提高BPQD附近的温度,保持“尾巴”RNA的结合能力。超快激光烧蚀的特点是由于多光子吸收而在焦体积外的热扩散有限,使其成为通过多光子吸收激发ROS的理想方法。在本研究中,其独特的MPA特性的无数优势有助于实现精确的定点DNA切割。此外,这些特性为蝌蚪系统在生物体中的未来应用奠定了基础。通过最小化意外损伤的风险,并确保有效的组织渗透。
非线性光学性质的研究:
在研究黑磷量子点(BPQDs)的非线性光学性质时,我们采用了开孔径z扫描技术。该方法有助于检测BPQDs对强激光照射的响应,特别是在800 nm波长下,揭示了独特的光子-物质相互作用,对本研究具有重要意义。强光−物质相互作用诱导了一些高阶非线性光学过程,导致材料特异性吸收和折射特性的显著改变。这些变化可以用以下方程式进行数学描述:

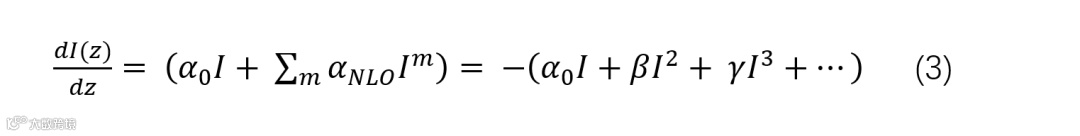
 是基于m,其中m = 1为双光子吸收(2PA, β),m = 2为三光子吸收(3PA, γ)等。合成的归一化透射率表示为:
是基于m,其中m = 1为双光子吸收(2PA, β),m = 2为三光子吸收(3PA, γ)等。合成的归一化透射率表示为:
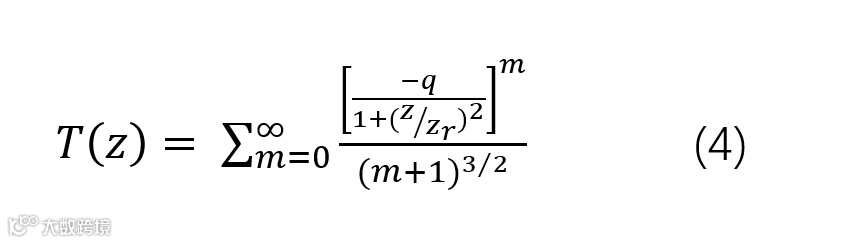
 是焦点,
是焦点, ,处的峰值强度,即瑞利长度,
,处的峰值强度,即瑞利长度, ,表示有效样品长度,L是样品的厚度。在存在占优势的高阶吸收效应时。
,表示有效样品长度,L是样品的厚度。在存在占优势的高阶吸收效应时。
光强度(I)可以描述为:


图2 蝌蚪ROS产生机理及其非线性光学特性 A. 在超快激光照射下,BPQDs产生ROS的示意图。BPQDs吸收能量等于或大于其带隙的光子,产生1O2 -用于位点选择性DNA切割。超快激光器确保了高选择性。B. z扫描分析揭示了双光子吸收(2PA)的BPQDs的非线性光学性质。C. ESR光谱学证实了ROS的种类。BPQD/Ags表现出增强的ROS生成。D,E和F.瞬态吸收(TA)光谱和单波长动力学的测量。
为了研究在复杂的生理环境中的定点基因切割活性,我们在活细胞中使用了光激活的DNA切割系统。单链DNA(ssDNA)模板如上所述进行标记,在“蝌蚪”的“尾巴”上再标记Cy5(SH-DNA-Cy5)。在图3中,用标记的ssDNA、MCF-7(ATCC HTB-22)和MDA-MB-231(ATCC HTB-26)转染标记的ssDNA或只包含“蝌蚪”(SH-DNA)或整个“蝌蚪”(BP/Ag@SH-DNA)的不匹配的SsDNA。使用共聚焦显微镜监测细胞内荧光,无论是有照射还是不照射30分钟。
值得注意的是,只有正确配对的ssDNA和BP/Ag@sh-DNA转染的细胞在照射后显示出FAM信号荧光,并与相应的纳米颗粒共定位。这一结果与体外实验的结果一致,提供了确凿的证据,表明恢复的荧光来自于由“蝌蚪”促进的活细胞中的特定DNA断裂。这些实验结果验证了已开发的光活性“蝌蚪”在活细胞中的成功应用,显示了其在高特异性精确切割DNA的能力。
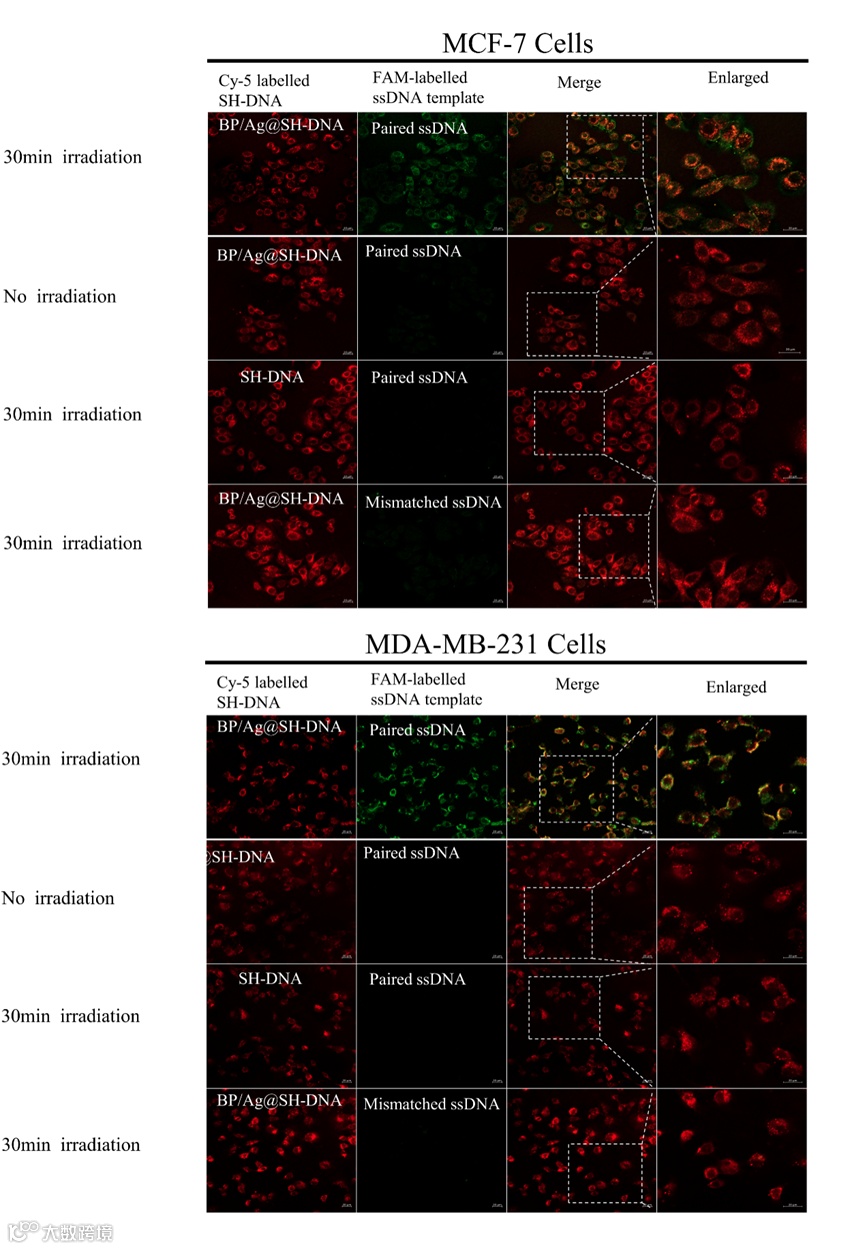
图3 细胞验证实验
共聚焦显微镜图像显示了转染标记单链DNA(ATCC HTB-22)、MCF-7(ATCC HTB-2NA(“蝌蚪”-SH-DNA的“尾巴”)或完整的“蝌蚪”结构(BP/Ag@SH-DNA)不匹配的ssDNA)后的细胞内荧光。ssDNA模板按照描述进行标记,“蝌蚪”“尾巴”另外标记了Cy5(SH-DNA-Cy5)。在照射30分钟和不照射30分钟后,均监测细胞内荧光。观察到的荧光信号,特别是来自正确配对的ssDNA和BP/Ag@SH-DNA样本,证实了光活性“蝌蚪”诱导的活细胞内特异性DNA断裂,验证了其在生物学背景下的有效性和位点特异性。
在本研究中,蝌蚪系统在位点定向基因切割领域取得了显著的进展,为位点定向DNA切割提供了一个新的、精确的平台。利用黑磷量子点(BPQDs)通过多光子吸收(MPA)的特殊非线性光学性质,我们成功地实现了在超快激光照射下活性氧(ROS)的生成。位点靶向RNA序列的整合促进了任意的位点特异性DNA切割,将本研究中开发的创新方法封装为术语“蝌蚪(TADPOLE)”(靶向DNA精确定向激光切除Targeted DNA Precision Oriented Laser Excision)。
蝌蚪的一个显著特征是它在不同环境条件下的稳健性能,超过了传统的基于CRISPR的方法。蝌蚪对温度、氯化钠和氯化镁浓度以及pH水平的变化表现出更强的耐力。重要的是,该系统利用了BPQDs的多光子吸收特性,使低能量光源能够激发,使其适合于体内应用.引导RNA和超快激光技术的集成提供了对局部ROS产生和最小热量产生的精确控制,保证了位点特异性DNA的切割,同时最大限度地减少对非靶向序列的损伤风险。蝌蚪在广泛的条件下保持高活性的能力增强了其实用性。此外,在活细胞中进行的光触发DNA裂解实验证明了蝌蚪系统在复杂生理环境中的适应性和有效性。在人类腺癌细胞中观察到的位点特异性DNA断裂证实了该系统的精确性和特异性,即使是在活细胞的复杂环境中。光活性“蝌蚪”在活细胞中的成功应用凸显了其未来生物学应用的潜力,为基因工程、生物技术和医学的进步铺平了道路。
总之,“飞秒激光剪刀”在基因切割方面显示出了转化的潜力,为传统的酶基方法提供了一个精确和有弹性的替代方法。我们的研究建立了一个坚实的基础,展示了在活细胞的适应性和有希望的体内应用。随着超快激光激发、深穿透波长的利用和在复杂环境中的多功能性,“飞秒激光剪刀”成为推进体内基因切割技术的有力候选者。

图4 “飞秒激光剪刀”的优势与前景
Light-guided Genetic Scissors Based on Phosphorene Quantum Dot
Zhi Chen#; Hao Huang#; Jiefeng Deng#; Changle Meng#; Yule Zhang; Taojian Fan; Lude Wang; Shuo Sun; Yi Liu; Huiling Lin; Shuang Li; Yunpeng Bai; Lingfeng Gao; Junle Qu; Dianyuan Fan; Xueji Zhang; Han Zhang*
DOI:10.1002/lpor.202400777

论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/lpor.202400777




