


医美类 医疗器械
合规准入概述

1
•医美类医疗器械分类
2
•合规准入程序
3
•临床评价策略
4
•临床试验流程

定义
01



属性、监管
01

举例
01

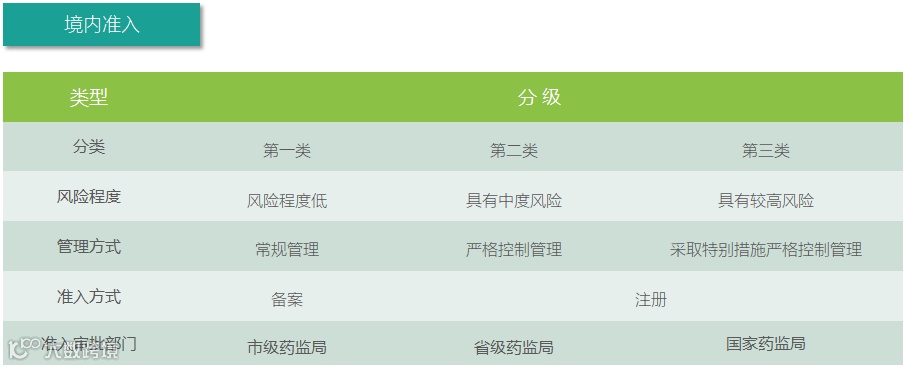
准入程序


产品研制-设计开发
02

产品分类-根据属性分类
02


医疗器械分类-不同类别监管方式
02

产品检验
02

办法 第三十二条
申请注册或者进行备案提交的医疗器械产品检验报告可以是申请人、备案人的自检报告,也可以是委托有资质的医疗器械检验机构出具的检验报告。
临床评价
02
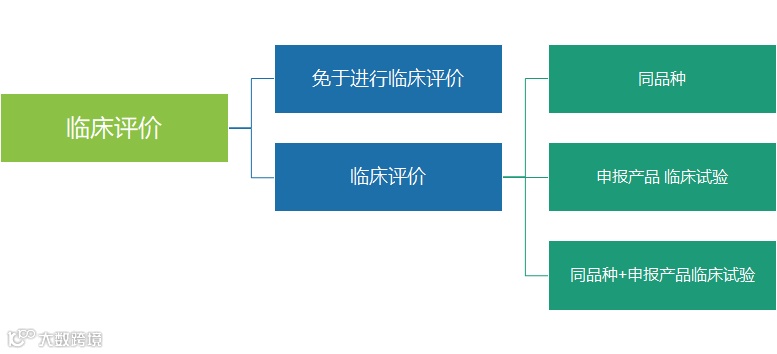
办法 第三十三条
医疗器械临床评价是指采用科学合理的方法对临床数据进行分析、评价,以确认医疗器械在其适用范围内的安全性、有效性的活动。
申请医疗器械注册,应当提交临床评价资料。
办法 第三十四条
免于进行临床评价的,可以免于提交临床评价资料。
免于进行临床评价的医疗器械目录由国家药品监督管理局制定、调整并公布。
产品注册
02

资料整理


证照格式
02


CMDE推荐策略
03
光电类
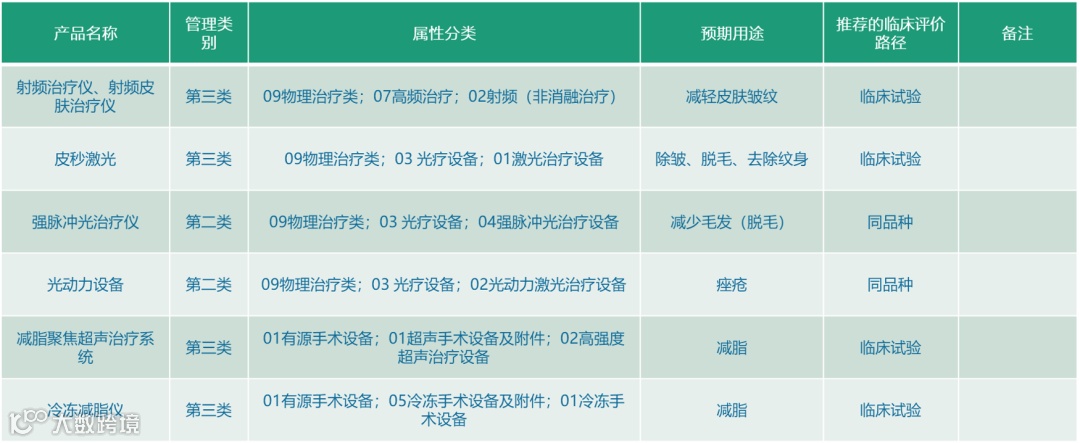
植入类

敷贴类



相关方
04

相关角色方
04

一般流程
04

参考
04
Ø医疗器械监督管理条例,2021年第76号
Ø医疗器械注册与备案管理办法,2021第47号
Ø体外诊断试剂注册与备案管理办法,2021第48号
Ø医疗器械临床试验质量管理规范,2022年第28号
ØClinical investigation of medical devices for human subjects — Good clinical practice,ISO 14155-2020,Third edition 2020-07
Ø医疗器械分类界定目录(含历年增补)
Ø免于开展医疗器械临床评价目录
医疗器械全生命周期
临床研究服务 CRO

更多医美产品合规准入,请关注公众号,或添加微信。



END








