导读
ENTER TITLE
光热疗法是近年来兴起的一种新型治疗癌症的方法,纳米材料在其中扮演着肿瘤杀手的角色。近日,北京化工大学徐福建教授、赵娜娜教授研究团队以及美国芝加哥伊利诺伊大学的程刚教授共同合作,成功制备了多种包封金纳米棒的自毁性多糖纳米复合材料(记作Au@PSa),并将其作为关键的光热转换材料有效应用到了癌症的光热治疗系统。这种复合材料具有自适应的自毁特性,可以在细胞质基质中释放包封的金纳米棒,并且数量可以控制。与传统疗法相比,Au@PSa具有更高效的光热转换效率以及优异的光热效应,在癌症治疗中表现出了良好的治疗效果[1]。相关成果以“Self-destructible polysaccharide nanocomposites with unlockable Au nanorods for high-performance photothermal therapy”为题发表在NPG Asia Materials杂志上。
迄今为止,癌症仍然是一种致命性疾病,也是导致世界人口死亡的主要原因。医学上为了克服这一难题,已经开发了多种治疗模式,例如化疗和光热疗法(PTT)。光热疗法是近年来兴起的治疗肿瘤的一种新方法,其原理是人为注入光热转换材料,利用靶向识别技术将其聚集到肿瘤区域,在近红外光的照射下将光能转换为热能,肿瘤组织产生局部高热,导致癌细胞死亡[2-3]。光热疗法的关键是能够获得高光热转换效率的材料。
多功能的有机/无机纳米复合材料一直以来都是生物医学领域研究人员关注的重点,在这项研究中,研究者将制备的包封金纳米棒的自毁性多糖纳米复合材料(多糖指葡聚糖和普鲁兰多糖,分别记作Au@Dex和Au@Pul)作为光热转换材料,将其应用于癌症的光热治疗系统中。这种多糖纳米复合材料能够在酸性环境和高浓度谷胱甘肽(GSH)作用下发生响应性自我破坏,在细胞质基质中释放出大量包封的金纳米棒。金纳米棒(Au NRs)是一种良好的光吸收材料,与近红外光接触可以实现高效的光热转换,利用金纳米棒的强吸收,还可以动态检测到治疗过程中的实际光热性能。此外,由于普鲁兰多糖具有良好的生物兼容性,因此Au@Pul纳米复合材料能够对HepG2细胞表现出极好的亲和力;其肝细胞靶向特性还能够有效降低副作用,从而进一步增强治疗效果。值得一提的是,Au@PSa材料在光热疗法上的应用仅仅是一方面,多糖中丰富的羟基可以被用来引入更多的功能,从而使Au@PSa材料实现其它更多方面的生物医学应用。


a,b:不同类别Au@PSa纳米复合材料的TEM图像;
c,e:Au NRs和Au@PSa纳米复合材料的紫外可见光谱;
d,f:水和200 μg/mL的Au@PSa溶液在波长808 nm (2 W/cm2)照射下的温度变化
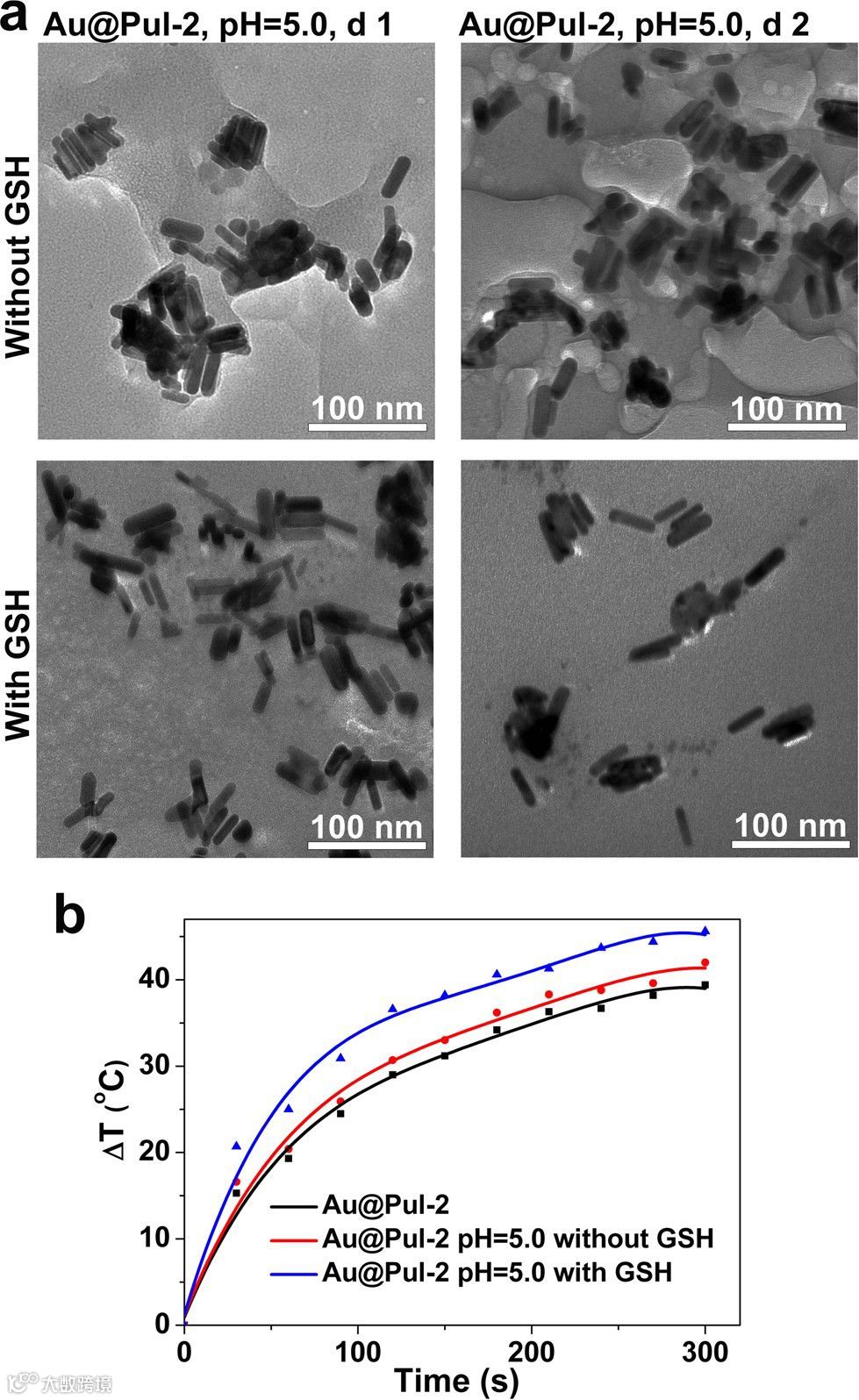
a:pH=5时Au@ Pul-2在有无GSH条件下的TEM图像;
b:pH=5,t=4h,wavelength=808nm,c=200 μg/mL时Au@Pul-2溶液在有无GSH条件下的温度变化图像

a:分别用Au@Dex-2和Au@Pul-2处理C6和HepG2细胞4h后的荧光图像和流式细胞术分析结果;
b:分别用Au@Dex-2和Au@Pul-2处理0.5小时和4小时的HepG2细胞CLSM图像,其中用FITC标记的纳米复合物呈绿色,用DAPI标记的细胞核呈蓝色

a.定量分析:用电感耦合等离子体质谱(ICP-MS)测定HepG2细胞中Au@Dex-2和Au@Pul-2的An含量(存在显著性差异,P<0.05);
b.在HepG2细胞孵育4h后从细胞摄取的Au@ Dex-2(b)和Au@Pul-2(c)代表性生物TEM图像

a.Au@Dex-2和Au@Pul-2在10%胎牛血清(FBS)培养基中的粒径随时间的变化图像(平均±SD,n=3);
b.分别用Au@Dex-2和Au@Pul-2处理的HepG2细胞在有无NIR照射的条件下,细胞活性随浓度的变化图像(平均±SD,n=6;存在显著性差异,P<0.05);
c.用FDA-PI染色的HepG2细胞的三幅代表性荧光图像:仅NIR照射、仅Au@ Pul-2(30μg/ml)处理、既经过Au@ Pul-2(30μg/ml)处理又进行NIR照射

a,b.在有无808 nmNIR光源照射下,将PBS(作为对照组)或Au@Pul-2注射到HepG2荷瘤小鼠体内得到的红外热像(图a)和温度变化(图b);
c.经上述不同处理后,肿瘤的大小、重量随时间变化的依赖性生长曲线及照片;
d,e.荷瘤小鼠体内肿瘤(图d)和主要器官心脏、肝、脾、肾、肺(图e)的H&E染色图像;比例尺:50μm
在这项实验中,研究人员通过一种简单可行的方式制备了包封Au NRs的Au@PSa纳米复合材料,其响应性自我破坏可以在细胞基质内解锁不同含量的金纳米棒,从而获得更好的光学性能,并在体内实现了优异的光热转化。这项研究工作不仅为合成Au@PSa纳米复合材料提供了一种通用方法,同时也成功构建了具有自适应自毁功能的灵活治疗平台。值得一提的是,由于多糖有丰富的羟基群,对该官能团的进一步功能设计可以把这种纳米复合材料应用到其它生物医学应用领域上去,这也为其它研究者去设计更多合理的多功能治疗平台提供了一条新思路。
[1] Self-destructible polysaccharide nanocomposites with unlockable Au nanorods for high-performance photothermal therapy. By Lizhi Song1, Xin Zhou3, Xiaoguang Dai, Ranran Wang, Gang Cheng, Nana Zhao and Fu-Jian. NPG Asia Materials, 06 Jun 2018.
[2] Day.Elucidating the Fundamental Mechanisms of Cell Death Triggered by Photothermal Therapy. By Jilian R. Melamed, Rachel S. Edelstein, and Emily S. ACS Nano
[3]Huang X,Jain PK,EI-Sayed IH,et al.Plasmonic photothermal therapy(PPTT) using gold nanoparticles.By Huang X,Jain PK,EI-Sayed IH,et al. Lasers Med Sci,2008,23(3):217-228
作者:Jane Chou
编辑:Jane Chou


免责声明:本文旨在传递更多科研信息及分享,提供志同道合者的交流平台。如涉及侵权,请联系下方邮箱,我们将及时进行修改或删除。转载请注明出处,如原创内容转载需授权,请联系下方微信号。
邮箱:zunzun@imeta-center.com
微信号:Jessica_2313


