
疟疾(malaria)是一种由疟原虫(plasmodium parasites)寄生在人体而引起的一种寄生虫病。通过蚊虫叮咬,疟原虫可以在人群中快速传播。每年,全球有2亿人受到疟疾的困扰,并有50万人死于疟疾。对抗疟疾除了阻断蚊虫叮咬的传播之外,开发能够杀死,抑制疟原虫在人体繁殖的药物也有着重要意义。为了实现后者,我们得首先了解疟原虫在人体的发展路径。
首先,蚊虫叮咬人体,疟原虫经过蚊虫的口器进入血液。进入血液的疟原虫最先到达人体的肝脏,等繁殖到一定程度后,肝细胞坏死,释放大量的疟原虫再次进入血液,并最终寄生在红细胞内。
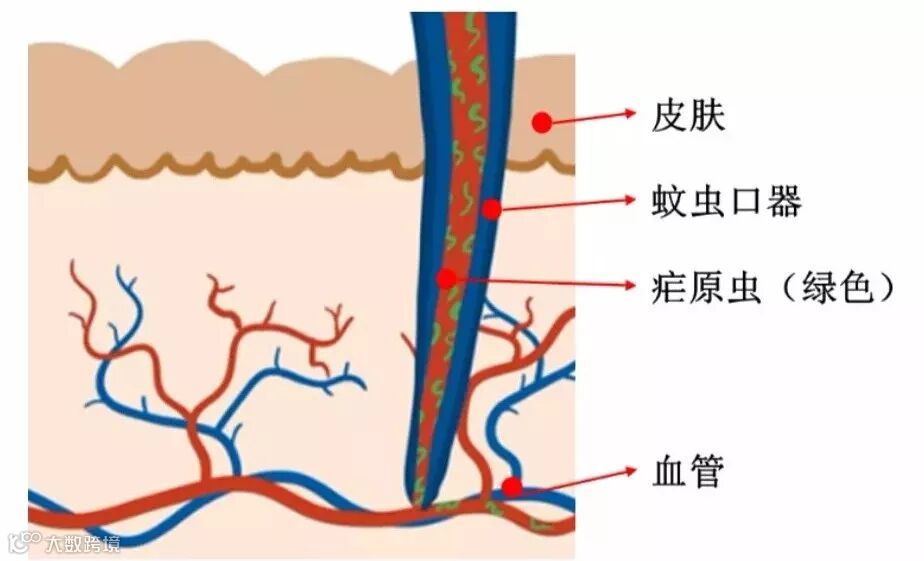
图1. 疟原虫经过蚊虫口器传播
随后,进入到红细胞的疟原虫经过早期的滋养子(early trophozoite),晚期的滋养子(late trophozoite)到最后的繁殖体(schizont),这样一整个生命周期只需要几天甚至更短的时间,所以疟原虫可以在人体内快速大量繁殖。

图2. 疟原虫在红细胞内的生命周期
有趣的是疟原虫进入细胞之后,它将会获取一片红细胞的细胞膜包裹自己,因而在红细胞内形成一个空泡结构(parasitophorous vacuole)。为了更好地从红细胞里获取营养物质和排除代谢产生的废物,疟原虫要分泌成千上百种效应蛋白(effector proteins)。生活在空泡里的疟原虫像是呆在家里一样安全,但是这样的一个“家”却也阻碍了效应蛋白从空泡里进入红细胞基质内。 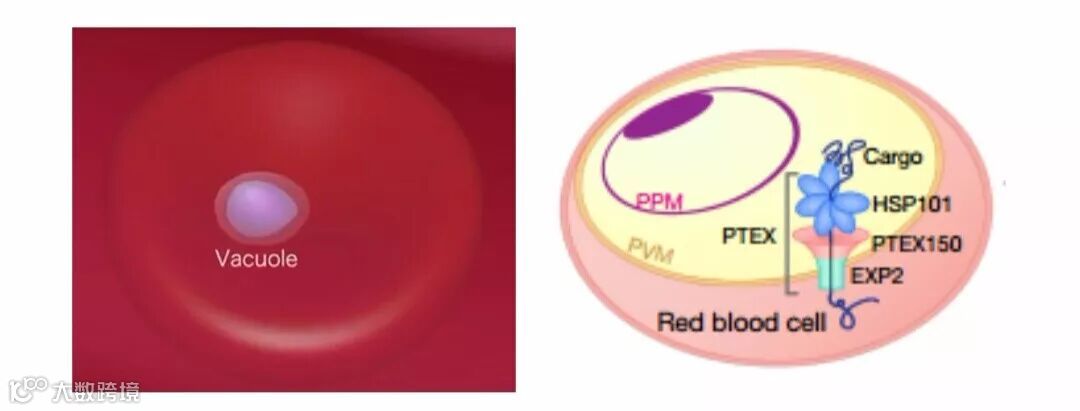
图3. 疟原虫生活在红细胞内的空泡结构内(左),人类感染恶性疟原虫红细胞示意图(右)(PPM, parasite plasma membrane寄生虫质膜;PVM, parasitophorous vacuole membrane液泡膜)
为了解决这个问题,疟原虫搞出了一种新奇的跨膜蛋白,疟原虫输出蛋白转运体(plasmodium translocon of exported proteins, PTEX),PTEX就是将这些疟原虫效应蛋白运输到红细胞中的蛋白复合物。PTEX就像三峡大坝的升降机,若没有它,这些效应蛋白就会被困在液泡中不能实现其自身的功能。但是迄今为止,科学家们并不知道PTEX如何参与将这些蛋白运输到红细胞中,这也是本文作者要阐明的问题。
借助于原子级别高分辨的冷冻电镜(cryo - EM),研究人员观察了从这些疟原虫中提取出的PTEX,并在零下190摄氏度快速将它冻结,以此保存冷冻瞬间蛋白的结构。通过对PTEX结构的解析,发现该蛋白由三种蛋白组成,他们分别是HSP101和另外两种新奇的蛋白 PTEX150 和 EXP2。三种不同蛋白之间承当着不同的功能。
PTEX的结构:
解析结构探真知
HSP101是第一个蛋白,它主要负责对效应蛋白进行解折叠和引导肽链进入后面两个蛋白的通道中。位于中间的蛋白(PTEX150)就像是一个适配器,将HSP101蛋白连接到最后的一个跨膜蛋白(EXP2)上。
三种蛋白按照6:7:7的化学计量比组成各自对应的复合体,再构成PTEX。研究人员主要研究了负载态(Engaged state)和复位态(Resetting state)PTEX的结构,发现蛋白宽度从170 埃米变为180 埃米,长度从195 埃米变窄为175 埃米,表现出明显的伸缩运动规律。

图4. b,c对应冷冻电镜图;d,e对应蛋白质大小测量图
对PTEX蛋白中间孔洞直径的研究发现,无论是负载态(Engaged state)和复位态(Resetting state),第二(PTEX150),第三个(EXP2)蛋白复合体的直径没有明显变化,只有第一个结构蛋白(HSP101)复合体对应位置的孔洞直径变化明显。

图5. PTEX中间孔洞直径的研究
以上的结构解析可以说明,HSP101蛋白复合体在PTEX运输效应蛋白过程中起着引擎的作用,通过PTEX的伸缩,配合着HSP101结构体中孔直径的缩小变大,把效应蛋白的肽链从PTEX的中孔中运输出去。
“眼见为实”抓证据
以上对于PTEX蛋白功能的推测都是基于结构的基础上得出来的,如果能够观察到PTEX正在转运某一个效应蛋白,这种现场目击的效果将会更有说服力。

图6. HSP101六聚体内的效应蛋白肽链
图6中的a 和b分别是HSP101单体蛋白在负载态(Engaged state)的一维和二维结构。c是HSP101单体蛋白在负载态(Engaged state)是的冷冻电镜解析图,c左边和右边分别是整个蛋白的切分,NBD1和NBD2环用浅色(NBD1)和深色(NBD2)的蓝色梯度着色,以强调六边形的右手螺旋形状。一分为二的图显示NBD2孔隙环的原体密度,其中ATPγS用洋红色表示和载运蛋白的密度用浅粉色表示。
图d是HSP101 NBD2孔隙环原子模型的放大图和展开载运蛋白多肽链的显示密度。NBD2孔隙环用c表示,用原体(protomer)标记(例如,D2PL,P1为NBD2孔隙环,protomer 1)。D2PL、P1 D2PL、P6孔隙环酪氨酸单元的垂直距离分别为6.52 埃米、6.28 埃米、6.38 埃米、6.96 埃米和6.12 埃米。这些精细结构的解析,同时还能够捕捉到载运蛋白在HSP101六聚体中存在的证据。对下一步整体理解有着重要意义。
作者研究表明,PTEX蛋白的HSP101六聚体中NBD2孔环形成两个“手”,它们共同作用以使载运蛋白多肽穿过中心孔。来自HSP101原体1-3的NBD2环形成被动手,最靠近PTEX150(S668-D823)-EXP2像一个漏斗,其保持固定在状态。来自HSP101原体4-6的NBD2环形成活性手,其沿着通道轴(在被动手上方)移动,抓住展开的肽并通过被动手喂食。

图7. PTEX运输整个蛋白过程示意图
在负载状态下(Engaged state)状态下,所有六个NBD2孔环都抓住螺旋楼梯形成中的未折叠肽。当HSP101六聚体塌陷到复位状态(Resetting state)时,活性指针向下移动,通过被动手将新展开的肽进入下方的PTEX150(S668-D823)-EXP2漏斗。然后被动手抓住未折叠的肽,防止其向后滑向HSP101顶端入口,同时主动手向外摆动,释放载运蛋白多肽。最后,活动的手向上移动以进一步向上游抓住展开的蛋白质,转变回接合状态。这种循环进料机制使未折叠的载运蛋白多肽穿过易位子,穿过PVM并进入宿主细胞的胞质溶胶中。
随着人们对疟疾发病机理的持续性认识,本文的研究结果可能有助于开发靶向PTEX的新药,以此来阻止它正常地发挥功能,达到抑制和杀死疟原虫的效果。
https://en.wikipedia.org/wiki/Malaria
https://zhuanlan.zhihu.com/p/21252386
https://www.youtube.com/watch?v=2O3YrdUZQ5U
https://www.nature.com/articles/s41586-018-0469-4
( doi:10.1038/s41586-018-0469-4)
友情提示:点击下面“阅读原文”即可转到原文地址查看原文

两江科技评论
精彩回顾
3. 科技快讯丨新型语音智能交互系统——贴在皮肤上的扬声器和麦克风
4. 科技快讯丨癌症无创诊断的新方法——高分辨“超透镜”光学内窥镜
5. 芯片级的单光子量子光源
6. 发现拓扑表面态负折射效应——《自然》刊登武汉大学刘正猷-邱春印团队最新研究成果
8. “超材料前沿研究”一周精选 [2018.7.30-8.5]

编辑:冯元会
审核:颜学俊


免责声明:本文旨在传递更多科研信息及分享,提供志同道合者的交流平台。如涉及侵权,请联系下方邮箱,我们将及时进行修改或删除。转载请注明出处,如原创内容转载需授权,请联系下方微信号。
邮箱:zunzun@imeta-center.com
微信号:Maysun1992



