劲爆消息! 《纳米结构材料》所有章节内容PDF文件均可下载!(点击进入>>)
纳米电催化d带中心效应!
在所有纳米效应中,电子效应是最重要的效应。我们将从电荷转移效应、d带中心理论、电子金属-支撑相互作用(EMSI)和轨道势理论四个方面讨论电子效应(详见图1)。

图1 (A-C)电荷转移效应,(D和E) D波段中心理论,(F和G-I)电子金属-支撑相互作用(EMSI), (J-L)轨道势理论。
1 电荷转移效应
电荷转移效应又称电子增益和电子损失效应,是基于不同组分之间的界面电荷转移,实现电荷密度的定向调节或特定的电子泵功能,最终实现对反应物在催化剂上的吸附和活化机理的调节。纳米材料的物理和化学性质在很大程度上取决于其电子结构。当纳米材料的尺寸缩小到亚纳米尺度时,材料的电子结构将发生显著变化,具有较强的尺寸依赖性。纳米材料的整体电子性质是由所有原子轨道的叠加得到的。配体和溶剂在表面的配位或吸附也会对纳米材料的电子结构和性能产生重大影响。对于负载型催化剂,由于活性位点和底物之间的费米能(Ef)水平的差异,电子转移发生在界面原子附近,这对催化性能有显著影响。
抑制铂(Pt)在电化学能量转换中的溶解仍然是提高铂基催化剂长期稳定性的主要挑战。近期,中科院学者通过调整表面Pt原子的电子结构,减弱Pt- o偶极子,成功抑制了Pt纳米颗粒的溶解(详见图1 A-C)。石墨氮掺杂碳纳米片锚定的Pt纳米粒子氮含量和石墨化程度平衡,缺陷少,可以显著增强金属与载流子之间的电子相互作用。界面结构可以加速Pt向基体的电子转移,降低Pt的表面电子密度,减弱Pt-O相互作用,降低Pt在氧还原反应中的溶解速率,提高催化剂的稳定性。理论模拟表明,表面铂溶解的抑制是由于初始弛豫期间势垒的增强]。最近,新加坡国立大学的研究人员提出利用电荷转移效应构建与CO2匹配的最佳孔隙化学环境,降低金属有机骨架(MOFs)中C2H2的受力,实现CO2/C2H2的高效反吸附分离。一般来说,在化学吸附和多相催化领域中,电荷转移效应可以通过调节电荷密度来有效地调节反应底物的吸附或催化。
2 d带中心理论
在非均相催化反应过程中,化学反应活性受到催化剂的元素组成、化学状态、尺寸和晶体表面结构等多种复杂因素的影响。金属催化剂的性能很难控制,因为很小的结构变化就会引起巨大的性能变化。然而,有一个神奇的理论,即d带中心理论,认为研究单个变量就可以有效地判断金属催化剂的活性。
催化中吸附的本质是分子(吸附剂)与金属催化剂表面之间形成化学键。从能量的角度看,吸附后吸附剂和金属催化剂表面的总能量降低,即化学键形成。具体来说,当被吸附的分子与金属表面相互作用时,会形成新的成键轨道和反键轨道,如果电子填充成键轨道,则系统的总能量会降低。系统能量下降多少(即吸附是否稳定)取决于分裂能,分裂能与两段的重叠积分近似成正比(分子),与两个轨道之间的能量差成反比(分母)。Hammer和Norskov提出的著名的“d带中心理论”就是从这个分母的角度来分析的。当吸附分子靠近金属表面时,吸附分子的轨道会与金属的s轨道和d轨道相互作用,其中吸附分子轨道与金属d轨道的相互作用会导致能级分裂,生成的反键轨道的位置对体系的稳定性非常重要(详见图1 D)。
吸附后,如果反键态高于费米能级,则有利于吸附,因为没有电子填充在高能轨道上。如果产生的反键状态低于费米能级,就不利于吸附,因为高能量轨道被电子填满了。根据norskov在1995年的工作,我们可以通过观察新形成的反键态的能级位置来判断金属对分子的吸附是否稳定。考虑到这一点,我们可以从下图(图1 E来自Norskov在2000年的工作)中看到,d波段(浅灰色)的能级越高,新的反键态(深灰色)就越高,使得整个系统更稳定。由于这些反键态高于费米能级(它们是空的),并且随着空反键态数量的增加,键变得越来越强。该模型说明了“弱”和“强”化学吸附的变化。它还说明了催化表面成键的一般原理:如果反键态通过费米能级向上移动(变为空),则会发生强键;而如果成键态通过费米能级向下移动(被填充),则是正确的(详见图1 E)。
金属吸附吸附剂分子时的电子带结构发生变化,吸附剂的价态与金属 s 态发生耦合,然后转向金属 d 态进行耦合,吸附剂与金属 d 态的相互作用导致 d 态分离为成键态和反成键态。

金属与吸附剂分子相互作用时会形成结合态和反d结合态。吸附剂与充满的成键态和未充满的反成键态的结合将得到加强,而反成键态的占据只与它们相对于费米级的位置有关。
在拉伸应变情况下,晶格参数较小的金属原子被插入晶格中,或作为覆盖层沉积在晶格参数较大的金属表面。对于 d 带超过一半的过渡金属(本例中为 Ni),其 d 带中心会相对于费米级发生上移,以保持固定的 d 占有率。随着 d 带中心的上移,反键 d 态将上移,同时占据率下降,从而导致与反应中间产物的吸附相互作用增强。同样,对于沉积在铜表面或插入铜晶格的铂原子,收缩的铂晶格也会导致其 d 带宽的增加。d 带中心的相应下移削弱了对反应中间产物的吸附强度。
【1】d带中心最新案例分析
【1】最近,山东大学冯金奎教授通过d带中心调控与空间限域设计的协同作用,有效抑制了多硫化物的穿梭效应,实现了对多硫化物转化的高效催化。通过自组装与原位硒化策略,在三维MXene空心微球上原位构筑了Ni掺杂的CoSe2纳米颗粒。该中空结构不仅提供了空间限制,作为物理屏障能够有效减缓多硫化物的穿梭效应。此外,中空结构的设计防止了MXene的自堆积效应,最大限度地暴露了Ni掺杂的CoSe2纳米颗粒,提供了额外的活性位点并增强了其对多硫化物的吸附能力。电化学测试、理论计算和原位XRD等多种表征表明复合材料展现出优异的多硫化物吸附能力和催化活性。这一研究为空间限域结构设计与电子态调控协同效应开发高性能锂硫电池提供了一种具有潜在应用价值的创新路径。掺杂工程进一步通过调控电子态,将活性位点的d带中心上移,促进了过渡金属位点与多硫化物之间的杂化作用,加速了多硫化物的转化动力学。

图1. 样品的实验合成步骤和限域催化机理示意图
https://doi.org/10.1002/adfm.202416997
【2】金属中的应变工程已被证实能够显著影响d带中心位置,从而改变表面吸附质的相互作用,这对于优化电催化活性具有重要意义。 应变效应的优化:有序排列的SFs产生了以压缩应变为主的拉伸-压缩应变对,优化了d带中心位置,减弱了Ru位点的晶体场分裂效应,增强了电子转移能力,从而提高了OER活性。

图1展示了通过快速冷却法合成富含堆叠层错(SFs)的Ru纳米催化剂(SF-Ru)的过程,与通过慢速冷却法合成的无SFs纳米粒子形成对比。图1a顶部展示了快速冷却的合成路径,而底部则展示了慢速冷却的路径。图1b中的红外图像和温度-时间曲线展示了在氩气和液氮中Ru的温度变化情况。图1c展示了在hcp-Ru中从‘AB’排列到‘ABC’排列的堆叠层错区域的结构,以及在拉伸和压缩应变下d带中心变化的示意图。图1d和e分别展示了SF-Ru和Ar-Ru的高分辨率透射电子显微镜(HRTEM)图像和相应的选区电子衍射(SAED)模式。这些图像和模式揭示了SFs的存在,这些缺陷通过改变原子间距引入了拉伸或压缩应变,显著影响了Ru的电子结构。这些结果表明,通过非平衡合成策略,可以在Ru纳米粒子中引入丰富的SFs,从而优化其电催化性能。

https://doi.org/10.1016/j.apcatb.2022.121682
【3】系统的实验和理论计算表明,核壳结构异质结和单原子掺杂的协同作用可以驱动d带中心位置偏移,促进Ni3S2和Fe-SACs之间的电子重新分布,优化水分子的吸附和中间产物的吸附。因此,作为双功能催化剂,所获得的Ni3S2@Fe-N/S-C/NF展现出了卓越的电催化性能,为电催化纳米原子催化剂的合理设计提供了新的机会,这些催化剂可以应用于广泛的能源转换领域。

图1:通过密度泛函理论(DFT)计算,展示了Ni3S2@Fe-N/S-C的电子态、过渡态和吸附自由能,以及吸附H在不同位点的吉布斯自由能图和OER的吉布斯自由能图。
https://doi.org/10.1002/smll.202409542
【4】本文提出了一种基于单碘原子掺杂的策略,通过精确调控镍基催化剂的d带中心,显著提升了碱性析氢反应的性能。I−Ni@C催化剂不仅在低过电位下展现了优异的催化活性,还在长时间稳定性测试中表现出超群的稳定性。这一研究为镍基电催化剂的设计提供了新的思路,并为未来碱性析氢反应催化剂的开发提供了理论与实验依据。
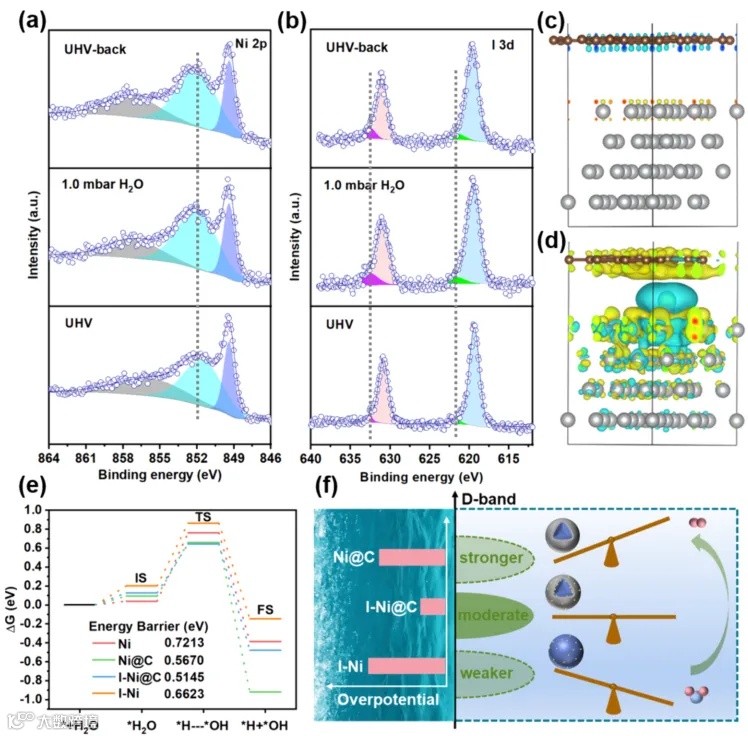
图4:I−Ni@C的自由能变化与HER反应机制分析密度泛函理论(DFT)计算表明,I−Ni@C的d带中心位于较适中的能级,有利于平衡HER反应中间体的吸附和解吸。此外,I−Ni@C的电荷密度差分图显示,碘原子在镍与碳壳之间起到了“桥梁”作用,增强了电子相互作用,从而促进了水分子的解离,降低了反应能垒。
https://doi.org/10.1021/jacs.4c07607
【5】调控Fe 3d-Ce 4f轨道耦合,优化异质纳米粒子Fe位点d带中心,提升电催化氧还原效率!文章通过深入研究Fe 3d-Ce 4f轨道耦合对Fe 3O4/CeO2异质纳米粒子中Fe位点d带中心的影响,成功制备了具有高效ORR电催化性能的纳米粒子,为新型能源设备的商业化发展提供了有力支持。通过工程化Fe 3d-Ce 4f轨道耦合来优化Fe 3O4/CeO2异质纳米粒子中Fe位点的d带中心。采用实验和理论计算相结合的方法,深入分析轨道耦合对电催化性能的影响。

图5 DFT计算。(a)Fe3O4(440)模型,(b)CeO2(220)模型,(c)Fe3O4/CeO2异质结中的电荷密度差,(d)Fe3O4的DOS,(e)CeO2的DOS,(f)Fe物种中d带中心变化对改变含O中间体强度影响示意图,(g)Fe3O4和Fe3O4/CeO2的ORR自由能图。
https://doi.org/10.26599/NR.2025.94907016.
【6】研究表明,Co的掺入导致Pt的d-电子构型的改变,有效地增强了Co在CO2还原反应中的解吸,同时抑制了进一步还原到C,该研究代表了实用高能效Li-CO2电池的实质性进展。该研究成功控制反应路径,并在非质子Li-CO2电池中实现了CO的选择性生成。具体来说,Co原子被掺入到立方Pt中,使Pt的配位数从12改变到11.3,并产生显著的晶格压缩应变。实验结果和DFT计算模拟均表明,CoPt合金内部Co和Pt原子之间存在明显的电子转移,导致Pt的d带中心从-2.17 eV转移到-2.47 eV。

https://doi.org/10.1002/anie.202415728
【7】通常,当Fe单原子的局域电子结构被调整时,可以利用多个参数(电荷转移、d波段填充程度和自旋态)来表征电子结构的改变。由于各种元素之间存在电负性差异,中心Fe原子周围的电荷分布会受到局部配位环境的影响。此外,由于含氧中间体与活性Fe中心之间的强相互作用,调节Fe基SACs与关键反应中间体之间的电荷转移有利于促进中间体的吸附/解吸。此外,中心Fe原子的d-band电子结构可以用几个特定的描述符(d带中心、宽度或相对于费米能级的位置)来表述,这决定了含氧中间体的吸附亲和力。自旋极化最近作为关联催化剂电子结构和电催化性能的一个因素而广受关注。由于配位构型不同,Fe3+可以具有三种电子自旋态,即低自旋(L.S.)、中自旋(M.S.)和高自旋(H.S.)。单原子Fe的中等自旋态具有适中的eg轨道填充,有望成为优良的双功能氧电催化剂。

图2. 描述Fe单原子电子结构的参数:(a)由于电负性差异导致的电荷转移;(b)调整后的d带电子结构;(c)定制的自旋状态。
[8] d带中心理论——发展历程及基本理论
1990年代,Hammer和Nørskov首次利用d带理论建立了过渡金属的电子结构与催化活性之间的关系d带理论。如图1a所示,吸附物在过渡金属表面吸附后,其价态先与过渡金属的s态耦合然后变宽并向下移动,之后继续与d态相互作用形成一个填充的成键轨道与部分填充的反键轨道。反键轨道的填充情况由它与费米能级EF的相对距离决定:d态相对于EF的能量越高,反键轨道的能量越高,键合就越强,反之则越弱。
因此需要电催化剂的最佳Ed能级以实现OER活性最大化。其中掺杂过渡金属基化合物是影响d态的最有效途径,例如将Cu掺杂到RuO₂晶格中会使d带中心远离费米能级EF,导致反键轨道能量降低,Ru-O键强度相应减弱(图1b)。相反,Ni 2p的低Ed能级(即弱吸附能)使含氧中间体难以吸附在表面上。再比如Chen 和同事发现,Fe掺杂可以提高Ed能级更接近EF(图 1c),从而提升反键能态并加强吸附物与催化剂表面之间的相互作用,从而增强吸附能力OER过程中的中间体。值得注意的是,我们还可以通过改变Fe浓度,从而改变d带中心的能态获得位于火山顶的良好OER 性能的催化剂(图1d)。

【2】电化学催化-Sabatier原理
Sabatier原理是催化科学中的一个重要概念,由法国化学家Paul Sabatier在20世纪初提出。该原理强调催化剂表面活性位点的适当吸附能力,以确保反应物能在其上吸附并发生反应,同时产物也能从其上解离。以下是Sabatier原理的核心要点:
Sabatier原理不仅为催化反应机理的研究提供了重要的指导思想,而且对于设计和开发高效的催化剂具有实际的应用价值。
从 Sabatier 原理到过渡金属多相催化的预测理论
科泰催化 容容 科泰催化 2023年02月25日 08:30

https://doi.org/10.1016/j.jcat.2014.12.033
DOI:10.1016/j.jcat.2014.12.033
20世纪中后叶,科学家们在Sabatier原理的定量描述上做了很多发展,如Ronald Percy Bell, Meredith Gwynne Evans,和 Michael Polanyi 建立的BEP relation;Balandin提出Sabatier-Balandin volcano 模型等等。(因为我不是做理论电催化出身,涉及理论计算这部分的理解能力有限,欢迎专业人士来稿补充。)
一直到到20世纪末和21 世纪,随着 BEP relationship, adsorption‐energy scaling relation 和d‐band theory的发展,理论指导实践才开始流行起来。
这篇文章为我们理解从 Sabatier 原理到过渡金属多相催化的预测提供理论指导,介绍Sabatier原理为我们思考最佳催化剂提供了一个概念框架,但作为多相催化理论,它的主要缺点是它不是定量的。目前尚不清楚应使用哪个量来表征相关中间体与催化剂之间的“键合强度”,或者“键合强度”的什么值对应于最佳催化剂。由于这些原因,Sabatier 原理不能用作催化剂设计规则的基础。

计算电子结构方法能够先验地识别给定催化反应的良好描述符,并且可以绘制出描述符空间的最佳区域以帮助发现新催化剂的线索。
文章从以下三个方面引导出Sabatier定量过程:
1. 量化键合强度
催化反应是由表面介导,而非本体结构,以合成氨为例,用DFT构建出的表面金属位点氮物种吸附能比起氧化物生成能更具有火山型关系

2. 降低变量/维度,引入比例关系
构建出活性中间体之间的线性比例关系,将多个反应步骤简化为单个或少个变量,来作为整个反应的描述符,构建火山图,预测催化剂。尤其是像CO加氢这种多个基元反应和变量的,非常需要降低复杂性。因为表面的键合是通过 C 和 O 原子发生的,使用比例关系的概念,问题的有效维数因此减少到只有 2,从而更易于优化和理解。
3. 构建活性图,理解催化活性和选择性趋势
构建催化活性与描述符的线性关系,预测性能和选择性趋势。
将计算方法与测量结果进行基准测试是建立此类程序的一个非常重要的部分,与之很好匹配的是理论计算电子结构因子:d-band center 理论,和实验X-射线光谱测量。
以合成氨为例,描述了金属表面电子结构参数的函数:氮吸附能ΔE N和过渡态能量ΔE N–N,投射到吸附物键合的表面原子上的金属d带的上带边缘。d-带模型与杂交能量相关,原因是相互作用强度与金属d态和吸附物价态之间形成的反键态的填充有关。d态相对于费米能量最高占据态的能量越高,反键态的能量越高,它们越空,相互作用越强。该图片已通过直接光谱测量得到证实。

图为氮吸附能 (a) 和 N2过渡态势能 (b) 作为金属表面原子状态密度d的上带边缘的函数。 (a) 中的插图显示了吸附在 Cu 和 Ni 的 (1 1 1)表面上的 N 的实验 X 射线吸收和发射光谱, 分别测量填充(由阴影区域表示)和空 N 诱导状态。可以清楚地看到从 Cu 到 Ni 时反键合 N-2 p /metal-3 d状态的排空,这解释了为什么 Ni 与 N 的结合要强得多。
不同中间体的过渡态和吸附能都以类似的方式依赖于表面电子结构。不同的吸附状态与表面d电子杂化形成键合和反键合状态。相互作用的强度主要取决于反键合状态的填充程度,而反键合状态又取决于 d 的位置相对于费米能级的状态。
4. 最后总结出催化剂设计策略:
i. 限制关系提供的给定反应的表征催化剂系统的参数数量的减少允许识别一些描述符并使人们能够识别最佳值。
ii. 一系列可能催化剂的描述符值的计算(或测量)可用于筛选新催化剂。
iii. 给定比例关系,找到一个好的催化剂变成了确定不同竞争因素(例如,N2解离和NH3之间的最佳折衷)的问题解析)。
iv. 规避比例关系,即找到稳定中间体或过渡态之一的吸附状态而不稳定其他状态的方法:找到更低比例关系的活性位点基序、添加促进剂、设计具有三维特征的活性位点图案,可以区分各种中间体和过渡态结构。
【3】细说电化学催化理论基础
马震 氢眼所见 2024年05月20日
催化理论是理解和开发好的电极的基础,下面针对一些催化的基本理论做简单科普。
1、多相(或异相)催化

对于这类反应,A和B必须处于相同的状态。这不是本文中电解槽的情况,因此不再进一步讨论。
多相催化是通过提供反应位点来催化特定反应的过程。对于正在催化化学反应的金属制成的催化剂,金属充当的是位点(场)而不是反应物。对于相同的A2⇒2A反应,用下式(2)表达:

式(2)
其中:S*表示特定反应的表面活性位点,不含吸附物。
为了说明任何双原子分子的分子轨道,不妨考虑一下氢原子。当任何一个氢原子与另一个氢原子密切接触时,描述原子电子的波函数就会重叠,这就是通常所说的结合。这种相互作用将导致杂化并产生两个分子轨道。
一个能量较低,叫做分子成键结合轨道。还有一个能量更高的分子轨道叫做分子反键轨道。对于氢分子,每个氢原子贡献一个电子,这意味着当这两个原子成键时,它们会完全填满成键轨道,由于 Pauli 排他性,两个电子,一个自旋向上,一个自旋向下。这就解释了为什么没有“He2”分子,因为成键轨道和反键轨道都被填满了,原子相互排斥。对于不相同的原子结合也可以这样做。图1(b)说明了这一点。

鉴于原子的不相同性质,每个原子的起始能级都不在同一点上,同样,成键轨道必须低于两个起始能级。考虑到原子的不可描述性,成键轨道和反轨道可能杂化成几个不同的轨道,但在这个抽象的层面上,这是一个无差别的区分。
从单个分子到宏观结构,成键轨道和反成键轨道的可量化能级相互融合。在原子数量无穷大的情况下,离散的能级会走向能级带的极限。与其说是特定轨道的占有率,不如说是电子的状态密度(DOS)更方便。这些能带的能量和位置分布最终决定了催化剂与任何吸附剂之间的相互作用,因此有必要花一些时间讨论其中的两个能带。
对于过渡金属来说,有两个轨道带是我们最感兴趣的,即杂化(sphybridized)带和 d 带。由于本论文的大部分篇幅都在探讨由过渡金属和过渡金属合金制成的催化剂,这自然是一个研究重点。
过渡金属的 sp 带涉及与晶格中其他金属原子的结合。因此,这些电子并不局限于特定的原子核心,因此它们形成了一个能量分布非常广泛的能带。

考虑特定周期过渡金属从左到右的电子结构变化。为简单起见,考虑第四周期的过渡金属,当从 Sc 到 Zn 时,越往右移,d 带的填充就越多。对于图3.3的说明,这意味着具有最高能量的电子能级,称为费米能级,正在向d带的顶部移动。周期系的第五和第六周期也体现了这一趋势。
1.3吸附物与金属表面的相互作用
 的能级上。假设这个原子可以吸附到一个金属表面,这意味着在吸附过程中能级
的能级上。假设这个原子可以吸附到一个金属表面,这意味着在吸附过程中能级 会下降,能带会变宽,原因在前面已经解释过了。
会下降,能带会变宽,原因在前面已经解释过了。

通过更多的数学和量子物理推导出吸附质与d带电子相互作用和杂化所产生的键能可以用下式(3)表示为:

式(3)
 是d波段的能量中心,如前所述
是d波段的能量中心,如前所述 是吸附电子的最高能级。
是吸附电子的最高能级。
在考虑反应性的趋势时,有必要观察Ed-hyb 在特定周期内和周期之间的变化情况。
由上式可知,当 0< f <1 时,第一项为吸引力项,这意味着它能促进成键;第二项为排斥力项,这意味着它能阻碍成键。在一个周期内从左到右移动意味着从低 f 到高 f,当 f 增大时,上式(3)中的吸引力项下降,而排斥力项增长。
从元素周期表的一个周期向下移动,原子核变大,这意味着局部电子轨道会减少,这意味着吸附态和金属态之间的重叠会增加,从而导致两个项的绝对值都增加。
这两种趋势回答了一个合理的问题:为什么金是最惰性的过渡金属?金处于一个具有完整 d 壳的周期的末端,这意味着高 f;金处于最高周期,这意味着更大的β。
这些倾向导致单原子金属表面对特定反应可能过于活泼,或者对特定反应过于惰性,从而达到最佳状态。这些信息通常以火山图的形式呈现。示例见下图4:

图4:过渡金属对氧还原的活性与氧吸附物结合能的关系。
从上图4 中的数据可以看出,氧气还原的最佳单原子金属表面是铂(Pt),这也许不足为奇,但有趣的是,催化理论表明,与最佳表面相比,铂的反应性稍高。上图4中的数据表明,最佳点为 ∆EO = 1.7eV,而在∆EO ≈ 1.6eV 时,铂表面的结合力稍强。

图5:表面的电子结构示意图,以及在另一种晶格常数较大的金属上沉积一个伪晶覆盖层时发生的变化。
类似的论点也可用于催化剂颗粒的边缘位置。这些边缘位点在两个不同的晶体面相交点和较低的布拉格指数面处更为普遍。这些平面碰撞和低布拉格指数平面在较小尺寸的粒子中相对更多。这是首选纳米级催化剂的两个原因之一,另一个原因是表面与体积比趋于∝1/R。这与多相催化有关,因为根据定义,相关反应必须在催化剂表面进行。
https://mp.weixin.qq.com/s/fdmzVMak-cM9ROeYg6sodA
【4】理论指导电催化过程——综述推荐
科泰催化 容容 科泰催化 2023-02-21 08:30 广东
今天给大家推荐一篇综述,入门级电催化基础知识,语言清晰明了,内容详尽,非常适合电催化小白。

理论指导电催化过程:从机理分析到结构设计。通讯作者是吉林大学邹晓新教授。
在这篇综述中,作者先是总结了电催化剂设计中常用的催化理论的一些基本方面(如Sabatier原理、d带理论、吸附-能量标度关系、活性描述符)及其相关性。
这篇综述基本是一个理论电催化的发展史,几乎涵盖了催化理论的基本方面,由Sabatier原理到volcan-shaped plot模型,再到过去10~20年间发展的BEP relationship、adsorption-energy scaling relation、d-band center theory等等,理论指导实践才开始成熟起来,引入描述符:ΔG、d-band center、eg filling、p-band center、unsaturated coordination number 等等,建立起电子结构—表面吸附能—催化活性的内在关系。
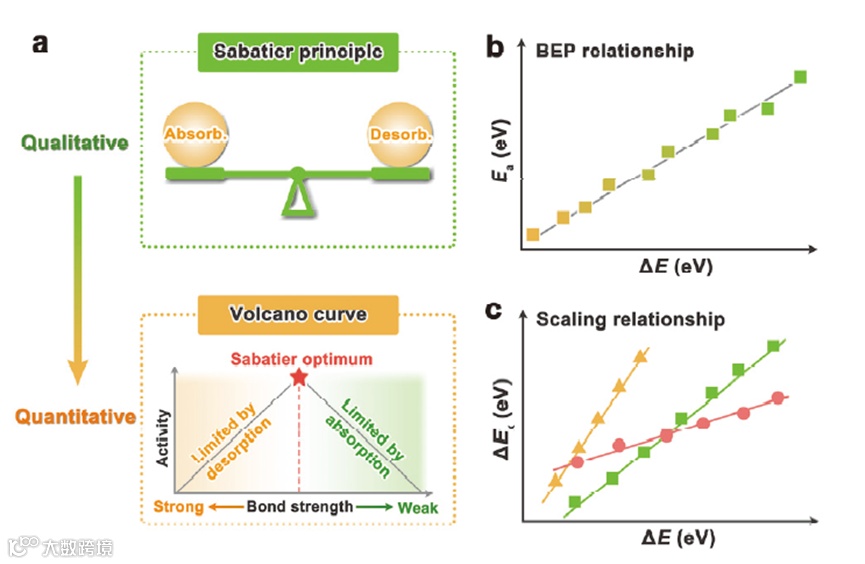
(a)萨巴蒂尔原理从定性到定量分析的示意图。(b)显示活化能与反应能之间线性关系的BEP图。(c)不同中间体之间的比例关系。

(a)过渡金属表面的s/d态与吸附质价态之间化学键形成的示意图。应变效应(b)和配体效应(c)对催化剂d带中心的影响。

用于反映催化活性的主要描述符示意图。
然后,简要介绍了HER、OER、ORR、CO2RR和NRR电催化剂的基本机制和面临的主要挑战,并重点介绍了用于解决这些电催化过程面临的挑战的基于理论的努力。
可以说非常深入而且全面了,尤其对还未确定研究方向的,是很好的理论入门指导。
最后,提出了理论驱动电催化在未来的主要挑战和机遇。
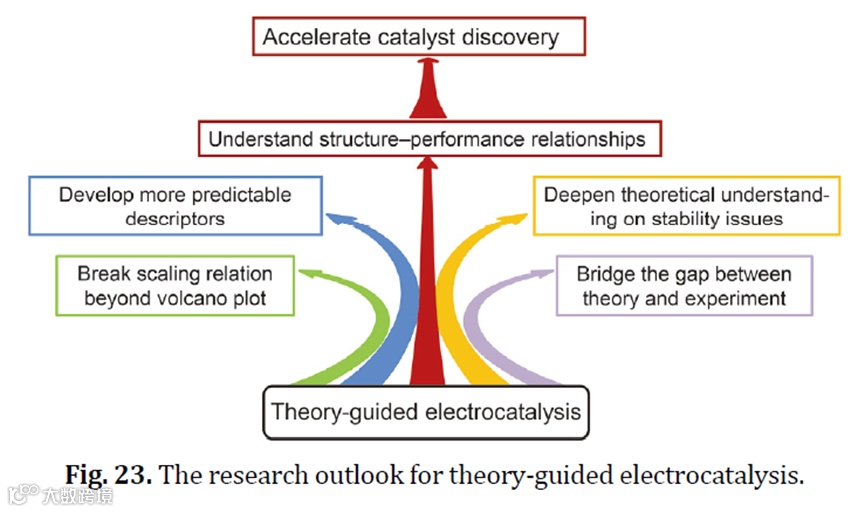
这些催化理论知识对于帮助我们理解催化机制、解释催化现象、构建自己的知识架构非常关键。建议电催化入门的小伙伴认真研读。
我后面也会出一期系统的电催化理论知识串联汇总,但我只能做个引路人,路还是要自己一步步走的。加油!
【5】电催化理论知识(入门级)
科泰催化 2023年02月23日 08:30 广东
电催化理论知识对于帮助我们理解催化机制、解释催化现象、构建自己的知识架构非常关键。

(电催化理论知识入门框架,B站“科泰催化-容容”有视频讲解)
我将电催化理论知识方面的内容分成了10个要点, 1. Sabatier原理 2. 火山图曲线 3. 线性标度关系 4. d-带中心理论 5. 金属不饱和配位 6. eg轨道填充7. 金属-氧共价 8. p-带中心理论9. 反应路径AEM对比LOM 10. 质子耦合电子转移和非质子耦合电子转移理论。结合者这几篇比较好的电催化机理综述来看,会更有效果。
1. Theory-guided electrocatalyst engineering: From mechanism analysis to structural design. Chin. J. Catal. 2022, 43, 2987-3018.
2. A review on fundamentals for designing oxygen evolution electrocatalysts. Chem. Soc. Rev. 2020, 49, 2196-2214.
3. Main Descriptors to Correlate Structures with the Performances of Electrocatalysts. Angew Chem Int Ed Engl 2022, 61, e202111026.

第一个Sabatier原理,它的起源是研究有机分子在金属上直接加氢,后来发现这个规律:还原金属作催化反应剂,过强、过弱的吸附都不利于反应发生,奠定了有机无机催化的理论基础。但它的缺点是它不是定量的,这意味着缺乏预测能力,无法通过实验对其进行测试。
为了定量描述这一原理,后人发展了一系列理论,与物理量建立起定量关系,引入一系列描述符如生成焓、活化能、表面能、中间体吸附能等等,比如这张合成氨不同金属N吸附能与反应活性的关系。

关于火山图的分析,如OER过程涉及到复杂的多电子质子转移步骤,有多个中间体,所以这部分会着重帮大家理解OER的这种二维火山和三维火山怎么去分析。
像这种多个中间体的火山图的构建,涉及到中间体吸附能之间的线性标度关系,这种关系是固有的,比如OER,催化剂表面与吸附氧物种之间都以金属-氧键相连,这些中间体的吸附能满足一种线性关系,这种限制关系,使我们可以以某个中间体为变量,构建火山趋势,帮助我们简化计算过程,尤其是像CO加氢这种多个基元反应和变量的,尤其需要降低复杂性。再根据中间体吸附能和线性关系,算出每一步反应能垒,画出能量台阶图,找出决速步,验证实验结果、指导性能优化。

但线性标度关系的这个特性,使它具有局限性。我们知道电催化OER的理论电极电势1.23 V,但由于线性比例关系,ΔG*OOH-ΔG*OH这两步的电势差为3.2 V,这就使得理论最低电势是每一步能差均分1.6 V,减去理论电势,理论最低过电位370 mV。想要进一步提升是很难的,后来为破除这个局限性,又发展了一些打破线性标度关系的方法,后面会讲。这就好像,你为了看得更远在门口建了座山,后来发现这座山却挡住出门的路了,现在又需要把这座山移开。

d-带中心理论(d-band center)起源于Norskov提出的d能带占据电子数,发现金属d电子数在NH3和CH4的吸附活性呈现火山图关系。

而后计算不同表面上H2解离能的差别,首次应用了d能带中心作为描述催化活性的自变量。

从分子轨道理论出发,当吸附分子靠近金属表面的时候,吸附分子的轨道会和金属的s和d轨道发生作用导致能级分裂,形成的成建轨道会比原来的轨道能量更低更稳定,而同时形成的反键轨道会比原来能级能量还要高,不稳定。如果电子都填充到成键轨道之上,那么体系的整体能量是下降的。反之,反键轨道电子填充越多,结构越不稳定,中间体键合强度越弱。
根据d带中心相对于费米能级EF的位置和反键轨道填充度来定量分析中间体的吸附强度。生成的反键轨道的位置对体系的稳定性如此重要,所以后来又发展出了eg 轨道填充(eg filling)又叫eg 轨道占有率(eg orbital occupancy)单独作为描述符。
同年,Norskov在nature上发表了非常经典的文章:“为什么金是最贵重的金属?”

分析了过渡金属的d电子结构与吸附能之间的关系。而后,d带中心理论开始发展,拓展到贵金属和过渡金属,成为异相催化/电催化中最出名的“描述符”。现在依然是主流的描述符。

如何能够通过调节d带中心位置来优化其吸附强度呢?从两个方面:
1. 调节d电子数,首先不同金属元素的d电子数不同,通过引入不同元素调节吸附能,其次通过改变价态,氧化还原或者诱导电荷转移的方式,也可以改变活性位点价层d电子数。
2. 调节d-带展宽。当吸附单能级与连续能级相互作用后,其能量会有一定的展宽。而展宽代表金属d轨道与吸附物p轨道的相互作用强度,作用越强,能带越宽。当带宽变窄,费米能级不变,则d-band center一定上升。d-带展宽受周围应力效应和配体效应的影响,通过引入拉伸和压缩应力、或者改变配位数和配位强度,改变d-带展,从而调节d带中心位置,调节吸附能。其中配位数的研究最多,又额外发展出了新的描述符——配位数,这里MCUS写的是不饱和配位金属阳离子。
得知d-带展宽也是影响d带中心理论的重要因素,Norskov将d带中心理论做了完善,引入了d-带展宽作用,整合出用上带边upper band edge作为描述符代替d-band center position来构建反应性火山图。

另外,从态密度分析也可以计算出的能带结构,可以用来分析带隙和材料性质,分析导电性。

配位数引出的金属不饱和配位(MCUS)作为描述符,反映了吸附剂的p轨道与金属原子d轨道的相互作用,这是根据过渡金属不饱和配位度与表面吸附强度的火山图关系,根据过渡金属氧化物所在的吸附强度位置,通过增加或者降低不饱和配位度来调节中间体吸附能,本质是调节d带中心位置和反键轨道填充。调控方法有很多,比如通过部分氧化、还原调节配位,或者左右两边结合,调节MCUS到火山顶点,其实本质还是调节d电子结构,它们都是融会贯通的。

前面说到根据反键轨道填充度发展的eg 轨道填充作为电子描述符,其基本原理还是分子轨道理论,金属d轨道与氧配体作用后,发生裂分,分成三重简并的t2g轨道,和双重简并的eg轨道,根据配位环境和分裂能形成六配位的八面体结构和四配位的四面体结构。

Goodenough和邵阳老师(Yang Shao-Horn)从大量的钙钛矿氧化物ABO3中构建出B位点金属eg轨道填充与反应活性火山图,B位点就是八面体位点,对于八面体配位的金属来说,B位点在xyz轴上的d电子云直接与八面体位点吸附O的2p电子云头碰头交盖最大化形成σ键,分裂能更大,杂化后形成能量更低的t2g成键轨道,和能量更高的eg反键轨道,所以eg轨道的填充度是影响吸附能的主要因素。指出当eg轨道的填充为1时吸附最优,性能最好。eg < 1,造成氧中间体吸附过强,不利于反应物脱附,eg > 1,氧中间体吸附过弱,不利于吸附。

其他的发展比如氧化态调控、自旋态调控和诱导Jahn-Teller效应,除了上面提到的方法之外,还可以引入磁场和手性分子改变电子自旋结构从而消除兼并,调控eg轨道填充。eg轨道填充也有其自身局限性,比如解释不了像LaMnO3、LaCoO3和LaNiO3这些具有相同eg轨道占用率(eg = 1)但OER活性不同的现象,这是因为金属阳离子的eg轨道填充理论是建立在离子模型上,而不能反映金属-氧键共价的情况。

M-O共价与O 2p带有关,反映d-p杂化程度。事实上,当金属-氧共价达到一定程度,金属和氧都能作为催化反应活性位点,氧作为活性位点时,O 2p带最上端参与氧化还原反应,这就发展了邵阳老师等人提出的p-band center p-带中心理论。
根据O 2p带相对金属d带的位置,O 2p带越高,O的反应性越大。当O 2p带高于金属d带上带边时,活性中心由原本的金属转移到O上, 当O 2p带再升高超出费米能级,氧离子得电子自发生成氧气从晶格中逃逸。


p-带中心理论与与d-带中心理论的相同点是:都是电子结构特征描述符,不同点是:p-带中心理论弥补了d-带中心理论上的误差和局限性,对于金属、氧化物用于OER/ORR反应更精确。利用p-带中心理论建立起与活性中间体的关系,确定反应决速步,为理解机理、优化性能提供指导方案。
OER的反应路径:吸附演化机理AEM和晶格氧介导机理LOM。

吸附演化机理比较常用,满足线性限制关系,中间体氧物种在金属表面发生连续的吸附演化过程,LOM机理就是p-带中心理论的发展,与AEM不同的是,它涉及到晶格氧迁移、耦连和氧空位的生成。
它们的区别是:AEM是金属为活性位点,优点是结构稳定、满足scaling relation、便于利用描述符预测、设计催化剂。缺点是受限于scaling relation 理论过电势370mV,性能很难突破。而以氧为活性位点的LOM刚好可以打破这个线性限制,避免了高能垒*OOH的生成,性能可以更好。
LOM根据活性位点涉及氧空位、单个金属、还是双个金属,发展了OVSM、SMSM和DMSM机理,慢慢被大家接受而广泛研究。但LOM致命的缺点是结构不稳定,这是由于它自身的特点晶格氧参与氧析出造成的,由此也可以看出活性和稳定性控制天平的两端,如何平衡这两个点是催化永恒的课题。
目前发展的解决办法比如将高活性的LOM机理与高稳定性的AEM机理相结合,还有拓展新的机理路径比如OPM氧耦合机理,未来还需要很长一段路要走。
打破AEM线性限制关系的方法除了LOM之外,还有比如引入两个或者多个活性位点,增加其独立对中间体吸附的控制,或者引入质子受体增加其脱质子反应过程等等。

与AEM和LOM相对应的就是质子耦合电子转移PCET和非质子耦合电子转移non-PCET。质子耦合电子转移定义顾名思义就是,脱质子与电子转移同时进行,反之则是两者不同时发生。前者发生也就是吸附演化机理,受限制关系约束。后者则质子转移步是限速步,受pH影响,产生pH依赖效应,这个现象在LOM中也可以经由实验验证。
以上就是电催化理论知识框架的内容了,没有涉及到的,后期单独补充。除了理论知识的内容,我会尽可能将实验与理论相结合,比如这个理论用来解释哪种实验现象,证明这个理论需要用到哪些实验方法等等,用实际案例加以分析。
【6】河南大学李秋叶/付现伟JEC综述:实现电催化水分解工业化发展的电催化剂结构设计
JEC 研之成理 2022年03月29日 12:13






文章信息
Structural Design for Electrocatalytic Water Splitting to Realize Industrial-Scale Deployment: Strategies, Advances, and Perspectives
Xianwei Fua,1,*, Ruijuan Shib,1, Shilong Jiaob,*, Mengmeng Lia, Qiuye Lia,*
J. Energy Chem., 2022.
DOI:10.1016/j.jechem.2022.02.010


