


声镊操控技术突破生物系统精密操控瓶颈,为单细胞与组织层级的生物功能干预提供新思路!
由杜克大学牵头,联合哈佛大学医学院、宾夕法尼亚大学、北卡罗来纳州立大学、布里斯托大学等多所研究机构近期发表关于声镊综述文章于国际权威期刊《Nature Reviews Methods Primers》,研究团队系统总结了声镊的基本原理、典型装置结构以及其在精准生物学和医学中的关键应用路径。文章指出,声镊技术凭借声辐射力与声流的耦合效应,可实现对微纳尺度颗粒、细胞、组织乃至模式生物的非接触式精密操控,具备跨尺度、高通量、生物相容性强等显著优势,为相关领域提供了新的实验范式与工程手段。

声镊是一类基于声辐射力与声流运动实现精细操控的非接触式装置。其工作原理依赖声波在传播过程中将动量传递给目标对象,从而在不直接接触样本的情况下对其进行捕获、推动或旋转。声波在液体或固体介质中传播时,与粒子之间产生的作用力由其尺寸、密度、压缩性及所在环境决定。通过调节声波频率、幅度和相位等参数,可灵活构建不同类型的声场结构,实现对目标对象空间运动轨迹的主动调控。根据声场维度与结构的不同,声镊主要分为二维面内系统与三维聚焦系统。二维系统多应用于微流控通道和平面微腔内,其特点是结构紧凑、易于成像、装置集成度高。三维系统则更适合复杂空间内的粒子控制,如对小动物体内的靶向定位,能够实现轴向力与三维轨迹调控,适配组织工程与体内应用场景。

图1. 声镊在精准生物学与医学中的应用。声镊可通过多种声学方式实现操控目标的目的:一方面利用声涡旋束构建局部单点声阱,实现对单个对象的精确操作;另一方面可通过表面驻波或体积驻波形成多点声场阵列,采用一对指叉换能器或体积压电换能器阵列,达到并行操控颗粒或细胞的效果。这些技术支持从纳米至毫米尺度范围内的广泛粒子操控。不同类型的声镊已广泛推动科学研究与医学应用的发展,包括疾病诊断与治疗、单细胞免疫操作、单细胞组装以用于组织工程、模型生物操控以支持生物成像,以及活体组织尺度的体内生物打印等。
在实验平台与系统构建方面,二维声镊通常使用体声波(BAW)或表面声波(SAW)技术。BAW系统以压电换能器为核心,通过交变电场激励换能器本体振动,从而在腔体中形成声场。常用材料包括铌酸锂、压电陶瓷等,器件布置方式有方形、环形或阵列结构,声波在介质中干涉叠加后形成可控的驻波结构。SAW系统则利用指状换能器在压电基底表面激发高频表面波,这些声波在液体中形成漏波(leaky wave)形成面内声场,适用于高分辨率操控。三维聚焦系统的构建相对复杂,通常需要采用声学透镜或多通道换能器阵列以实现声束聚焦与旋转场生成。声透镜通过调控厚度或材料相位差引导声波聚焦,生成集中声压区域;而阵列控制则依赖于对各通道输入信号的幅相调制,可在空间中合成复杂声场图案。此外,近年来兴起的声全息技术通过三维打印或微纳加工手段构建声相位板,能够生成多焦点或自定义三维声场,用于并行操控多个粒子目标。为实现更高的操控精度与系统鲁棒性,一些研究团队引入了逆滤波声场整形方法与时间复用控制技术。这些方法可实时重构所需声场模式,提高操控的灵活性与响应速度,进一步推动声镊向生物过程动态调控方向拓展。

图2. 二维面内声镊。a,方形配置下的二维平面波,其相位可控,在换能器所在的x–y平面中形成类棋盘格的节点排列。b,环形配置下形成固定轴对称声场,声压分布呈第一类零阶Bessel函数形态,节点呈同心圆分布。该结构本身不变形,需通过整体装置的平移来移动声场位置。c,二维环形阵列结构可生成任意形状的声场,并支持动态重构。通过多个一阶Bessel函数的叠加,可在阵列控制下实现双声阱结构。
粒子操控与物理机制
声镊具备强大的操控功能,涵盖四种核心模式:
粒子捕获(trapping)
空间平移(translation)
方向旋转(rotation)
图案重构(reconfiguration)
在典型操作中,目标对象被捕获于声场的节点或反节点处,实现稳定固定;而通过调节激励频率、相位差或器件排列,可以在不改变物理接触的前提下引导粒子沿任意路径移动;引入旋转声场或螺旋相位结构时,粒子可在平面或三维空间中实现自旋或轨道旋转;多通道操控或声场调制还支持图案重构功能,快速实现细胞阵列、组织框架或纳米结构的布局调整。粒子运动过程中的力学响应不仅受声压梯度影响,还可能由声流诱导的流体拖曳作用主导,尤其在近边界或黏性液体中更为显著。因此,实际系统中操控性能高度依赖于粒子尺寸、密度、声场参数及腔体结构。研究表明,不同尺度下声辐射力与斯托克斯力的主导地位存在转化阈值,需依据具体应用进行优化设计。
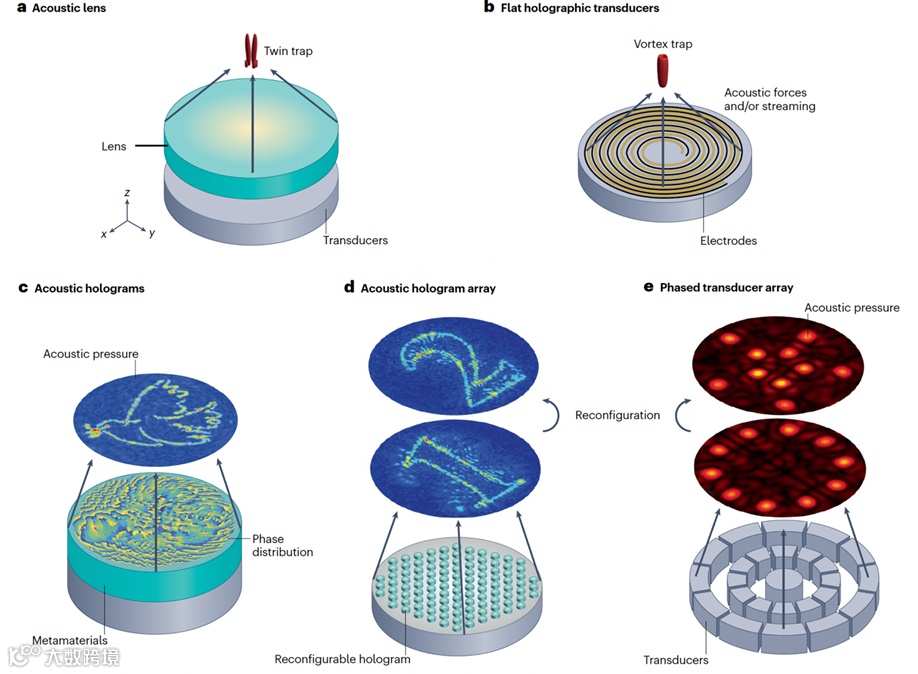
图3. 三维聚焦型声镊。a,最基本的三维声束生成方式由换能器与声学透镜组合构成,透镜可通过多种技术制备,包括超材料设计。b,采用螺旋图案电极构建的三维声镊器件,可形成具有方向性的聚焦声场。c,利用声全息板通过三维波束整形生成静态二维图案,实现场形可控。d,可重构的全息板使声场能够在二维与三维结构间灵活切换,实现动态场调控。e,二维相控阵列可生成并实时操控三维声场。
应用场景与技术拓展
在当前研究框架下,声镊被广泛应用于以下五类代表性场景:
1)单分子力谱学:通过声控微球对连接蛋白、核酸等生物大分子施加控制力,可实现快速、非接触、高通量的力学性质测量,为药物筛选、疾病建模与结构生物学研究提供高效工具;
2)单细胞操作:声镊具备并行操控能力,可同时操作数百个细胞进行阵列排列、精准配对或动态分离,在免疫学、干细胞工程及细胞疗法等方向发挥重要作用;
3)组织工程构建:利用可重构声场将不同类型细胞引导至特定三维位置,实现多细胞异质构建体的自动装配,是类器官、微组织模块快速生成的新策略;
4)模式生物操控:声镊可对秀丽隐杆线虫、斑马鱼等模式生物进行角度调控与姿态调整,有助于实现高分辨率、全方位生物成像与功能分析;
5)体内精密操控:在超声成像引导下,声镊可对活体组织内的微粒子实现毫米级输运与定位,为微创介入、靶向治疗与体内制造等应用提供技术支撑。
这些应用不仅证明声镊在基础研究中的广泛适用性,也展现了其工程应用潜力,特别是在自动化操作、微环境调控及可编程构建等领域中具有独特优势。

图4. 声镊应用示意图。a,在声阱中实现对单个目标的声学捕获。捕获位置依赖于目标的物理属性,如尺寸、密度与可压缩性。插图展示了单个声阱的声场分布及声辐射力的方向。b,同时并行平移多个目标对象。运动路径可通过预设的声场相位图案规划,或通过移动声场实现动态引导。c,对捕获目标进行平面内与垂直平面的旋转操控。通常以声波传播方向所在的x–y面作为参考平面。d,声场结构与目标图案的重构。通过调控声场分布,可实现目标位置的连续可控切换与图案重新排列。

图5. 声镊在典型应用中的实验结果展示。a,声镊可在多种环境中(如微流控芯片、培养皿以及活体血管内)捕获生物成分,包括细胞与细菌。b,声镊可用于对颗粒或细胞对进行平移操控,实现精确控制的成对运动。c,声镊可实现对模型动物如斑马鱼幼体的旋转操作,显著提升三维体积成像质量。右侧小图为体积OCT扫描的选定切片图(l)及其反射信号图像(R)。d,实现对颗粒的三维重构声阱捕获,并可灵活重构声场结构。
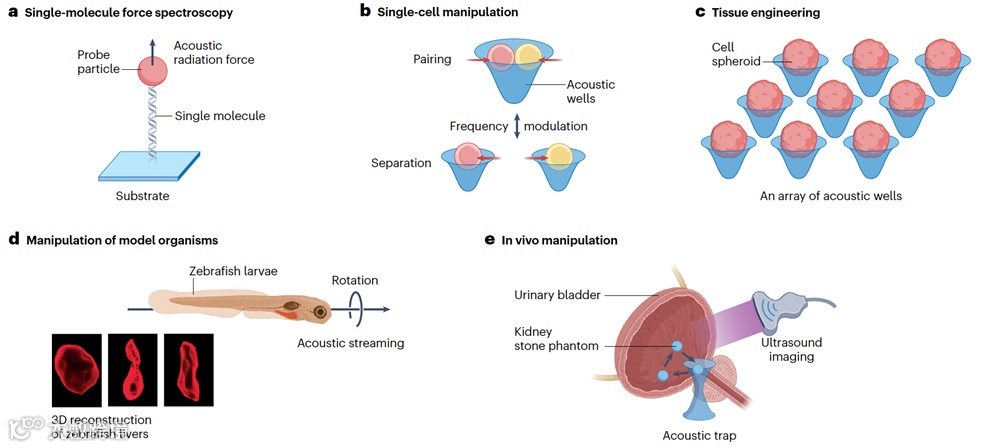
图6. 声镊在精准生物学与医学中的典型应用。a,声镊可用于捕获单个颗粒并牵引单分子,用于开展力谱研究。b,该技术支持细胞对的可逆配对与分离,适用于细胞间相互作用研究。c,声镊可引导单细胞组装成类似组织的结构,为组织工程提供新手段。d,已应用于模型生物如斑马鱼幼体的操控,支持其空间定位与行为干预。e,可在猪膀胱体内实现毫米级颗粒的操控,展示其在活体环境中的应用潜力。
尽管声镊已取得显著进展,其技术推广仍面临若干挑战。首先,现有装置在频率提升与能量聚焦方面仍有瓶颈,高频换能器的集成效率、热损耗控制与器件稳定性需进一步优化。其次,在三维操作系统中,实时成像与反馈调控机制尚不完备,限制了复杂生物过程中的动态干预能力。此外,不同实验平台之间缺乏统一规范,数据复现性与标准化程度亟待提高。
为此,研究团队建议未来从以下几个方向推进:
材料层面,引入透明、低损耗、高耦合效应的新型压电材料;
结构层面,设计可弯曲、微型化、多通道集成的可穿戴声控模块;
算法层面,开发基于深度学习的声场快速重建与实时路径调控模型;
应用层面,探索声镊与光学成像、微流控芯片、生物传感器的融合接口,构建闭环式多模态操控平台。
未来,随着软电子、生物材料及人工智能技术的进一步发展,声镊有望演化为智能化、自适应的生物操作平台,全面服务于精准医疗、个体化治疗与生命科学前沿研究。
综上所述,声镊不仅为实验科学家提供了稳定、高效、可扩展的操作工具,也正逐步成为工程实践与临床诊疗中的核心接口技术之一。
该研究由Shujie Yang (杜克大学、哈佛医学院、宾夕法尼亚大学)等作者完成,通讯作者为Shujie Yang (杜克大学、哈佛医学院、宾夕法尼亚大学), Chuyi Chen(北卡州立大学), Bruce W. Drinkwater(布里斯托大学),Luke P. Lee(哈佛大学医学院)和Tony Jun Huang(杜克大学)。

原文链接:
https://www.nature.com/articles/s43586-025-00415-w



