
国家药监局器审中心关于发布医疗器械可用性工程注册审查指导原则的通告(2024年第13号)
为进一步规范医疗器械可用性的管理,国家药监局器审中心组织制定了《医疗器械可用性工程注册审查指导原则》及其应用说明,现予发布。
特此通告。
附件:1.医疗器械可用性工程注册审查指导原则(下载)
2.关于《医疗器械可用性工程注册审查指导原则》的应用说明(下载)
国家药品监督管理局
医疗器械技术审评中心
2024年3月19日

01
附件内容

附件1:

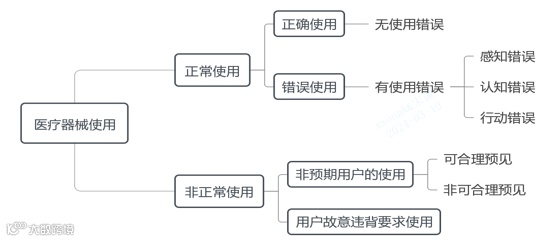

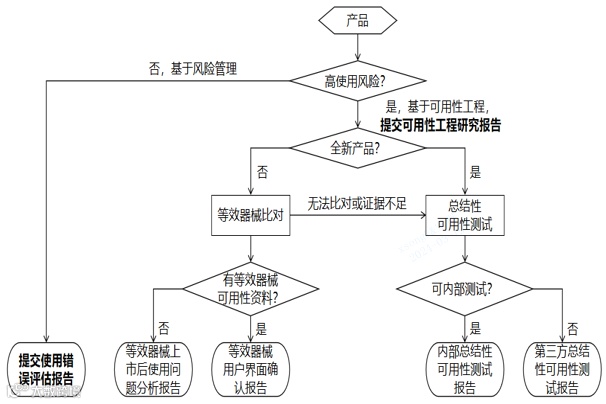
综上,本指导原则基本思路详见图4。
|
|
|
|
|
|
|
|
|
|
|
|
[55] SAC/TC7全国人类工效学标准化技术委员会[OL]. http://std.samr.gov.cn/search/orgDetailView?tcCode=TC7.
其他可用性工程方法详见可用性工程相关标准、书籍等文献资料,本指导原则不再赘述。
02
关于科睿



科睿医疗(care-real)是一家医疗器械合同研究组织(CRO),主要业务为:
●医疗器械全生命周期的临床评价;
●医疗器械多国合规准入全流程策划与一站式服务。
公司专注于医疗器械临床研究与临床评价,包括临床前可行性研究、注册临床研究、研究者发起的临床研究、同品种临床评价、上市后临床研究、真实世界研究。
公司聚焦于大外科、泌外、眼科、皮肤与整形、心内与心外领域,并拥有众多的临床专家资源,以及成功经验。
公司具有完整的临床研究服务组织架构与执行团队、质量管理体系、临床研究数据采集系统,能够满足临床研究与临床评价的全流程服务。


请扫描上方二维码联系我们
— END —

微信公众号

微信小商城


