

CARE-REAL
Clinicaltria登记流程
—知识分享—


欢迎关注我们的公众号!在这里我们将为您带来专业的临床试验相关知识。



01
Clinicaltria
1. 获得PRS账户---责任方注册(申办方、或者经授权的主要研究者)(2个工作日,邮件通知)
(1) 已拥有:提交PRS 管理人联系申请表- ClinicalTrials.gov,收到PRS管理员的联系信息,可以直接联系他们以请求用户登录。
(2) 未获得:
① 申请组织账户:申请 PRS 组织账户 - ClinicalTrials.gov
② 申请个人账户(不太建议,一般在没人担任PRS管理员时):申请PRS个人账户 - ClinicalTrials.gov
2. 收集有关研究的信息,可能包括研究方案、拨款申请、机构审查委员会(IRB)批准表以及任何研究性新药申请(IND)或研究设备豁免(IDE)信息。
3. 登入PRS,ClinicalTrials.gov PRS:登录

4. 在 PRS 主页上,单击“新记录”快速链接或从“记录”下拉菜单中选择“新记录”。

5. 输入研究方案ID、标题、研究类型等。

6. 填写以下模块内容

(1) “Study identification”包括研究方案的唯一识别号、临床研究的题目和研究类型(干预性研究、观察性研究和拓展性应用),这里研究方案的唯一识别号比较重要,要保证它的唯一性,一般我们都用单位的伦理批件号;

(2) “Study status”是指研究当前的试验状态,包括最近一次核对试验方案的时间、研究对象招募的状况、研究预备开始和完成的日期;

(3) “Sponsor/Collaborators”是要填写临床试验的责任方/主办方/合作方的信息;

(4) “Oversight”是豁免信息,如果研究有经FDA批准的临床试用新药申请或器械研究的豁免,就要填写相应的序列号和颁发部门;
(5) “Descriptions”是要对临床研究的基本信息和设计方案进行概括,并且要对研究的假说进行阐述,这部分内容需要填写在Brief Summary里;
(6) “Conditions”指的是研究关注的对象或重点,也就是研究关注的某种疾病或健康状况;

(7) “Study design”是研究设计。如果是干预性研究,就要填写研究目的、研究分几个阶段、干预模型、预备分组数目、盲法和干预措施分组的分配方式等内容。如果是观察性研究,就要填写观察研究的模型、观察时间、研究对象数目等内容;
(8) “Arms and interventions”是研究的分组和干预类型名称;
(9) “Outcome measures”是结局指标和测量方法;
(10) “Eligibility”是研究对象的纳入和排除标准;
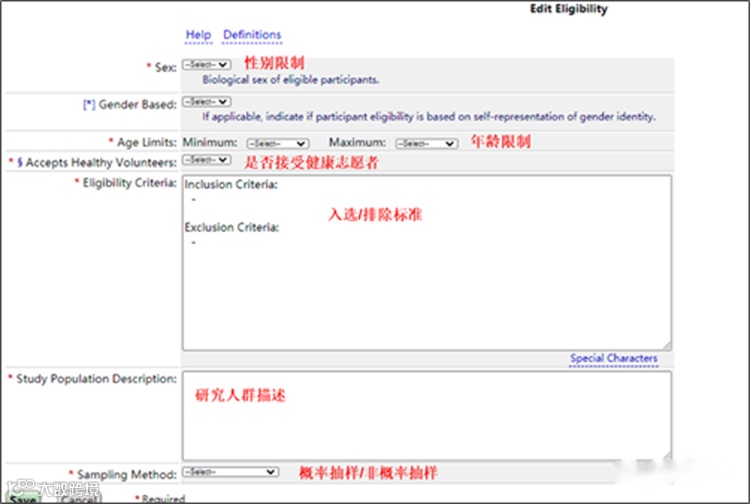
(11) “Contacts/Locations”是研究者的联系方式和通讯地址;
(12) “References”是研究方案的所有参考文献,这一项不是必填的。
网站对每一项内容都给出了具体的定义,网址是clinicaltrials.gov/policy/protocol-definitions,也可以参照别人已经发布的研究填写。
7. 注意查收评阅意见,审核通过后即获得NCT注册号。

02
中国临床试验注册中心
1. 注册账号,填完个人信息注册表即可

2. 点击“新注册项目”,有“*”为必填项,填完注册表点提交(若一次性填不完,可先点保存)

(1) 新项目注册概况:注册题目、研究课题名称等
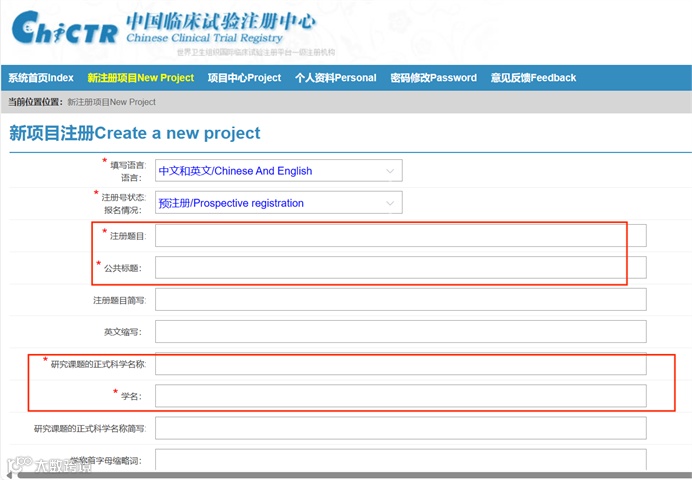
(2) 申请注册人信息:联系人姓名、电话、邮箱、所在单位等
研究负责人信息:联系人姓名、电话、邮箱、通讯地址等

(3) 研究实施负责(组长)单位:名称、单位地址等
试验主办单位:国家、单位、具体地址等

(4) 研究方案:目的、设计、纳排标准、干预措施(组别、样本量、干预措施、样本总量)、测量指标等



(5) 采集人信息:名称、研究对象情况、性别、年龄等

3. 可先注册后补交:均需提交伦理审查批件复印件(伦理审查批件扫描保存为jpg格式,在注册申请表“伦理审查批件”栏中上传,文件大小限制在2M以内。可于注册完成后提交,即先填注册表,获得注册号后研究者再提交伦理委员会审查)
4. 可先注册后补充:均需提交研究计划书全文和受试者知情同意书(模版可在该站“重要文件”栏中下载https://www.chictr.org.cn/file.html)(电子版在注册表中“研究计划书”上传文件中提交)。
5. 注册表中需提供临床试验计划使用的数据收集(CRF)和管理系统信息(EDC),注意:是两种同时具备,不是二选一。

6. 审核完成后,自提交注册表之日起两周内获得注册号。
7. 获得注册号后第二周即可在世界卫生组织国际临床试验注册平台(WHO ICTRP)检索到已注册试验,目前WHO ICTRP每周四更新(假期后延)。

03
关于科睿

科睿医疗(care-real)是一家医疗器械合同研究组织(CRO),主要业务为:
●医疗器械全生命周期的临床评价;
●医疗器械多国合规准入全流程策划与一站式服务。
公司专注于医疗器械临床研究与临床评价,包括临床前可行性研究、注册临床研究、研究者发起的临床研究、同品种临床评价、上市后临床研究、真实世界研究。
公司聚焦于大外科、泌外、眼科、皮肤与整形、心内与心外领域,并拥有众多的临床专家资源,以及成功经验。
公司具有完整的临床研究服务组织架构与执行团队、质量管理体系、临床研究数据采集系统,能够满足临床研究与临床评价的全流程服务。
科睿能够提供多国准入的法规服务。

周先生
18118447767
请扫描上方二维码与我们联系

— END —



