到2022年12月为止,新冠病毒Covid-19已经在全球肆虐了三年。疫情放开的这一波时间里,身边小阳人与日俱增,在出现的各种症状中,咳嗽是最常见、也是症状最长的一种。咳嗽久了得不到及时治疗,会造成胸闷胸痛和肺部损伤,严重者还有咳血的发生,继续下去将会是严重呼吸系统疾病,甚至会危及生命。
01
新冠病毒感染导致肺部损伤巨大
新冠病毒感染导致的肺脏组织结构破坏,可能进展为严重的呼吸窘迫综合征(Acute respiratory distress syndrome,ARDS)并最终导致呼吸衰竭,此为各类病毒性重症肺炎患者死亡的最根本原因。
新冠病毒感染导致白肺
病理学研究显示,ARDS的发病机制主要是冠状病毒攻击肺泡细胞之后诱发的免疫反应;免疫细胞浸润导致肺泡血管内皮结构破坏,使血浆、血浆蛋白和血细胞涌入肺间质和肺泡腔,形成肺水肿;由于肺泡上皮组织被破坏,水肿液大量涌入肺泡内,导致肺泡弥散功能受限,无法行使正常呼吸功能;同时,随着组织损伤的加剧,细胞进一步释放各类炎性因子形成所谓“细胞因子风暴(cytokine storm)”;最后彻底摧毁肺内大部分的肺泡和支气管呼吸结构,使得通气-血流比例严重失调,导致顽固的低氧血症以及最终患者的死亡。
02
治疗新冠肺炎的新方式——MSCs来源的外泌体
外泌体(Exosomes)是由活细胞分泌的微小囊泡,其直径约为30-150 nm,具有典型的脂质双分子层结构,广泛存于各种体液(如血清、血浆、唾液、尿液、羊水等)中,携带和传递着十分复杂且重要的信号分子(如mRNA、miRNA、蛋白质、脂质、代谢物等),外泌体在机体的生理过程中发挥重要调控作用。

研究表明外泌体具有将信号分子递送到其他细胞的固有靶向能力,可作为细胞之间物质和信号通讯的途径,可以通过旁分泌或者内分泌的方式作用于组织或者细胞。基于这些特性,外泌体在炎症相关疾病和自身免疫性疾病治疗方面具有很大的应用前景,也成为了科学研究以及资本的新风口。值得注意的是,许多临床研究表明,间充质干细胞(MSCs)及其衍生的外泌体(MSCs-Exo)可显著减少由不同类型肺损伤引起的肺部炎症。

03
轻症、重症均有效!MSCs来源外泌体雾化治疗新冠肺炎安全可行
2022年5月26日,知名期刊《Stem Cell Reviews and Reports(干细胞评论和报告)》杂志(2022年影响因子6.692)发表了题为Nebulized exosomes derived from allogenic adipose tissue mesenchymal stromal cells in patients with severe COVID-19: a pilot study 的文章。研究结果认为,脐带间充质干细胞来源的外泌体雾化治疗新冠肺炎安全可行。研究者将源自人异体脂肪间充质干细胞衍生的外泌体haMSCs-Exos以雾化吸入形式对7名重症COVID-19患者进行干预,初步研究结果显示参与者肺部损伤得到显著改善。

现将文章部分内容摘出,仅供交流

正文
参与者的临床特征

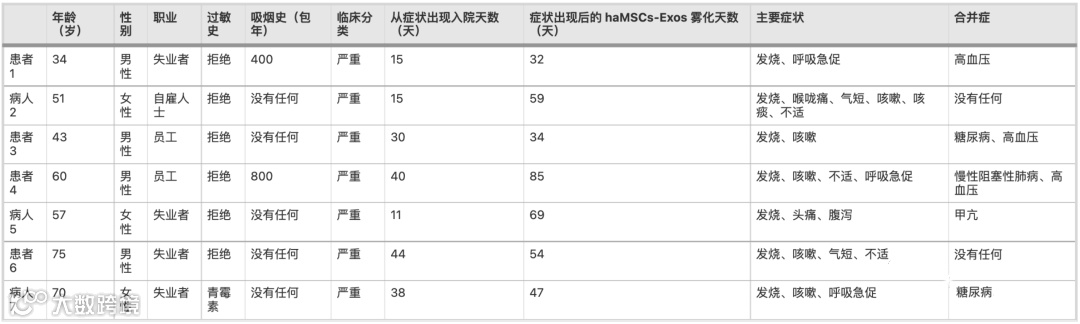
研究中入组患者的基础信息
研究结果

临床表现、实验室和放射学检查结果
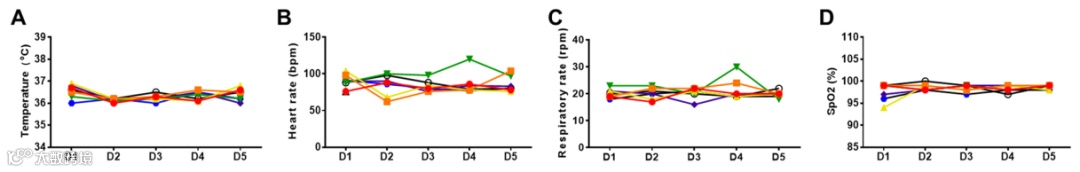
图示:A温度;B心率;C呼吸频率;D COVID-19 患者 hMSC-Exos 雾化干预前后的氧合血红蛋白饱和度。

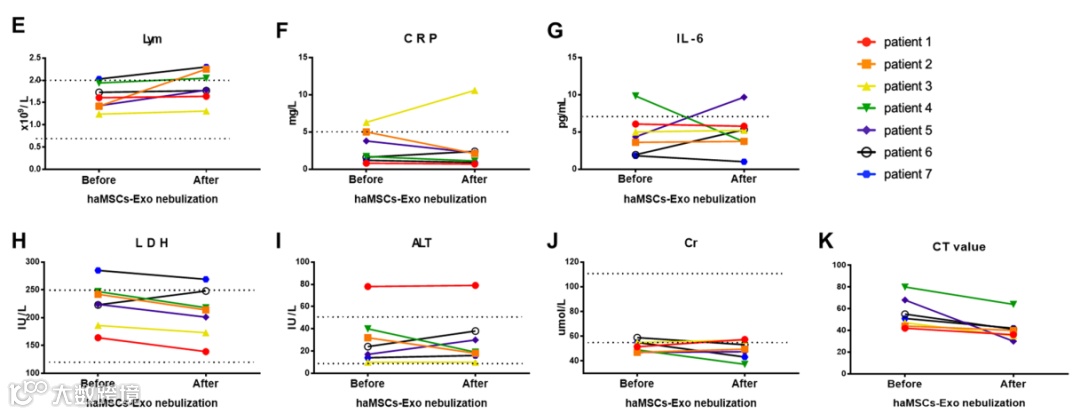
图E-J为COVID-19患者haMSC-Exos 雾化前后实验室参数的动态变化。图K为COVID-19患者haMSC-Exos 雾化前后的胸部CT评分。


COVID-19 患者吸入haMSC-Exos前后胸部 CT 扫描的变化

雾化治疗后患者的随访反馈
结论

如果把干细胞比作“物流站”,那外泌体完全可以用“快递员”来形容。它的作用就是将干细胞分泌出的各种有用的物质,运送到需要的组织和细胞中。这些囊泡小包裹中包含的很多影响其他细胞行为的重要物质,影响和促进原本细胞功能的提高和自我修复。
科研人员突破了给药途径的局限,在方法学上尝试创新,将外泌体雾化后吸引人体,起到修复肺部损伤的作用,为新冠肺部损伤的治疗带来了更多可能。
雾化外泌体优势
1、靶向强:通过雾化呼吸,靶向输送到肺部,无需通过血液循环输送。
2、生物利用度高:避免肝脏的首过效应,提高活性成分的生物利用度。
3、见效快:采用干细胞外泌体活性因子,分子量比细胞还小,可以快速深入组织细胞内部快速起到改善作用。
4、安全性高:外泌体无细胞核为非免疫原性,非药物,无副作用。
5、提高免疫力:可修复受损和清除变异的肺部细胞,激活处于抑制状态的。细胞,提高免疫力。
6、使用方便:操作简单,潮式呼吸有效,无需配合,使用简便,在家都可以使用。
雾化外泌体对肺部的作用
1、净肺:由于修复与不断再生肺泡细胞并保持高度活性,加速新陈代谢,达到自然快速净化肺部细胞。
2、润肺:由于携带蛋白质、酶、生长因子等细胞所需营养,达到自然滋养肺部细胞。
3、养肺:由于调节了肺部细胞的免疫能力,减少有害细胞与病毒的受侵,达到给肺部细胞良好的生存内环境。
附:参考文献:
[1]Hashemian S-MR, Aliannejad R, Zarrabi M, Soleimani M, Vosough M, Hosseini S-E, Hossieni H, Keshel SH, Naderpour Z, Hajizadeh-Saffar E, Shajareh E, Jamaati H, Soufi-Zomorrod M, Khavandgar N, Alemi H, Karimi A, Pak N, Rouzbahani NH, Nouri M, Sorouri M, Kashani L, Madani H, Aghdami N, Vasei M, Baharvand H. Mesenchymal stem cells derived from perinatal tissues for treatment of critically ill COVID-19-induced ARDS patients: a case series. Stem Cell Res Ther 2021;12:91.
[2]Lanzoni G, Linetsky E, Correa D, Messinger Cayetano S, Alvarez RA, Kouroupis D, Alvarez Gil A, Poggioli R, Ruiz P, Marttos AC, Hirani K, Bell CA, Kusack H, Rafkin L, Baidal D, Pastewski A, Gawri K, Leñero C, Mantero AMA, Metalonis SW, Wang X, Roque L, Masters B, Kenyon NS, Ginzburg E, Xu X, Tan J, Caplan AI, Glassberg MK, et al. Umbilical cord mesenchymal stem cells for COVID-19 acute respiratory distress syndrome: a double-blind, phase 1/2a, randomized controlled trial. Stem Cells Transl Med. 2021;10:660–73.
[3]Shi L, Huang H, Lu X, Yan X, Jiang X, Xu R, Wang S, Zhang C, Yuan X, Xu Z, Huang L, Fu JL, Li Y, Zhang Y, Yao WQ, Liu T, Song J, Sun L, Yang F, Zhang X, Zhang B, Shi M, Meng F, Song Y, Yu Y, Wen J, Li Q, Mao Q, Maeurer M, et al. Effect of human umbilical cord-derived mesenchymal stem cells on lung damage in severe COVID-19 patients: a randomized, double-blind, placebo-controlled phase 2 trial. Signal Transduct Target Ther 2021;6:.
[4]Dilogo IH, Aditianingsih D, Sugiarto A, Burhan E, Damayanti T, Sitompul PA, Mariana N, Antarianto RD, Liem IK, Kispa T, Mujadid F, Novialdi N, Luviah E, Kurniawati T, Lubis AMT, Rahmatika D. Umbilical cord mesenchymal stromal cells as critical COVID-19 adjuvant therapy: a randomized controlled trial. Stem Cells Transl Med. 2021;10:1279–87.
[5]Monsel A, Hauw-Berlemont C, Mebarki M, Heming N, Mayaux J, Nguekap Tchoumba O, Diehl JL, Demoule A, Annane D, Marois C, Demeret S, Weiss E, Voiriot G, Fartoukh M, Constantin JM, Mégarbane B, Plantefève G, Malard-Castagnet S, Burrel S, Rosenzwajg M, Tchitchek N, Bouch



