大家好!今天小编和大家分析一篇23年4月发表在Artificial Cells, Nanomedicine, and Biotechnology(IF:5.8)杂志的文章《Exploration of effective biomarkers and infiltrating Immune cells in Osteoarthritis based on bioinformatics analysis》。作者首先从GEO数据库中下载关于骨关节炎(Osteoarthritis,OA)的数据集。然后,利用xCell算法、GEO2R、SangerBox网站的富集分析、CytoHubba、ROC逻辑回归和相关性分析对数据进行了一系列分析。最后,获得了九种在OA和正常样本中丰度不同的免疫浸润细胞。通过差异基因和免疫相关基因取交集获得了42个差异免疫基因,发现它们的功能与免疫细胞和相应的生物过程关系密切。此外,还发现了5个枢纽基因(GREM1、NRP1、VEGFA、FYN和IL6R)。相关性分析表明,NRP1与NKT细胞呈负相关,NRP1和GREM1与aDC呈正相关,VEGFA与CD8+ naïve T细胞呈正相关,而VEGFA、FYN和IL6R与巨噬细胞M1呈负相关。得出这5个中枢基因可作为OA的有效诊断生物标志物。
背景
骨关节炎(Osteoarthritis,OA)是一种病因不明的慢性退行性关节疾病。它以关节软骨退化和继发性骨质增生为特征,临床表现为进行性关节疼痛,导致关节僵硬、活动受限甚至功能丧失。在全球范围内,OA是最常见的慢性关节疾病,发病率随着年龄的增长而逐渐增加。截至2017年,受OA影响的人数已达3.03亿,对人类健康构成了重大威胁,并造成了巨大的经济负担。然而,OA的发病机制仍不清楚。为了制定更好的OA预防和治疗策略,有必要阐明这种疾病发生和发展的潜在机制。
OA 是一种非常复杂的疾病,由多种因素相互作用引起,如年龄、职业、肥胖、代谢因素和免疫因素。值得注意的是,免疫因素在整个OA病程中具有重要影响。研究发现,滑膜组织内浸润的巨噬细胞、中性粒细胞和淋巴细胞在调节OA的慢性炎症过程中起着重要作用。这些浸润细胞通过产生大量细胞因子和趋化因子,刺激软骨细胞产生基质降解酶,加速软骨破坏,促进OA的发生。近年来,对OA中巨噬细胞极化及相关细胞因子进行了广泛的研究,并报道了其与滑膜和软骨炎症及损伤反应有密切关系。此外,慢性炎症诱导的持续性关节软骨损伤和修复与多种免疫细胞有关,包括T淋巴细胞、B淋巴细胞、NK细胞和树突状细胞等。在此背景下,迫切需要系统的方法来估计免疫细胞在OA中的作用,并探索与免疫相关的诊断生物标志物,以帮助揭示OA中的免疫机制。
在本研究中,作者首先应用xCell算法探讨了OA与健康组织之间免疫浸润的差异。随后,通过一系列生物信息学分析筛选出与OA相关的差异表达基因(DEGs),并研究OA的潜在病理机制,包括差异表达分析、GO和KEGG富集分析、蛋白-蛋白相互作用(PPI)网络分析、Hub基因筛选、ROC逻辑回归等。最后,采用相关性分析方法分析了候选生物标志物与重要浸润免疫细胞之间的关系。这项研究有助于确定诊断OA新的生物标志物,并为OA的诊断和免疫疗法提供新的见解。
方法:
从GEO数据库下载关于OA样本数据
差异表达基因的鉴定
免疫相关DEG的筛选
功能富集分析
枢纽基因的鉴定
评估候选生物标志物的诊断有效性
诊断生物标志物与浸润免疫细胞的关系
数据分析和可视化
研究结果
数据分析和可视化
首先基于GEO数据分析OA和正常组织中的免疫细胞浸润情况。PCA分析表明,两种样本类型之间的免疫细胞浸润差异具有统计学意义(图 1A).通过xCell算法分析了64种免疫细胞群的特异性浸润,并将其可视化为热图(图1B)和箱线图(图1C)。分析发现,OA与正常组织差异最显著的浸润免疫细胞以aDC、星形胶质细胞、CD8+ naïve T细胞、CMP、巨噬细胞、巨噬细胞M1、中性粒细胞、NKT和Th1细胞为主。并计算九个免疫细胞群的相应比例(图1D)。相关性分析表明,星形胶质细胞与CMP的正相关关系最强(r = 0.87),而NKT与中性粒细胞的负相关关系最强(r = -0.77)(图1E)。
箱线图表明,与正常组织相比,OA组织具有显着丰富的aDC,星形胶质细胞,CMP,巨噬细胞,巨噬细胞M1和中性粒细胞(图 2A-F),但丰度较低的CD8+ naïve T细胞、NKT和 Th1细胞(图 2G-I)。


OA和正常组织之间的IODEG
在GSE169077数据集中,在OA和正常组织之间共筛选出382个DEG,包括OA样本中的166个上调基因和216个下调基因(图 3A、B)。同时,从ImmPort数据库中检索到1,793个免疫相关基因。通过将382个DEG与1,793个免疫相关基因取交集(图 3C-D),获得了42个IODEG,包括23个上调基因和19个下调基因。

IODEG的GO和KEGG通路分析
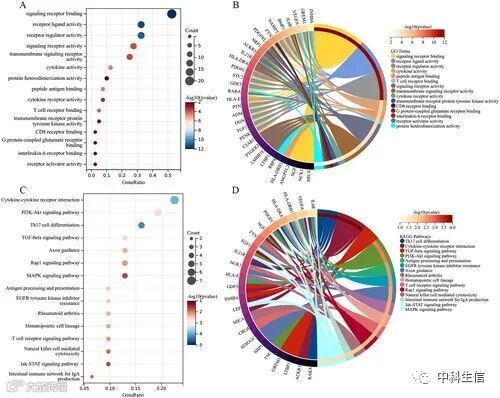
IODEG的GO通路由BP,CC和MF表示。关于BP,IODEGs主要富集于免疫细胞相关通路,包括细胞表面受体信号通路、免疫系统过程调节、细胞粘附调节和免疫系统过程正向调控(图 4A和4B);对于CC,IODEGs富集在MHC蛋白复合物,细胞外区域和细胞外基质(图 4C和4D);

而对于MF,IODEGs主要富集信号受体结合、受体配体活性、受体调节活性、T细胞受体结合和G蛋白偶联谷氨酸受体结合(图 5A和5B)。IODEGs最富集的KEGG通路涉及Th17细胞分化、细胞因子-细胞因子受体相互作用、TGF-β信号通路、PI3K-Akt信号通路、抗原加工和呈递、类风湿关节炎、T细胞受体信号通路和Jak-STAT信号通路(图 5C和5D)。总的来说,IODEG的功能与免疫细胞密切相关。
Hub基因的鉴定和可视化
IODEG的PPI网络是用STRING数据库生成的,并由Cytoscape可视化(图 6A,B)。通过 Cytoscape 的插件CytoHubba实现的8种算法,对前15个节点(基因)进行评分和可视化(图7A-H)。


使用R包“UpSet”进一步筛选得到8个Hub基因,包括VEGFA,FYN和IL6R,它们在OA中显示下调表达,以及NGF,PTN,FGF1,NRP1和GREM1显示上调表达。它们在GSE169077微阵列数据集中的表达可视化为热图(图 8A,8B)。8个Hub基因的表达在GSE55235和GSE55457数据集中得到验证,并可视化为箱线图和热图(图 8C,8D)。一致的是,VEGFA、FYN 和IL6R在OA 组织中的表达显著低于正常组织,而NRP1 和GREM1在OA组织中的表达率相反地显著更高。可以推断,VEGFA、FYN、IL6R、NRP1和GREM1可作为OA诊断的候选生物标志物。

评估候选生物标志物的诊断有效性
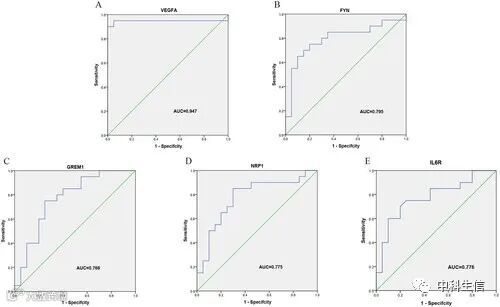
为验证5个Hub基因在OA诊断中的有效性,基于GSE55235和GSE55457数据集进行了ROClogistic回归分析。AUC 值>0.700被认为是有效且高度可靠的。研究发现,VEGFA、FYN、GREM1、NRP1和IL6R的AUC值分别为0.947、0.795、0.768、0.775和0.776(图 9A-E),表明5个Hub基因在OA诊断中具有良好的敏感性和特异性。
OA中诊断生物标志物与浸润免疫细胞的关系
分析了5种候选诊断生物标志物(VEGFA、FYN、GREM1、NRP1和IL6R)与9种差异浸润免疫细胞类型(aDC、星形胶质细胞、CD8+ naïve T细胞、CMP、巨噬细胞、巨噬细胞M1、中性粒细胞、NKT和Th1细胞)之间的关系,并通过 r > 0.70 和 p < 0.05 确定了显著的关系对(图 10A)。VEGFA与CD8+ naïve T细胞呈显著正相关(r = 0.852,p < 0.001)(图10B),而VEGFA(r = −0.840,p = 0.001)、FYN(r = −0.765,p =0 .006)和IL6R(r = −0.732,p =0 .010)与巨噬细胞M1( 图 10C-E)。此外,NRP1与NKT呈负相关(r = −0.764,p =0 .009)(图10F),而NRP1 (r = 0.700, p = 0.021) 和 GREM1 (r = 0.764, p = 0.009) 与 aDC正相关(图 10G,10H)。




