早!今天小编和大家分析一篇2023年6月发表在《Front Immunol》(IF:5.0)期刊上的文章《Mitochondrial DNA methylation is a predictor of immunotherapy response and prognosis in breast cancer: scRNA-seq and bulk-seq data insights》。本研究采用生物信息学工具,确定了BC中线粒体DNA甲基化(mitochondrial DNA methylation, MTDM)相关基因(MTDM-associated genes, MTDMAGs),并建立MTDMAGs预后模型;进一步使用免疫微环境、微卫星不稳定性、突变、无监督聚类、恶性细胞亚型分化、免疫细胞亚型分裂和细胞通讯特征分析来评估MTDM介导的免疫微环境的改变。最后,通过细胞实验来验证MTDM相关预后基因NCAPD3在BC中的作用。这些富有洞察力的发现为肿瘤免疫提供了新的视角,并有可能彻底改变BC的诊断和治疗。该思路同样适用于其它肿瘤分析,有相关需求的老师欢迎联系我们。
背景:
线粒体DNA甲基化(mitochondrial DNA methylation, MTDM)的改变存在于许多肿瘤中,但其在乳腺癌(breast cancer, BC)发展中的作用尚不清楚。
方法:
1,结合scRNA-seq和bulk-seq来分析BC患者的数据;
2,TCGA数据的加权共表达网络分析(WGCNA)确定了BC中MTDM相关基因;
3,COX回归和LASSO回归用于建立预后模型;
4,使用多种方法评估MTDM的生物学功能,如信号通路富集分析、拷贝数核型分析和细胞增殖率的定量分析;
5,使用免疫微环境、微卫星不稳定性、突变、无监督聚类、恶性细胞亚型分化、免疫细胞亚型分裂和细胞通讯特征分析来评估MTDM介导的免疫微环境的改变;
6,进行细胞实验来验证MTDM相关预后基因NCAPD3在BC中的作用。
研究结果:
(一)单细胞测序分析描述MTDM分区和BC细胞定位
利用GSE195861数据集进行单细胞数据分析。使用“KNN”算法,将选定的细胞分为12个簇(Fig 1A),然后根据细胞特异性标记物的表达水平对其进行注释。注释结果显示,簇中存在五种细胞类型:B细胞、T细胞、内皮细胞、上皮细胞、巨噬细胞和其他细胞类型,其中上皮细胞最多,内皮细胞最少(Fig 1B,Fig 1C)。为了确定筛选细胞中的MTDM水平,根据MTDM相关基因表达的中位数,将注释细胞分为高MTDM组和低MTDM组,高MTDM组主要集中在上皮细胞和巨噬细胞中(Fig 1D)。通过检测MTDM相关基因的表达来验证MTDM组划分的准确性。结果显示,在低MTDM组中,所有线粒体编码的多肽都显著上调(Fig 1E),与之前的报道一致。因此,MTDM组的划分是合理的。为了确定MTDM和BC恶性肿瘤之间的相关性,我们将注释细胞分化为导管原位癌(DCIS)和浸润性导管癌(IDC)细胞(Fig 1F)。结果显示,与DCIS组相比,更具侵袭性的IDC组的上皮细胞与高MTDM组的上皮细胞有更高的重叠。因此,高MTDM状态可能有助于BC的进展。

(二)线粒体DNA甲基化程度高的BC细胞容易恶性
为了进一步探索具有高MTDM状况的BC细胞的恶性倾向,进行了生物途径富集分析和拷贝数核型分析。生物途径富集分析结果表明,MTDM组基因的改变不仅发生在增殖相关的E2F信号通路、MYC信号通路、G2M检查点、转移相关的WNT信号通路和上皮-间充质转化相关的生物通路中,还发生在细胞凋亡、血管生成、炎症反应和代谢相关的通路中(Fig 2A)。拷贝数核型分析表明,恶性BC细胞主要集中在上皮细胞中,其分布区域与高MTDM区域高度重叠(Fig 2B)。考虑到肿瘤增殖率较高的患者通常预后较差,通过使用增殖相关标志物区分单个细胞,进一步检查了MTDM状态和增殖之间的关系(Fig 2C)。结果显示,高增殖区与高MTDM区重叠,表明高MTDM状态下有恶性倾向。为了探索影响MTDM的关键基因,使用WGCNA分析了与MTDM相关的基因模块获得了7个非灰色模块,其中绿松石和黄色模块与MDTM评分的相关性分别为0.68和-0.53,这两个模块中包含的基因与MDTM得分密切相关(Fig 2D)。选择P值<0.001的基因进行进一步分析。

(三)线粒体DNA甲基化状态对BC预后有价值
考虑到MTDM水平变化对各种生物学过程的影响,作者研究了与MTDM水平改变相关的基因是否可以作为BC患者的预后指标。因此,基于564个高和低MTDM组的差异表达基因和WGCNA分析所得的MTDM相关基因,进行单变量Cox分析,在TCGA队列中确定了16个与患者预后相关的基因(P<0.05)。进一步进行LASSO回归分析,并鉴定了11个基因(ARID1B、B3GNT2、MPHOSPH10、NCAPD3、RABGAP1、RBM41、RBMXL1、SLBP、TMEM167A、TMEM67和TUBGCP5)(Fig 3A,Fig 3B)。为了将患者分为高风险组和低风险组(即高MTDM组和低MTDM组),使用11个基因和中位数构建了预后模型。结果显示,TCGA训练队列中的高MTDM组的预后比低MTDM组差(P<0.0001,Fig 3C)。在GSE21653验证队列中也观察到了同样的趋势(P=0.016,Fig 3D)。在训练和验证队列中进行ROC曲线分析,进一步评估MTDM在预测BC患者预后方面的准确性。在TCGA队列中,1年、2年和5年时的曲线下面积(AUC)值分别为0.734、0.731和0.706(Fig 3E),在验证队列中,分别为0.732、0.686和0.673(Fig 3F)。这些结果表明,在两个队列中,MTDM状态可以准确地用于预测BC患者的预后。此外,作者对训练集和验证集模型中的11个基因进行了主成分分析,结果表明,构建的模型可以区分两个队列中的高MTDM和低MTDM(Fig 3G,Fig 3H)。

(四)筛选正向调节乳腺癌细胞增殖的MTDM相关预后基因
由于MTDM水平的改变可能影响BC细胞增殖,因此需要进一步筛选积极调节BC增殖的MTDM相关预后基因,这些基因可能被用作治疗靶点。因此,作者首次探索了MTDM相关预后基因在不同细胞类型中的表达。结果显示,除ARID1B在B细胞中高表达外,所有MTDM相关基因在上皮细胞中均高表达(Fig 4A)。此外,所有与MTDM相关的预后基因在恶性细胞和具有高MTDM状态的细胞中高度表达(Fig 4B-4D)。
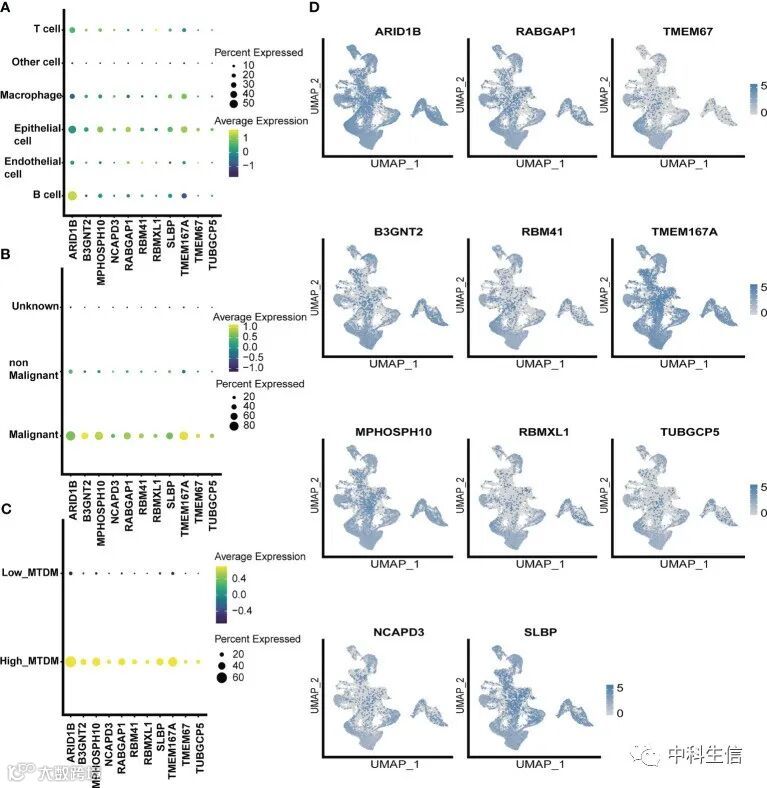
此外,作者研究了高增殖率组和低增殖率组中MTDM预后相关基因的表达(Fig 5A),发现除ARID1B在低增殖率小组中高表达外,所有MTDM相关预后基因在高增殖率小组均高表达。同样,在TCGA BC患者队列中使用ssGSEA生成增殖相关标志物的评分(Fig 5B)。高增殖率组和低增殖率组通过增殖相关标志物得分中位数进行区分(Fig 5C)。结果表明,MPHOSH10、NCAPD3和SLBP在高增殖率下高表达,其中在NCAPD3中观察到最显著的差异。相关热图结果还显示,NCAPD3与增殖相关标志物呈显著正相关,并与MKI67的相关性为0.52(Fig 5D)。进一步细分了恶性细胞,以关注MTDM相关预后基因与恶性细胞之间的关系。共鉴定了六个恶性细胞簇(Fig 5E),并比较了每个簇的特征基因,发现簇1在增殖相关标记物中高度表达,如MKI67、CCNB1和UBE2C(Fig 5F),GSVA分析还显示簇1在增生相关通路中高度富集,如MYC信号通路、DNA修复通路,E2F信号通路和G2M检查点信号传导(Fig 5G)。这表明簇1是处于增殖状态的恶性细胞。最后,研究了恶性细胞亚群中MTDM相关预后基因的表达,与TCGA BC患者队列一致,NCAPD3在增殖状态的恶性细胞中表达最高(Fig 5H)。这些结果还表明,高MTDM状态可能促进恶性细胞增殖,尤其是NCAPD3可能在这一过程中发挥关键作用。

(五)免疫微环境的变化表明MTDM状态可能响应BC免疫治疗的敏感性
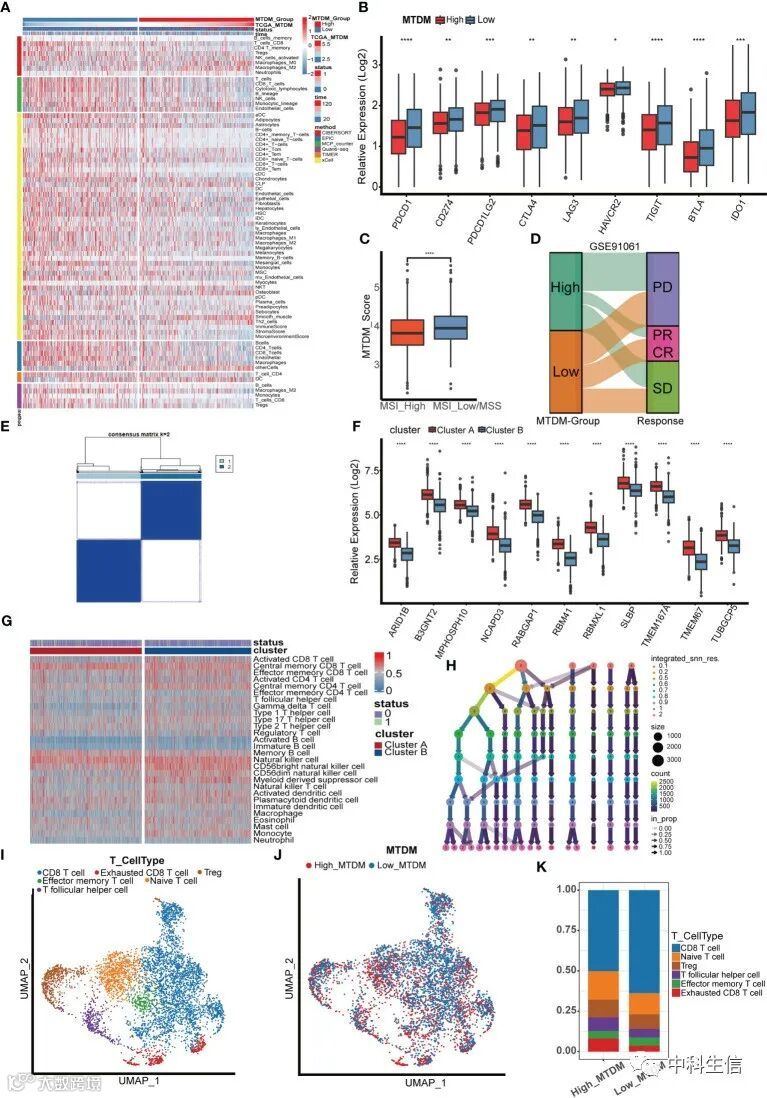
接着,作者探讨了高MTDM组和低MTDM组之间免疫细胞浸润水平的差异。结果显示,低MTDM组的免疫细胞浸润增加,包括B细胞、NK细胞和T细胞(Fig 6A)。分析了免疫检查点相关基因的表达,结果显示,纳入研究的免疫检查点有关基因在低MTDM组中高度表达(Fig 6B)。为了探讨免疫疗法是否更适用于低MTDM组,计算了MSI和TMB评分,以评估它们与MTDM的关系。结果表明,高MSI组的MTDM评分较低(Fig 6C),这一证据表明,低MTDM组的患者可能从免疫检查点抑制剂中受益更多。然而,作者发现高MTDM组的TMB较高,并且与免疫浸润程度呈负相关,这与大多数研究中TMB与免疫浸润之间的正相关不一致。因此,TMB评分不适合作为BC免疫治疗的生物标志物。为了进一步验证这个预测,作者使用了免疫疗法治疗的黑色素瘤患者队列GSE91061(Fig 6D)。正如预期的那样,低MTDM组获得CR或PR的患者比例最大。同时,无监督聚类显示,在TCGA数据集中,MTDM相关预后基因分为两组(Fig 6E-6F)。两组之间的免疫细胞也存在显著差异(Fig 6G),聚类B显示MTDM相关预后基因的表达较低,免疫细胞浸润水平较高。最后,在单细胞数据集中分化了T细胞,根据决策树,最佳聚类阈值为12个(Fig 6H)。根据可用的标记物,将T细胞分为CD8阳性T细胞、耗竭性CD8 T细胞、T卵泡辅助细胞、效应记忆T细胞、幼稚T细胞和Tregs(Fig 6I)。两组之间的细胞比例显示,高MTDM组具有更高比例的耗竭性CD8 T细胞(免疫功能障碍的标志物),而低MTDM组的CD8阳性T细胞比例更高(Fig 6J-6K)。这些结果表明,低MTDM组可能对免疫疗法更有反应。
(六)细胞通讯揭示了MTDM介导免疫抑制的潜在途径
接着,作者探索了不同MTDM状态下恶性细胞与T细胞亚群之间的细胞通讯特征,细胞间通讯特征可以有效识别细胞群之间存在的受体-配体关系,使用这种方法来揭示高MTDM/增殖相关的恶性细胞和免疫细胞亚群之间可能的配体-受体对,作为对这两个亚群之间的联系和潜在作用机制的反应。结果表明,高MTDM恶性细胞发出GDF15信号(Fig 7A)。相反,衰竭的CD8 T细胞依赖GDF15的受体TGFBR2来接收该信号(Fig 7B-7C)。此外,高MTDM恶性细胞分泌GDF15和耗竭的CD8 T细胞表达TGFBR2是细胞特异性的(Fig 7D)。这些研究结果表明,具有高MTDM状态的恶性细胞可能通过分泌GDF15导致CD8 T细胞耗竭,从而导致免疫抑制。同样,作者探索了增殖相关恶性细胞(簇1)和T细胞之间的细胞间通讯。Fig 7E显示了衰竭的CD8 T细胞和高MTDM恶性细胞之间的整体通讯。同样的结果表明,增殖相关的恶性细胞特异性分泌GDF15,耗竭的CD8 T细胞接收该信号(Fig 7F-7H)。这表明GDF15可能是具有高MTDM状态和增殖率的恶性细胞的免疫抑制反应的关键因素。

(七)体外实验证实,MTDM相关预后基因NCAPD3确实促进乳腺癌细胞的增殖
由于NCAPD3在增殖相关恶性细胞中表达水平最高,并且与增殖相关基因呈正相关,于是作者进一步探讨了NCAPD3对BC的表达及其对免疫微环境的影响。在TCGA转录组中,NCAPD3在肿瘤中也高度表达(Fig 8A)。然后,分别评估了NCAPD3表达与免疫评分和MSI之间的相关性,发现NCAPD3的表达与免疫得分和MSI呈负相关(Fig 8B-8D)。接下来,在体外对NCAPD3敲除进行生物功能验证,以测试模型基因敲除是否阻止乳腺癌症细胞系的生长,这可能间接反映NCAPD4敲除是否改善乳腺癌症患者的预后。首先,使用q-PCR验证了转染后1天MDA-MB-231-BC细胞系中NCAPD3的mRNA水平(Fig 8E),并发现所有siRNA干扰均导致NCAPD3 mRNA表达显著降低(P<0.05)。作者还通过蛋白质印迹验证了转染2天后MDA-MB-231和BCAP-37BC细胞系中NCAPD3的蛋白水平(Fig 8F-8G),并再次发现siRNA序列导致NCAPD3蛋白水平降低(P<0.01)。为了评估NCAPD3对细胞增殖的影响,作者进行了CCK8和克隆形成测定。CCK8结果显示,在NCAPD3敲除后,与siRNA阴性对照(NC)组相比,MDA-MB-231和BCAP-37BC细胞系的细胞活力显著降低(P<0.05)(Fig 8H-8I)。克隆测定的结果显示,在两种BC细胞系中,NCAPD3表达减少的集落数量显著减少(Fig 8J-8K)。最后,进行了划痕分析,以测试NCAPD3敲低是否影响BCAP-37BC细胞系的迁移能力。结果显示,NCAPD3敲除组的划痕愈合明显慢于siRNA阴性对照组(NC)(Fig 8L),表明NCAPD3的敲除可能是抑制BC细胞增殖和迁移的有效策略。这些结果表明,NCAPD3靶向可能是BC治疗的理想结果,并可能改善患者预后。




