大家好,今天小编个大家分享一篇23年11月发表在Biochemical And Biophysical Research Communications杂志的文章《Identification and validation of palmitoylation metabolism-related signature for liver hepatocellular carcinoma》。众所周知,蛋白质S-棕榈酰化是一种可逆的翻译后修饰,广泛参与肿瘤的进展。然而,棕榈酰化代谢在肝癌(LIHC)患者的预后和肿瘤微环境特征中的功能尚不完全清楚。因此,本研究采用生物信息学方法在肝癌中鉴定了与棕榈酰化代谢相关的预后基因,并探索了这些基因在肿瘤微环境中的作用。
背景
蛋白s -棕榈酰化是一种可逆的翻译后修饰,广泛参与肿瘤的进展。然而,棕榈酰化代谢在肝癌(LIHC)患者预后和肿瘤微环境特征中的作用尚不完全清楚。
方法
从TCGA和ICGC数据库中获取LIHC患者的mRNA和临床数据。并从相关文献中收集了23个棕榈酰化代谢相关的基因用于本研究分析。采用一致性聚类构建棕榈酰化代谢相关的聚类。然后通过单因素Cox和LASSO回归在LIHC中建立与棕榈酰化代谢相关的特征(PMS)。另外,通过ssGSEA评估每个LIHC样本的免疫细胞评分。并通过GO,KEGG和GSVA进行了富集分析。最后,对样本进行了药物敏感性分析。
结果
基于23个PMG的表达,作者建立了3个不同的棕榈酰化代谢相关簇(图1A)。并通过热图显示了基因表达谱和临床病理变量在不同聚类中的分布(图1B)。另外,KM曲线显示,B组的预后最差(图1C)。在簇间共筛选出838个共有的DEGs(图1D)。DEGs主要定位于组蛋白修饰、mRNA代谢和转录共调控活性(图1E)。同时,DEGs主要集中于肝细胞癌、细胞周期、mTOR信号通路和mRNA监测通路(图1F)。GSVA分析显示,簇B通过NFKB明显定位于促癌通路,包括PI3K AKT MTOR信号通路和TNFA信号通路(图1G)。簇A定位于多种代谢途径(图1H)。

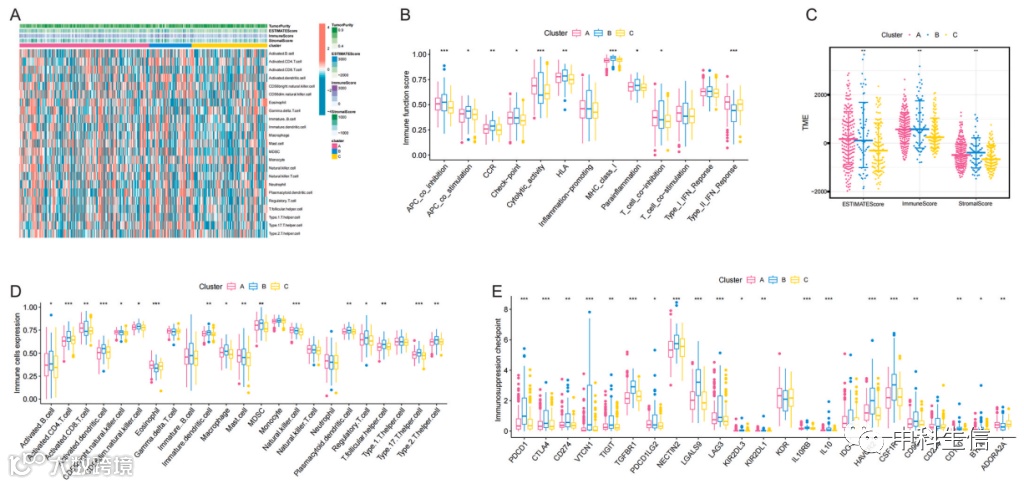
作者分析了浸润的特征。热图显示了肿瘤微环境评分和免疫细胞在细胞簇中的分布情况(图2A)。图2B显示,簇C的免疫功能评分最低。此外,基质评分、免疫评分和ESTIMATE评分在簇A和簇B中均显著过表达(图2C)。通过分析不同簇中免疫浸润细胞的差异表达,结果显示簇B免疫浸润细胞表达最高,C最低(图2D)。此外,大多数免疫抑制检查点的表达在簇B中最高,在簇A中最低(图2E)。
首先,我们发现这些PMG在LIHC中显著过表达,并与不良预后显著相关。然后,采用单因素Cox回归分析,筛选出8个与预后相关的PMG。(图3A)。然后,采用LASSO回归选择4个PMG建立PMS(图3B和C)。另外热图显示了4个预后基因在PMS组中的分布情况(图3D)。KM曲线和生存状态分布显示,高PMS组患者预后较差(图3E-G)。单因素和多因素Cox分析显示,PMS对LIHC患者预后的预测具有较好的准确性(图3I和J)。采用ICGC数据集作为外部验证数据集来验证PMS的准确性。KM曲线显示,KM曲线显示,在ICGC数据集中,高PMS组的患者预后较差(图3K)。ICGC数据集和TCGA数据集中均表明PMS有很好的预测能力(图3H)。

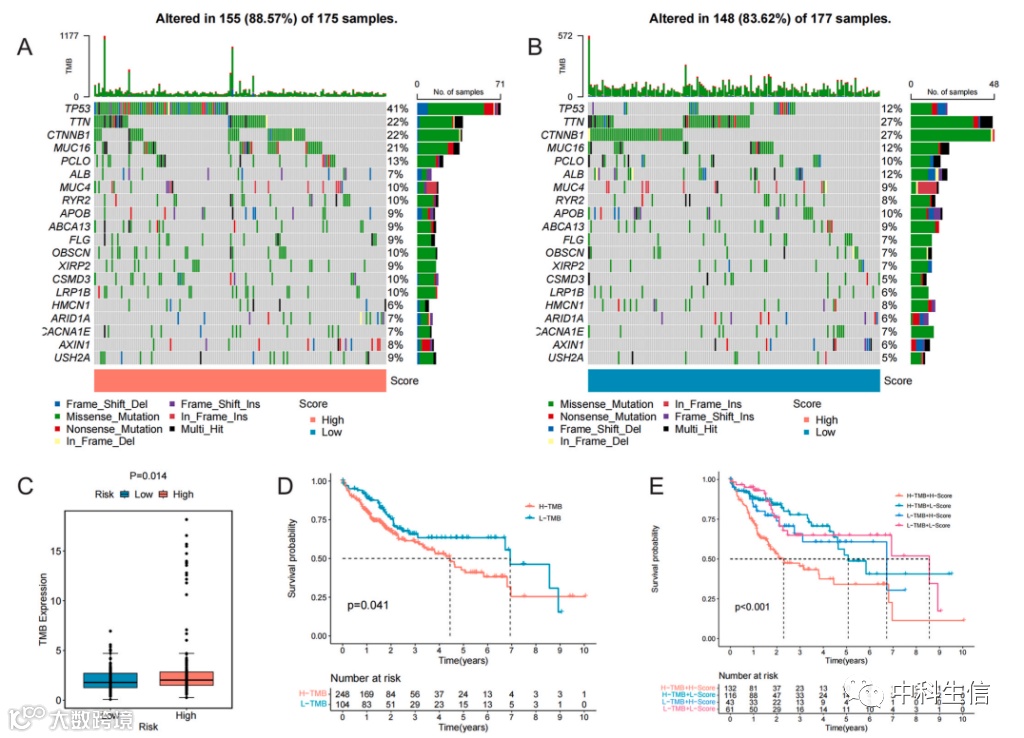
进一步评估了PMS与肿瘤突变负荷(TMB)之间的相关性。高PMS组的突变率为155/175(57 %),低PMS组的突变率为148/177(83.62%)(图4A和B)。同时,TMB在高PMS组中的表达量较高,与预期的相同(图4C)。因此,高TMB的患者预后可能较差(图4D)。接下来,评估了LIHC患者结合高低PMS组和高低TMB组的预后特征。KM生存曲线显示,H-TMB + H-PMS预后最差,L-TMB + L-PMS预后最好(图4E)。热图显示了PMS组中免疫细胞的表达(图5A)。图5B显示了免疫细胞与PMS之间的相关性。免疫抑制细胞(巨噬细胞、MDSCs、调节性T细胞)在高PMS组中显著过表达(图5C-E)。为了进一步评估经PMS组与免疫分型的相关性,随后分析了先前报道的全血癌免疫亚型中PMS的差异表达。PMS在C1和C2中的表达量较高,而在C3中的表达量最低(图5F)。图5G显示,C1和C2在高PMS组中占比较多,而C3和C4在低PMS组中占比较多。

为了评估PMS的预后特征,进一步分析了PMS与临床病理变量的相关性。首先,分析了PMS在不同临床病理变量中的差异表达。发现PMS在不同的临床病理变量(组织学分级、病理分期和T分期)上存在显著差异,且在晚期临床病理变量中显著过表达(图6A)。此外,作者还发现PMS组间不同临床病理变量的比例存在显著差异,高组组存在更高级的临床病理变量(图6B)。KM曲线显示,在不同的临床病理变量中,患者在高PMS组预后较差(图6C)。以上结果进一步证实了PMS与LIHC患者的预后呈显著负相关。为了进一步指导临床治疗策略的发展,筛选了15种主要化疗药物,以确定PMS是否与LIHC耐药相关。 B, Etoposide, gemcitabine, bortezomib and doxorubicin在低PMS组较高,提示这5种药物可能更适合于高PMS组的患者。

为了进一步分析导致肿瘤发生和进展的关键事件,分析了4个预后基因与临床病理变量之间的相关性。ZDHHC20在不同的临床病理变量中表达存在差异。ZDHHC20与LIHC患者的临床病理分期高度相关,并在LIHC中起促肿瘤作用。因此,作者进一步研究了ZDHHC20的免疫特性。图7A显示,高ZDHHC20组的免疫抑制细胞(MDSCs、调节性T细胞和巨噬细胞)过表达。同样,肿瘤微环境评分(免疫核心评分、间质评分)在ZDHHC20高组(估计评分)明显过表达(图7B)。此外,还进一步分析了ZDHHC20与免疫抑制检查点之间的相关性。结果显示,免疫抑制检查点在高ZDHHC20基因组中高表达(图7C)。

最后作者研究了ZDHHC20基因如何影响LIHC的增殖、迁移和凋亡,以进一步了解ZDHHC20在LIHC细胞中的作用。在HepG-2和SMCC-7721细胞中,si-ZDHHC20-1有效地降低了ZDHHC20的表达(图8A和B)。与si-NC组相比,CCK-8分析显示,ZDHHC20基因敲低影响了HepG-2和SMCC-7721细胞的增殖能力(图8C和D)。此外,ZDHHC20的缺失极大地抑制了HepG-2和SMCC-7721细胞的迁移,这可以通过跨孔迁移和伤口愈合实验得到证明(图8E-H)。流式细胞术检测结果显示,ZDHHC20显著降低了LIHC细胞的凋亡(图8I)。另外结合临床数据的列线图显示了ZDHHC20基因的表达与LIHC的临床特征之间的相关性。GSEA分析和来自人类蛋白图谱(HPA)数据库的免疫组化图像进一步验证了ZDHHC20在LIHC中的潜在作用。

结论
简单地说,本研究将LIHC患者分为3个具有不同预后和免疫特征的棕榈酰化代谢相关簇。此外,在LIHC患者中建立了一个棕榈酰化代谢相关的预后模型,这可能是预测LIHC患者预后和免疫反应的标志物。同时,ZDHHC20可能有助于构建免疫抑制肿瘤微环境,这可能成为免疫治疗的靶点,进一步指导临床治疗决策。
感兴趣的老师可以搜索查看。












