今天小编和大家分析一篇24年1月发表在Aging (Albany NY)(IF:5.5)杂志的文章《An endoplasmic reticulum stress-related signature featuring ASNS for predicting prognosis and immune landscape in prostate cancer》。背景:前列腺癌 (PRAD)是泌尿系统常见的恶性肿瘤之一。为了预测PRAD患者的治疗结果,本研究建议根据内质网应激(ERS)制定风险概况。基于纪念斯隆-凯特琳癌症中心(MSKCC)队列和基因表达综合数据库(GSE70769),验证了预测特征。使用随机生存森林分析,发现了具有预后意义的ERS相关基因。使用多变量Cox分析创建ERS相关风险评分(ERscore)。此外,还研究了与ERscore相关的生物学功能、基因突变和免疫景观,以揭示PRAD中与ERS相关的潜在机制。通过分析单细胞RNA测序(scRNA-seq)数据集(GSE137829)进一步探索了 ERscore相关机制,并通过体外实验探索了ASNS在PRAD中的致癌作用。本研究中构建的8个ERS相关基因构成的风险特征是一个独立的预后因素,并在 MSKCC和GSE70769数据集中得到验证。scRNA-seq数据还显示,在ERS评分高的组中,几种致癌途径明显过度激活。ASNS作为预后基因之一,在表达受到干扰后,会显著抑制PRAD细胞的增殖、迁移和侵袭能力。总之,本研究为 PRAD 患者开发了一种新的基于风险特异性ERS的临床治疗策略。
背景
前列腺癌 (PRAD) 的发病率在所有男性恶性肿瘤中排名第二。据估计,到 2022 年,美国将有 34,500 例 PRAD 死亡和大约 268,490 例 PRAD 新病例。2020 年全球记录了 1,414,259 例新病例和 375,304 例死亡。局部 PRAD 的标准治疗方法包括根治性前列腺切除术和根治性放射治疗。尽管大多数 PRAD 患者已治愈,但大约 35% 的根治性前列腺切除术患者和30-50%的根治性放疗患者在10 年内出现生化复发(BCR)。这些患者最终会发展为去势抵抗性PRAD,导致 32-45% 的患者在15年内死亡。为了预测复发风险并调整主动监测,必须确定 PRAD 进展和 BCR 的早期生物标志物。然而,PRAD 的早期预后已经区分了新出现的病理参数,这在临床实践中仍然存在一些局限性。因此,识别 PRAD 进展的预后生物标志物对于预见复发风险具有重要意义。
蛋白质折叠和钙储存的主要位置是内质网(ER),它还调节脂质膜和细胞内胆固醇的形成。相反,内质网应激(ERS)的合理性在于,面对缺氧、氧化应激、异常糖基化和钙稳态等应激条件,内质网应激(ERS)会干扰ER折叠蛋白质的机制,从而导致错误折叠或未折叠的蛋白质积累。此外,遗传改变还可以促进 ERS 并持续激活未折叠蛋白反应(UPR)通路。研究发现,ERS的过度激活会消耗细胞中的ATP,导致自噬甚至细胞凋亡。此外,ERS在肿瘤发展中起着不可或缺的作用。它改变了肿瘤细胞死亡、休眠和侵袭性发展之间的平衡,此外还特别影响实体瘤对化疗的敏感程度。另一方面,已经表明这种情况会改变肿瘤微环境(TME)中免疫系统的活动,从而抑制癌症的生长和复发。越来越多的研究表明,ERS与肝细胞和乳腺癌的肿瘤发展、侵袭性和对类似治疗的反应有关。此外,最近的一项研究表明,膀胱癌患者预后的预测与ERS相关的lncRNAs有关。ERS相关基因在PRAD中的潜在功能尚未阐明。
基于癌症基因组图谱(TCGA)数据库获取了转录组数据和相关临床信息,并从分子特征数据库(MSigDB)中提取了ERS相关基因集。此外,还从纪念斯隆-凯特琳癌症中心(MSKCC)和基因表达综合(GEO)数据库获得了数据。然后,使用 MSKCC 和 GSE70769 队列作为验证集,使用 TCGA 队列作为训练集。专注于研究ERS相关基因对预测PRAD患者BCR风险的影响,并通过将相关基因与PRAD临床病例联系起来来检查它们对肿瘤发展和进展的可能过程。
方法:
1.数据收集和预处理
2.共识聚类分析
3.生成 ERS 相关签名
4.功能富集分析
5.突变分析
6.评估免疫景观和肿瘤治疗反应
7.scRNA-seq 数据分析
8.ASNS 的体外实验
9.统计分析
10.数据可用性声明
研究结果
ERS 相关基因的共有聚类
根据ERS相关基因的表达谱,将PRAD患者分为两类(图 2A)。根据 Kaplan-Meier分析,集群2的BCRF存活率比集群1高得多(图 2B).GSVA富集分析发现,聚类1主要与突变相关通路相关,如同源重组、碱基切除修复、RNA 复制和错配修复。相反,簇2显著富集葡萄糖和氨基酸代谢,包括聚糖生物合成和降解、糖胺聚糖降解、丙酸酯代谢、β-丙氨酸代谢和色氨酸代谢(图 2C).GSVA 的进一步结果还揭示了两个集群之间免疫功能的显着差异(图 2D).综上所述,研究结果发现,两个与ERS相关的亚组在预后结局和生物学功能上是分开和不同的。

基于 ERS 的模型的构建
首先在TCGA队列中确定了47个与预后相关的基因(图 3A).通过RSF进一步选择了14 名候选基因,使用最小深度技术(图 3B,3C).采用多因素Cox回归,选择最后8个相关基因创建 ERscore,即 ASNS 、 FCGR2B 、 UFM1 、 SHC1 、 ATP6V0D1 、 PPP2R5B 、 MBTPS1 和 EIF2B5。(图 3D,表1)根据中位ERscore将患者分为高危组和低危组。高危组的BCRF生存率远低于低风险组 (图 3E).图3F显示了这些个体的 ERscore 分布、生存状态和 ERscore 概况。对于 1 年、 3 年和 5 年 BCRF 生存率,ERscore 的 AUC 分别为 0.722、0.740 和 0.754 (图 3G).
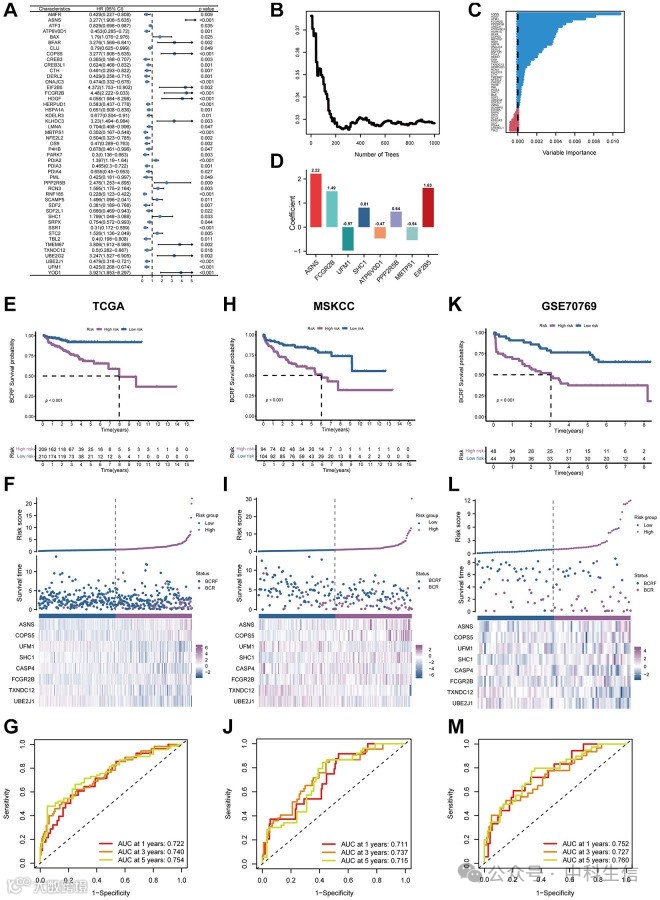
进一步的调查,发现较高的 ERscore 与较差的 TN 分期、较高的 GS 和较高的 BCR 可能性有关(图 4A).此外,高危患者更可能来自预后较差的第 1 组 (图 4B).此外,在单变量 Cox 回归中,发现 ERscore 和临床特征与 BCRF 生存率显著相关。ERscore 被揭示为独立的预测因子(图 4C).ROC 分析也支持 ERscore 预测的准确性 (AUC = 0.696,图 4D).ERscore 的预后价值也通过验证集(MSKCC 和 GSE70769)确认(图 3H–3M 和 4E、4F)。这些结果表明 ERscore 有可能指导临床治疗。

功能富集分析
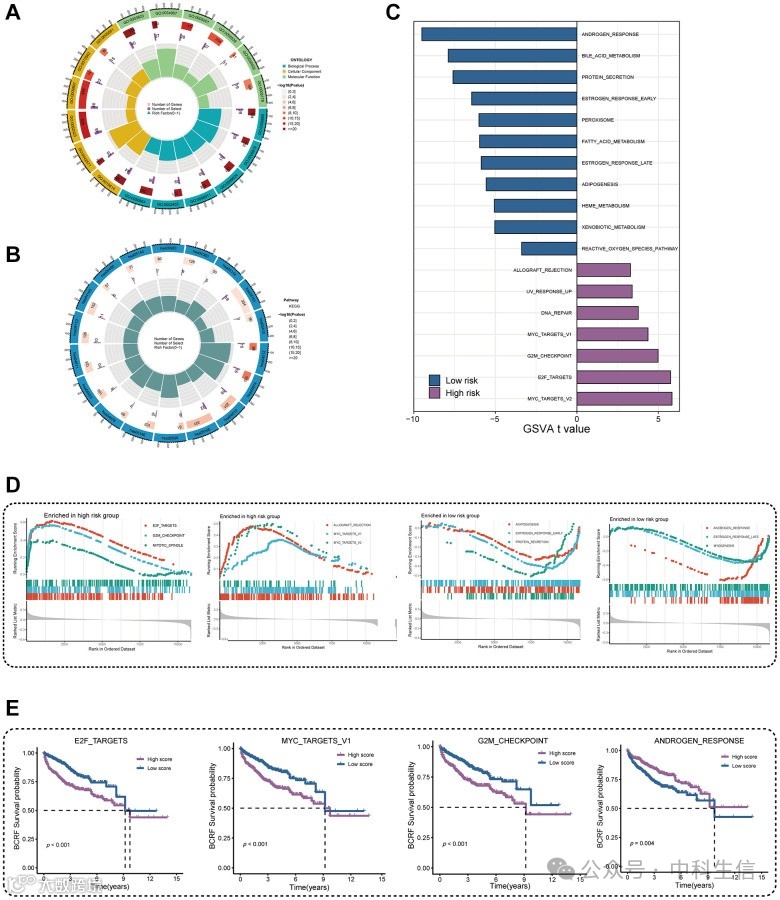
进行了 GO 和 KEGG 富集分析,以研究 ERscore 的潜在机制。PI3K-Akt 信号通路、p53 信号通路、有丝分裂纺锤体组装、染色体分离、免疫球蛋白受体结合和 B 细胞受体信号通路均被证明与 ERscore 相关 (图 5A,5B).根据上述 GO 和 KEGG 项目,ERscore 可能与免疫过程、肿瘤突变和致癌途径有关。在 GSVA 中纳入 50 个致癌特征通路后,结果显示 7 个特征通路在高危患者中显著增加,而 11 个通路在低风险患者中显著减少(图 5C).根据 GSEA 分析,高危组有7个基因高度升高,而低风险组有6个基因下调(图 5D).使用 Kaplan-Meier 方法分析交叉来源的途径,发现许多众所周知的致癌途径具有不同的BCRF生存概率,例如E2F_TARGETS、MYC_TARGETS_V1、G2M_CHECKPOINT 和 ANDROGEN_RESPONSE (图 5E).这表明 ERscore 在多种生物过程中发挥作用,尤其是PRAD中的致癌途径。
体细胞突变分析
瀑布图用于说明高危人群和低危人群之间的基因突变景观 (图 6A,6B)。TP53、SPOP、TTN、FOXA1和ATM是高危组中最常见的 5 个突变基因,而TTN、SPOP、TP53、KMT2D和MUC16是低风险组中突变频率最高的前 5 个基因。此外,分析了两个队列之间前 25 个突变基因中共存或排他性的突变,但没有观察到显著差异 (图 6C).根据致癌途径的突变富集,高危组 MYC、NRF 和 PI3K 信号通路显著增强,而 TGF-Beta 信号通路急剧减少(图 6D).与仅在高危人群中富集的 PIK3CA 和 FOXA1 相比,对致癌基因的研究中,SPOP 在高危和低危人群中均被证明富集(图 6E,6F).这表明 PIK3CA 和 FOXA1 在 ERS 相关肿瘤的发生发展中起重要作用。ERscore 和 TMB 之间的关系也是有利的 (图 6G,6H).生存分析还显示,高 TMB 和高风险评分的患者与不良预后相关 (图 6I).

免疫景观和治疗反应
通过检查肿瘤的免疫环境,发现高危组比低风险组有更多的免疫细胞浸润,包括 T 细胞、B 细胞、NK 细胞和巨噬细胞(图 7A).此外,高危组大多数免疫相关通路显著升高,包括免疫检查点、溶细胞活性、HLA 功能和 T 细胞共刺激 (图 7B).此外,发现免疫抑制受体表达在高风险患者(PD-1、CTLA4、BTLA 和 LAG3)以及免疫抑制配体(LGALS9 和 TNFSF14)中较高(图 7C).根据 TIDE 算法(图 7D).GSE91061队列的预期结果并未揭示这种差异,尽管 IMvigor210 队列中 ERscores 较高的患者比 ERscores 较低的患者具有更强的抗 PD-1 反应(图 7E,7F).考虑到 PRAD 对免疫治疗反应不佳的事实,评估了具有不同 ERscores 的 PRAD 患者的化疗反应。结果表明,各种化疗药物,包括 5-氟尿嘧啶、环帕胺、伊马替尼和沙鲁布里醛,在高危个体中的 IC50 值要低得多。图7G).

scRNA-seq 数据分析
样品预处理后,将细胞聚集并注释成 10 个主要簇:成纤维细胞、上皮细胞、恶性细胞、肌成纤维细胞、浆细胞、髓细胞、T 细胞、内皮细胞、B 细胞和肥大细胞 (图 8A)。随后,根据ERS相关的AUC评分(图 8B).高 ERS 评分组显示基于配体-受体信号转导的细胞间相互作用在数量和强度上增强(图 8C,8D).特别是,与低 ERS 评分组相比,高 ERS 评分组表现出升高的 EGF、VEGF、PDGF 和 IGF 信号通路(图 8E–8H).高 ERS 评分组和低 ERS 评分组患者表现出不同的细胞间通讯模式,高 ERS 评分组存在显著过表达的致癌途径。

ASNS 的体外实验
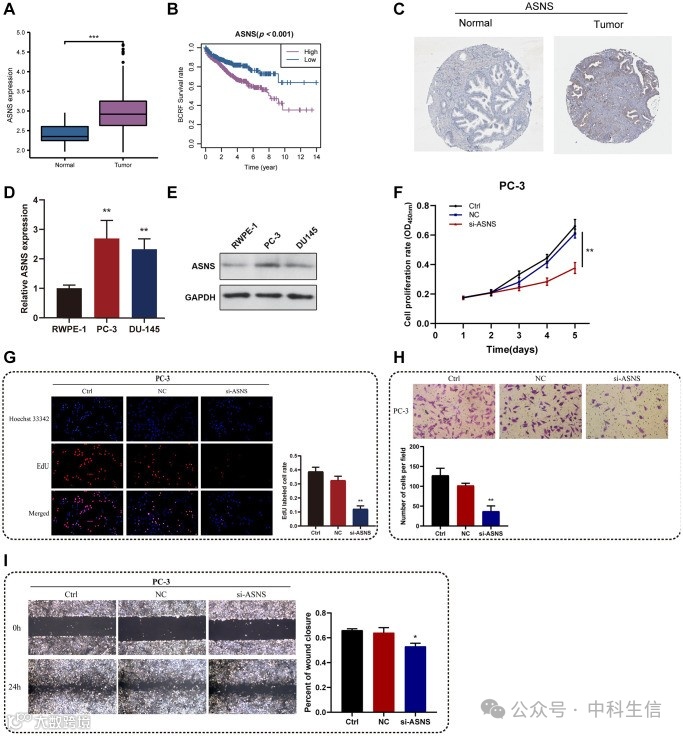
在构成 ERscore 的基本基因中,ASNS与PRAD预后密切相关(Coef = 2.22)。因此,选择了 ASNS 进行进一步分析。首先,TCGA 调查显示 PRAD 的 ASNS 表达比正常组织高得多,并且 ASNS 与 PRAD 患者 BCRF 生存率较差有关(图 9A,9B).来自人类蛋白质图谱 https://www.proteinatlas.org/ 的数据显示,ASNS 蛋白在 PRAD 中的表达相对较高(图 9C).随后,体外实验证实,通过 qRT-PCR 和 Western blotting 证实 ASNS 在 PC-3 和 DU145 细胞中的表达水平显著高于 RWPE-1 细胞。(图 9D,9E).为了验证预测的 ASNS 在 PRAD 中的肿瘤促进作用,使用 siRNA 敲低 PC-3 细胞中 ASNS 的表达,并使用 ov-ASNS 载体在 DU145 中过表达 ASNS。qRT-PCR 检测了 si-ASNS 的敲低效率,结果促使选择 si-ASNS 序列 2 进行进一步实验。通过应用 CCK-8 和 EdU 检测,发现抑制 ASNS 表达可以显著减慢 PC-3 细胞的分裂和增殖能力。图 9F,9G).此外,我们发现使用 Transwell 和侵袭测定 (图 9H,9I).这些发现表明 ASNS 可能成为 PRAD 患者的新靶点。