大家好!今天小编和大家一起分享一篇2024年4月发表在Journal of Translational Medicine.杂志的文章Comprehensive analysis of bulk and single-cell transcriptomic data reveals a novel signature associated with endoplasmic reticulum stress, lipid metabolism, and liver metastasis in pancreatic cancer:
背景
胰腺导管腺癌(Pancreatic ductal adencarcinoma,PDAC)既是最常见的胰腺恶性肿瘤,也是世界范围内死亡率最高的癌症之一。据报道大多数患者被诊断为晚期,而且肝转移是PDAC最常见的远处转移形式,这表明PDAC患者预后较差。肝转移既受肿瘤细胞的影响,也受肿瘤微环境的影响。然而,调控和促进PDAC细胞向肝组织转移的进一步机制仍有待探究。
内质网是调节钙稳态、脂质代谢、蛋白质合成和翻译后修饰的重要场所。内质网应激(Endoplasmic reticulum stress, ERS)是一种内源性和外源性损伤因素阻碍内质网正常折叠、分泌和修饰翻译后蛋白的能力,导致内质网细胞器中错误折叠蛋白负荷增加的情况。目前,持续和过度的ERS已成为包括癌症在内的许多人类疾病的关键因素,其可增强肿瘤细胞存活、血管生成、转移潜能、耐药性和免疫抑制。经过原癌基因家族MYC诱导的ERS在淋巴瘤、神经母细胞瘤等多种人类癌症中表现出未折叠蛋白反应(Unfolded protein reaction,UPR)的激活。然而,内质网应激在PDAC中的作用报道较少,除了UPR外,内质网应激在肿瘤发生和发展中的影响尚不清楚。
脂质代谢紊乱是肿瘤中最显著的代谢改变之一,它能提供肿瘤细胞增殖、侵袭和转移所需的能量、生物膜成分和信号分子。据报道,抑制SCD1通过内质网应激诱导的UPR导致肝肿瘤细胞分化。在胶质母细胞瘤、黑色素瘤、PDAC和前列腺癌中,乙酰辅酶a生成酶表达降低可降低肿瘤细胞活力并抑制肿瘤进展。下调LDLR可降低乳腺癌细胞、小细胞肺癌和PDAC细胞的胆固醇摄取和肿瘤增殖。酰基辅酶a氧化酶1 通过琥珀酰化和活性的增加来增强了原发性肝细胞癌细胞对氧化应激的反应。因此,脂质吸收、合成、水解等各方面的紊乱都与肿瘤的发生发展有关。然而,脂质代谢和内质网应激在PDAC肝转移中的作用有待进一步阐明。内质网应激可通过调节脂质合成和代谢关键酶的表达来影响脂质代谢。相反,脂质可以通过多种机制影响内质网功能和UPR。
肿瘤微环境(Tumor microenvironment,TME)的异质性对预后影响很大。TME在癌症免疫反应的调节中起着重要作用。肿瘤细胞及其微环境通常会产生大量免疫调节分子,这些分子可以消极或积极地影响免疫细胞功能。因此,阐明PDAC肝转移过程中免疫微环境的改变对改善患者预后至关重要。
本研究确定了PDAC中与ERS_脂质相关基因,并通过单细胞和大量转录分析识别了肝转移相关基因。随后,通过整合机器学习算法设计并验证了一种新的预后特征,这种风险特征在免疫特征分类、肿瘤突变负担(Tumor mutational burden,TMB)预后和药物选择方面显示出有效性。此外,在高和低ERS_脂质队列中仔细研究了细胞间信号传导,以揭示ERS和脂质代谢对肿瘤微环境和免疫反应的影响。
材料与方法
1.数据收集
从TCGA数据库((https:// por-tal. gdc. cancer. gov/)下载TCGA_PAAD队列的原始RNA_Seq数据。正常胰腺组的转录组数据从GTEx数据库(https:// www. gtexp ortal. Org)下载。TCGA和GTEx的转录组数据被整合并在数据集之间标准化处理,以共同筛选与胰腺癌相关的差异表达基因(Differentially expressed genes,DEGs)。GSE71729、GSE34153、GSE28735、GSE57495、GSE62452和GSE85916基因表达微阵列数据采集于GEO数据库(https:// www. ncbi. nlm.nih. gov/ geo/)。GSE154778和GSE197177的单细胞转录数据也从GEO数据库中获得。从ICGC数据库(https:// dcc. icgc. org/)下载PA_CA和PA_AU数据集的基因表达数据。从TCGA、ICGC、GEO(GSE28735、GSE57495、GSE62452和GSE85916)中合并并批入690例具有临床和基因表达信息的患者,通过R包将其随机分为训练集(n = 487)和验证集(n = 203)。
2.ERS与脂质代谢相关基因的鉴定
采用ssGSEA和共识聚类方法将ERS和脂质代谢相关途径和基因集分为2类。然后进行WGCNA分析,深度筛选与ERS和脂质代谢共表达的基因模块。最后,将文献中的521个脂质代谢基因和295个ERS相关基因以及紫色模块中的495个基因综合起来,对1240个基因进行后续分析。
3.肝转移相关基因的鉴定
利用单细胞RNA数据和RNA数据鉴定肝转移相关基因。筛选scRNA数据时(要求:nCount_RNA≥1000,nFeature_RNA≥200且nFeature_RNA≤10,000,percent.mt≤20以及percent.rb≤20)。选择RNA_snn_res.=1.5进行降级和细胞分组。采用tSNE和UMAP两种方法显示细胞聚类结果。Single R包用于注释细胞类型。采用WGCNA分析鉴定GSE71729和GSE34153共表达的肝转移基因。在scRNA数据集中使用Seurat包,在RNA数据集中使用limma R包获得原发肿瘤细胞与肝转移细胞之间的DEGs。然后,从肝转移共表达基因和DEGs中鉴定出1331个基因。最终,通过ERS与脂质代谢相关基因、肿瘤相关DEGs和肝转移相关基因的交集,选出92个潜在预后基因进行后续分析。
4.新型预后特征的构建和验证
为了建立一种新的预测胰腺癌总生存期(Overall survival,OS)的预后模型,我们整合和组合了10种机器学习算法(Cox boost、Lasso、stepwise Cox、plsRcox、Ridge、Enet、SurvivalSVMS、GBMs、SuperPC和RSF)来选择预后基因。然后,通过多元cox回归分析计算基因系数。根据公式(风险评分=Σ(Coefi×Exp))计算每位患者的风险评分。然后,根据风险评分的最优截止值将训练集中的所有患者分为高风险组和低风险组。采用Kaplan-Meier生存分析比较高风险组和低风险组的OS。在测试数据集和TCGA、ICGC队列中使用相同的计算公式和截止值。采用timeROC、ggDCA、survival和rms R 包绘制ROC曲线、DCA曲线和校准曲线,评价预后模型的准确性和一致性。
5.GSEA和KEGG富集分析
使用R包clusterProfiler和 enrichplot进行GSEA分析,识别高风险组和低风险组中的富集通路,并显示top5信号通路。通过GSVA分析分析风险评分和预后基因与肿瘤标志物的KEGG通路的相关性。使用R包scMetabolism进行单细胞转录组数据的代谢改变。
6.肿瘤突变负荷及药物敏感性分析
从TCGA数据库中收集SNP信息,然后使用R包“maftools”对高低风险组的基因突变信息进行分析。同时利用survminer R包探究了TCGA 队列中风险评分与TMB之间的相关性,并利用pRRophetic R包进行高风险组与低风险组之间的药物敏感性分析。
7.免疫微环境分析和细胞间通讯分析
采用CIBERSORT算法和ssGSEA方法对免疫浸润和肿瘤微环境进行计算估计。并通过ssGSEA分析了两个簇之间的免疫功能途径。还用limma和ggpubr R包分析了高风险组和低风险组的TCGA队列的TIDE和TCIA信息。通过CellChat R包分析了高风险组和低风险组之间细胞间的通讯分析。
8.细胞培养
本实验所使用的细胞来自北京大学第一医院普通外科实验室。HPNE和PANC1细胞在添加了10%胎牛血清的DMEM培养基中培养,而CAPAN1细胞则在添加了20%胎牛血清的IMDM培养基中培养,BXPC3细胞系在添加了10%胎牛血清的RPMI 1640培养基中培养。BXPC3细胞系被用作亲代细胞株,通过门静脉注射诱导的小鼠肝转移模型,建立了第一代肝转移细胞系。其中一部分第一代转移细胞系表现出增强的肿瘤生长能力和显著增强的远端器官转移潜能。随后,我们对这些细胞系进行了重复的门静脉注射和筛选,从体内转移后的肝转移灶中提取细胞,进一步培养和扩增,最终衍生出BXPC3_LMT细胞系。
9.定量聚合酶链反应 (qPCR) 和免疫组织化学
使用TRIzol试剂从HPNE、PANC1、CAPAN1、BXPC3和BXPC3_LMT等5个细胞系中提取RNA。使用PrimeScript™RT试剂盒对提取的RNA(1000 ng)进行逆转录。使用SYBR Green Master Mix进行实时定量PCR。 逆转录和qPCR反应体系均按照制造商的说明制备,所有操作均在冰上进行。使用GAPDH作为内参,通过2^− ΔΔCT方法计算相对基因表达水平。肿瘤组织和相应的邻近组织取自北京协和医院接受根治性切除术的80名PDAC患者。所有患者均进行了PDAC病理学验证,并获得了参与研究的所有参与者的知情同意。4 μm 石蜡切片在二甲苯中脱蜡,并在分级酒精中复水。使用EDTA缓冲液(pH 9.0)对 SOD2、P4HB 和TNFSF10进行抗原修复。随后,将切片在4 °C下用SOD2抗体(稀释度 1:40,000)、P4HB 抗体(稀释度 1:200)和 TNFSF10 抗体(稀释度 1:400)处理过夜。使用 DAB Plus 试剂盒进行染色。所有组织切片的评估均使用基于ImageJ的IHC Profiler插件进行,将切片分为三个级别:阳性(≥ 2+)、低阳性(1+)和阴性(0)。此外,切片由两名不知道样本身份的病理学家独立评估,所有评估均经过手动校正。
10.统计分析
采用Kaplan-Meier分析和log-rank检验比较高风险组和低风险组患者的OS。通过单因素和多因素Cox回归分析寻找患者预后的独立预测因子。采用Wilcoxon检验确定两组之间的基因表达水平,并评估两风险组之间TMB、药物敏感性、免疫评分、TIDE评分和IPS评分的差异。并用Spearman分析两组之间的相关性。每项分析都系统地重复进行,以确保结果的可靠性。所有统计分析均采用R软件进行。单因素检验双侧p<0.05,多重检验调整后p<0.05为统计学显著。
结果
1.PDAC中ERS和脂代谢相关基因的鉴定
为了研究胰腺癌中ERS和脂质代谢的预后意义,通过ssGSEA和一致聚类分析脂质代谢信号通路和ERS基因组(图1A,C)。共识矩阵热图显示k=2是最佳分类方法,将PDAC样本分为第1类(样本量=89)和第2类(样本量=89)。图1C中的聚类热图显示ERS和脂质代谢相关基因和途径在聚类1中具有较高的富集分数。然后进行WGCNA分析以确定PDAC高和低ERS_脂质人群中的共表达基因。在共表达网络构建过程中,我们观察到,当无标度拓扑的拟合指数达到0.9,识别出18个模块时,软阈值功率β为7(图1B,D)。在PDAC观察到紫色模块与ERS_脂质具有最显著的相关性(图1D)。最终,从标记基因和WGCNA模块基因中筛选出1240 个与ERS和脂质代谢相关的基因。
图1:ERS和脂质代谢相关基因的鉴定。(A)ERS和脂质代谢途径的一致性聚类分析,当k=2时,TCGA数据集被分成两个分化良好的亚组。(B)本节描述WGCNA分析的相关参数。(C)ERS和脂质代谢相关通路ssGSEA片段的热图和聚类。(D)WGCNA分析筛选出ERS_脂质共表达基因模块。
2.PDAC肝转移相关基因的鉴定
为了阐明PDAC肝转移的具体机制和内在驱动因素,进行了单细胞和批量转录分析以选择原发性PDAC组织和肝转移组织之间的DEGs(| log FC | > 1 和 FDR < 0.05)(图2和附加文件1:图S3)。检测样本中的每个细胞根据Single R包中的细胞类型参考进行评分,并通过细胞评分热图显示(图2A)。在GSE154778的单细胞转录分析中鉴定了9种细胞类型,在GSE197177群组中鉴定了11种细胞类型(图2B和附加文件1:图S3)。基因富集分析显示,肝转移上皮细胞中的细胞周期、嘌呤代谢、嘧啶代谢和代谢途径的得分显著高于原代上皮细胞(p<0.0001,图2C)。雌激素反应、雄激素反应、蛋白质分泌和其他信号通路在原代和肝转移上皮细胞中显著上调,而在巨噬细胞、单核细胞和T细胞中则相反。并且未折叠蛋白反应在肝转移上皮细胞中显著富集,但在原代上皮细胞中没有显著变化(附加文件1:图S3D,E)。通过WGCNA分析在GSE71729和GSE34153队列中筛选了肝转移共表达基因(图2D,E)。最后,从单细胞和大量转录组分析中鉴定出722个肝转移基因,从WGCNA分析中鉴定出857个肝转移共表达基因。通过limma R包筛选出TCGA和GTEx队列中正常组织和肿瘤组织之间的3887个DEGs(|log FC|>1且FDR<0.05)(附加文件1:图S2)。将所有鉴定的与ERS_脂质、肝转移和肿瘤DEGs相关的基因取交集,92个信号被包括在随后的分析中。
图2:肝转移相关基因的鉴定。(A)细胞评分热图。当一个聚类的单元分数在参考单元类型中明显高于其他标签时,它们被注释为该单元类型。(B)GSE154778数据集的细胞亚群聚类和注释结果。(C)原发组和肝转移组上皮细胞细胞周期、嘌呤代谢、嘧啶代谢和代谢信号通路的改变。(D,E)WGCNA分析筛选了GSE71729和GSE34153中与肝转移共表达的基因模块。(E)韦恩图说明了92个共有基因的存在。
3.基于机器学习的集成构建了PDAC的预测模型
对上面筛选的92个共有基因进行单变量Cox分析,并鉴定了42个预后基因(附加文件4:表S3)。然后,在基于机器学习的整合程序中分析这42个基因,以建立用于预测PDAC患者总体存活率的一致的ERS_脂质特征。采用留一交叉验证框架在训练集中拟合10个机器学习算法的组合并进行超参数调整,并在测试集进一步计算每个模型的C指数(图3A)。最佳模型是step Cox[backward]和plsRcox的组合,其在所有模型类型中具有最高的平均C指数(0.691)(图3A)。鉴定了7个具有主要预后价值的共有基因,并在模型中进一步计算了基因系数(图3B,C)。然后用回归系数对每个患者的7个基因表达进行加权,计算出风险评分。根据确定的最佳阈值,将所有患者分为高风险组和低风险组。为了进一步评估样本大小对模型准确性的影响,减轻过度拟合,并提高概化能力和可靠性,我们还在TCGA和ICGC数据集验证了该模型,并发现该模型在将患者分为高风险组和低风险组方面功能良好(图3D)。单变量Cox回归分析和多变量Cox回归分析提示,风险评分可以作为PDAC患者预后的独立危险因素(图3E和附加文件1:图S4)。此外,还建立了一个列线图,将临床变量和风险评分纳入临床应用(图3F)。根据临床特征对PDAC患者进行分层,该研究验证了ERS_脂质特征在不同临床亚组中的预后预测能力。结果表明ERS_脂质特征在不同年龄、性别、分级和T、N、M分类的患者中表现出良好的预后辨别能力(附加文件1:图S4)。这些发现表明,预后模型在不同的患者群体中表现出稳健性和通用性。
图3:胰腺癌预后模型的构建和验证。(A)机器学习预测模型的组合计算训练集和验证集上每个模型的C指数。(B)单变量cox回归分析的森林图显示了7个所选基因的风险比。(C)预测模型中的基因系数。(D)基于该模型的列车、测试集和TCGA、ICGC队列中OS的Kaplan-Meier曲线显示低风险组的生存时间更长。(E)进行单变量和多变量Cox回归分析,结合其他临床特征评估风险评分的预后价值。(F)在TCGA数据集中构建了一个结合风险评分和临床信息的列线图。
4.新模型的验证和评估以及相关的基因富集分析
为了进一步评估所建立模型的预后价值,分别在1年、3年和5年时绘制受试者工作特征(ROC)曲线并计算曲线下面积(AUC)。结果表明,风险评分的预后准确性明显高于年龄、性别和分期(图4A,B)。决策曲线分析(DCA)表明,风险评分在评估PDAC预后中的临床效益大于年龄、性别和分期(图4C)。1年、3年和5年风险评分的校准曲线显示,风险评分在预测训练和测试集的存活时间方面是稳定的(图4D)。从该预测模型得出的风险评分与肿瘤分级呈显著正相关,与低风险组相比,在高风险组中观察到的G3-4患者的比例显著更高(图4E,F)。这些发现表明这种风险特征与PDAC患者的临床进展之间存在关联。在所有的训练和验证队列中,高风险组的患者比低风险组的患者存活时间短(图4G)。还进行了GSEA分析以阐明高风险组和低风险组中的信号通路改变。结果显示,病灶粘连、胰腺癌、癌症中的途径和泛素介导的蛋白水解在高风险组中富集,而花生四烯酸代谢、氧化磷酸化和苯丙氨酸代谢在低风险评分的患者中富集(图4H,J和附加文件5:表S4)。用GSVA算法分析风险评分和标志性信号通路之间的相关性。风险评分与大多数肿瘤相关的信号通路显著正相关,例如MTOR、胰岛素、ERBB和Wnt信号通路,而与PPAR和Notch信号通路显著负相关(图4I和附加文件1:图S5)。
此外,还将构建的模型与之前发表的7个预后模型进行了比较。所有特征都表现出良好的预后辨别能力,与低风险组相比,在高风险组中观察到显著更低的存活时间(图5A-H)。然而,与之前发表的七个特征相比,ERS-Lipid特征在1年、3年和5年时显示出更大的AUC值,表明PDAC的预后准确性更高(图5I-P)。此外,ERS-Lipid特征在整个训练集和验证集中都显示出较高的C指数值,表明其具有优异的稳健性(图5Q)。结果表明,ERS_脂质特征在预测PDAC患者的生存结果方面功能良好(图4,5)。
图4:新预后模型的评估。(A)ROC曲线显示了模型在训练集和测试集中的1年、3年和5年生存预测准确性。(B)风险评分的AUC值高于临床特征的AUC值。(C)DCA曲线显示了风险评分和其他临床特征在预测临床结果中各自的益处。(D)1年、3年和5年的校准曲线评估了模型的预测稳健性。(E,F)风险评分与TCGA队列中患者的等级分类显著相关。(G)高风险组和低风险组的存活时间。(H,J)高风险组和低风险组中富集的前5个信号通路的校正P值< 0.05。(I)GSVA分析显示了KEGG途径和模型基因之间的关系。
图5:ERS _Lipid脂质相关预后模型与七种已发表的预后模型的比较。(A-H)Kaplan-Meier生存曲线表明,ERS_脂质特征和之前发表的七个预后特征在综合训练数据集中表现出显著的预后辨别能力。(I-P)ERS_脂质特征的ROC曲线下面积大于其他7个先前发表的特征。(Q)ERS_脂质特征在综合训练和验证数据集中显示了较高的C指数值。*p<0.05,**p<0.01,***p<0.001, ****p<0.0001。
5.高风险组和低风险组之间肿瘤突变负担和药物敏感性的分析
为了进一步探索肿瘤突变负荷(TMB)和风险评分之间的相关性,通过瀑布图将高风险组和低风险组中每个PDAC样本的体细胞突变景观可视化,并且观察到两个亚组中的前20个突变基因基本相同,但是总突变负荷在高风险组中为93.55%,在低风险组中为74.77%(图6A,B)。我们发现高风险组和低风险组中突变负荷最高的前4个基因KRAS、TP53、CDKN2A和SMAD4。对于变异的分类,错义突变、无义突变和移码缺失是所有突变类型中的前3位。结果还显示风险评分与TMB显著正相关(图6C,D)。并且高风险评分和高TMB组的患者的存活时间比低风险评分和低TMB的患者的存活时间短(图6E,F)。高风险组和低风险组中的药物敏感性分析显示,风险评分与多种药物敏感性相关(图6G)。结果显示,高风险组患者对5-氟尿嘧啶、阿法替尼、伊立替康、拉帕替尼和曲马替尼的敏感性低于低风险组,而在某一些药物的敏感性上出现了相反的结果,如多西他赛、表柔比星和吉非替尼(图6G)。
图6:高低风险人群肿瘤突变负荷和药物敏感性分析。(A,B)高风险组和低风险组中突变基因的累积改变。(C,D)TMB与风险评分呈正相关。(E-F)Kaplan-Meier曲线显示TMB和风险评分与不良预后相关。(G)高风险组和低风险组的药物敏感性。
6.高风险和低风险组之间的肿瘤免疫景观分析
为了评估高风险和低风险人群的免疫状况,我们分析了TIDE 评分和IPS评分的变化(图6A-H)。结果显示,高风险组的TIDE评分、免疫排斥评分和MDSC评分高于低风险组,表明免疫逃逸的可能性更高(图7A-D)。CTLA(+)PD1(-)的IPS在高风险组中显著降低,而CTLA(+)PD1(+)、CTLA(-)PD1(+)和CTLA(-)PD1(-)的IPS在高风险组和低风险组中没有显著差异(图7E–H),这表明高风险组的患者可能对免疫疗法反应不佳。还通过CIBERSORT和ssGSEA分析探索了免疫浸润的变化,这提供了肿瘤微环境内的计算估计。结果显示,在高风险组中CD8+ T细胞、M1巨噬细胞、T滤泡辅助细胞、T调节细胞和静息树突细胞的浸润水平下调,而浆细胞、静息记忆CD4+ T细胞、活化记忆CD4+ T细胞、静息NK细胞和活化树突细胞的浸润水平相反(附加文件1:图S6)。免疫浸润和免疫功能的丰富评分显示,高风险组活化B细胞、活化CD8+ T细胞、CD56亮NK细胞、CD4+中枢记忆T细胞和CD8+效应T细胞等免疫细胞明显下调。并且活化的CD4+ T细胞、自然杀伤T细胞、Th1辅助细胞和Th2辅助细胞的富集分数在高风险组中更高(图7I,J)。检查点基因与风险评分和预后基因的相关性也被分析并显示在图7K中。至于免疫功能,APC _ co _抑制、检查点和II型IFN应答信号通路在高风险组中上调,而免疫通路如APC _ co _刺激、CCR、细胞溶解活性和I型IFN应答信号通路在高风险组中降低(图7L)。此外,Fisher检验揭示了在高风险组和低风险组的患者中对免疫疗法应答的群组分布的显著差异(图7M)。子映射分析提供了额外的验证,即与高风险组中的患者相比,低风险组中的患者对靶向CTLA4的免疫疗法表现出更高的反应性(调整后的p值< 0.05)(图7N 附加文件6:表S5)。
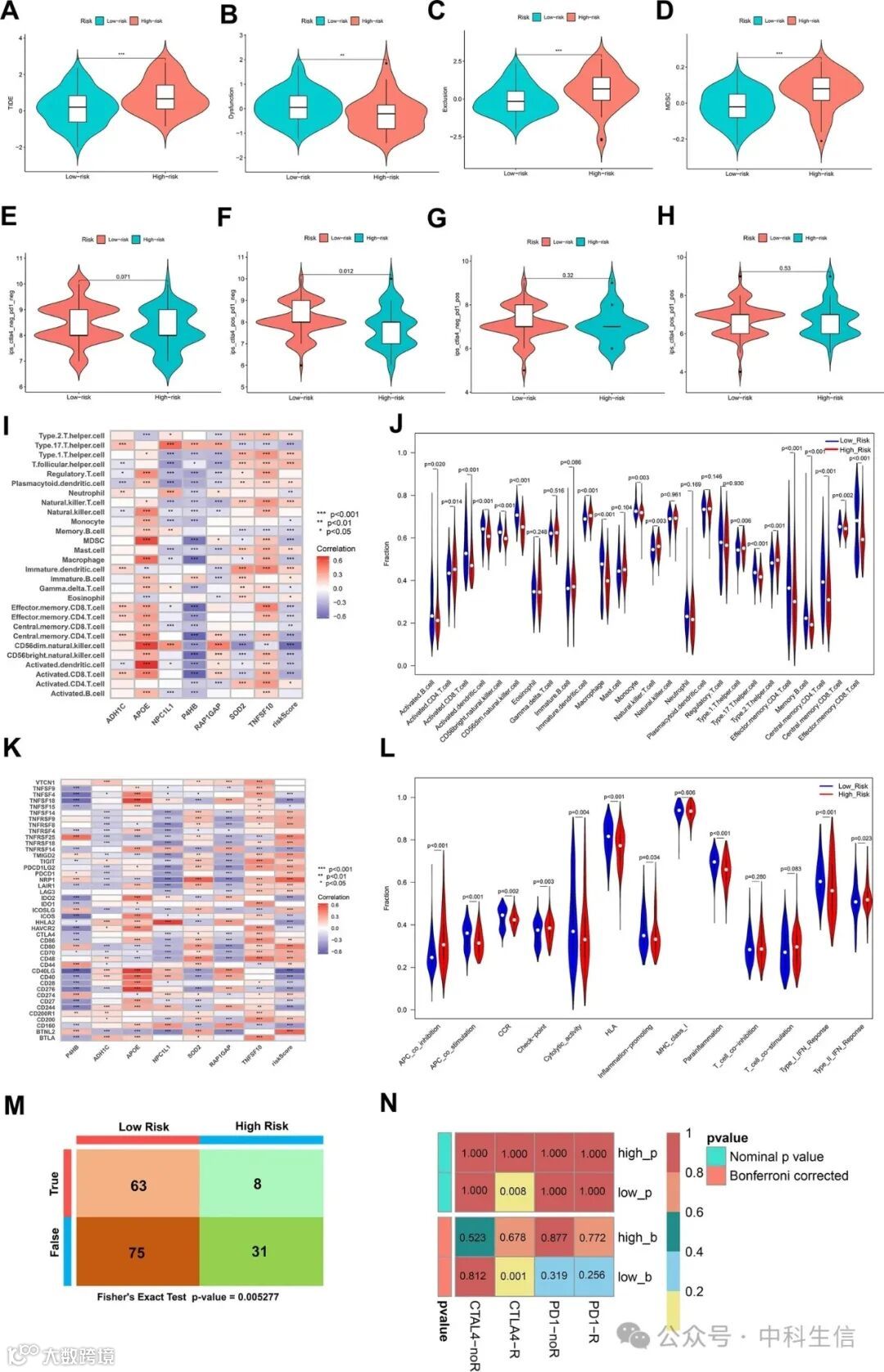
图7:高风险和低风险人群的免疫状况。高风险和低风险人群中(A)TIDE评分、(B)免疫功能障碍、(C)免疫排斥和(D) MDSC的改变。(E-H)高风险组和低风险组中PD1和CTLA4的IPS评分。(I,J)高风险组和低风险组中的免疫浸润变异。(K)风险评分与免疫检查点相关。(L)高、低危人群免疫功能改变。(M)Fisher检验揭示了在TCGA数据集中被分为高风险组和低风险组的患者中免疫治疗反应的队列分布。(N) 基于submap算法的患者对免疫检查点抑制剂(ICI)治疗的反应性和经Bonferroni校正的p值的TIDE评分。
7.高ERS组和低ERS组之间的细胞间通讯分析
CellChat算法被用于基于来自单细胞转录组的基因表达信息来探索和估计细胞间的信号传递。比较高ERS组和低ERS组之间的通讯模式,以预测PDAC细胞间通讯的病理变化。结果显示,在高ERS组中,细胞间通讯的数量和相互作用强度增加(图8A,B)。在高ERS组中,上皮细胞与巨噬细胞和单核细胞的相互作用数量和强度增加,而单核细胞、巨噬细胞和T细胞与上皮细胞的相互作用数量和其他细胞如上皮细胞与T细胞的相互作用强度下调(图8D)。然后计算每个信号传导途径的信息流,以确定所有细胞类型对之间的通信概率,并进一步量化上皮细胞和其他细胞之间的信息流(图8C,E)。在高ERS组,CLDN通路减少,而其他一些如RESITIN、MIF和SPP1增加。在高ERS组中,PECAM1信号通路关闭,而一些通路如CEACAM、桥粒和PTPRM信号通路打开(图8F,G)。我们选择了三个有趣的信号通路进行进一步分析。分析了高ERS组和低ERS组中所有细胞类型之间MIF、APP和SPP1信号通路中的通讯相互作用,如图8G–l所示。我们还研究了高低脂代谢组中细胞间通讯的变化。高脂代谢组的细胞间相互作用的数量和强度也显著增加。同时,一些与肿瘤增殖和进展相关的信号通路,如NOTCH、APP和CEACAM,在高脂代谢组中也显著激活(附加文件1:图S7)。
图8:高ERS组和低ERS组之间的细胞间通讯分析。(A)高ERS组和低ERS组中由单个信号通路介导的细胞相互作用的数量和强度。(B)免疫细胞和肿瘤细胞之间通讯数量和强度的圆形图。(C)排名条形图显示了高ERS组和低ERS组中互动网络的信号轴。红色标记的信号通路在低ERS组中更丰富,黑色标记的信号通路在两组中同样丰富,绿色标记的信号通路在高ERS组中更丰富。(D)细胞-细胞通讯数量和强度的热图。蓝色表示与对照组相比,高ERS组的细胞间通讯减少,而红色表示细胞间通讯增加。(E)单个信号轴介导的细胞间通讯改变的气泡图,横轴显示启动和接收信号的细胞类别,纵轴显示信号通路的受体-配体对。(F)热图显示了每个细胞群的整体(流出和流入)信号流。低ERS组和高ERS组的(G,H)MIF信号通路、(I,J) SPP1信号通路和(K,L )APP信号通路。
8.基于单细胞转录组的代谢重编程分析
使用UCell R包对PDAC单细胞数据集的分析揭示了所有细胞亚型中活跃的ERS信号,特别是在上皮细胞中。此外,ERS的下游适应性途径,如未折叠蛋白反应,在所有细胞亚型中都表现出显著的激活。同时,脂质代谢相关途径,包括脂肪酸代谢、胆固醇稳态和胆汁酸代谢,在各种细胞亚型中显著富集,在上皮细胞中观察到显著富集。值得注意的是,在不同的PDAC细胞亚型中,DNA损伤没有明显的差异。与转移、干细胞和增殖相关的恶性肿瘤相关基因组在上皮细胞、组织干细胞、其他基质细胞和巨噬细胞中表现出更高的富集分数(图9A)。为了进一步阐明高和低ERS和脂质代谢之间的代谢变化,我们通过scMetabolism R package研究了代谢途径。除了苯丙氨酸代谢、牛磺酸和次牛磺酸代谢,来自原发性肿瘤细胞的大多数代谢途径在高ERS和脂质代谢中都被激活,例如嘌呤代谢、嘧啶代谢、类固醇生物合成、氮代谢和脂肪酸生物合成(图9B,D)。肝转移细胞中的大多数代谢途径在高ERS和高脂质代谢组中也显著上调,除了氧化磷酸化、鞘糖脂生物合成和叶酸形成的一个碳库(图9C,E)。在原发组和肝转移组中,以上皮细胞为代表的肿瘤细胞和以T细胞为代表的免疫细胞的代谢变化也是显著的(图9F,G)。
图9:基于单细胞RNA_seq数据的代谢变化分析。(A)胰腺癌单细胞数据集中与ERS、脂质代谢和恶性行为相关的信号通路的富集强度。(B,C)高、低ERS组原发性和肝转移细胞中的代谢重编程通路。(D,E)原代和肝转移细胞中高和低脂质代谢组的代谢重编程途径。(F)原发性和肝转移组上皮细胞的代谢变化。(G)原发性和肝转移组中T细胞的代谢变化。
9.ERS_脂质相关枢纽基因表达和预后价值的验证
在这项研究中,通过机器学习算法的组合,鉴定了包含7个基因的具有预测意义的ERS_ 脂质特征。值得注意的是,在这些基因中,SOD2、P4HB和TNFSF10被鉴定为与胰腺癌不良预后相关的枢纽基因。为了进一步验证ERS_脂质特征的预测价值,进行了实验验证以评估三个风险基因的表达水平和预后相关性。单细胞测序数据表明SOD2和P4HB在各种细胞群中广泛表达,TNFSF10主要表达于上皮细胞,APOE主要表达于巨噬细胞和一小部分基质细胞。NPC1L1、RAP1GAP和ADH1C在不同细胞群体中表现出相对较低的表达水平(图10A)。qPCR结果显示,与HPNE相比,SOD2和TNFSF10在PANC1、CAPAN1、BXPC3和BXPC3-LMT细胞系中的表达升高。P4HB的表达在PANC1和CAPAN1中增加,在BXPC3中减少,而在BXPC3-LMT中显著上调(图10B)。通过IHC检测3个中枢基因的蛋白质表达,以确定PDAC组(n=80)和正常组(n=80)之间的显著差异。PDAC组SOD2总阳性率为75%(60/80),正常组为63.75%(51/80)。PDAC组P4HB总阳性率为96.25% (77/80),正常组为100%(80/80)。TNFSF10在正常组中显示出95%(76/80)的总阳性率,在PDAC组中显示出100%(80/80)(图10C)。PDAC组中SOD2和TNFSF10的阳性面积显著高于正常组,而P4HB的阳性面积无显著变化(图10D)。然而,P4HB主要在正常组织的腺泡细胞中表达,与肿瘤组织相比,在胰腺导管细胞中观察到明显较低的表达水平。此外,组织中每个蛋白质的阳性面积之间的相关性并对35例有完整随访资料的患者进行无进展生存期检查,揭示了PDAC患者中SDO2、P4HB和TNFSF10表达水平与预后之间的负相关(调整后的p值< 0.05,图10E)。

图10:枢纽基因表达水平和预后相关性的验证。(A)单细胞数据集中ERS_脂质特征的基因表达水平。(B)SOD2、P4HB和TNFSF10的相对RNA表达。(C,D)使用调整p值的多重测试,通过免疫组织化学染色检测80对PDAC肿瘤组织和非肿瘤组织中SOD2、P4HB和TNFSF10的蛋白表达水平。(E)PDAC hub基因表达水平与预后的相关性分析。ns调整后p值> 0.05, *调整后p值< 0.05, **调整后p值< 0.01, ***调整后p值< 0.001, ***调整后p值< 0.0001。
讨论
内质网稳态在调节细胞功能和生存能力中起着关键作用。ERS主要表现为错误折叠和未折叠蛋白的堆积,可通过ATF4和NRF2促进抗氧化反应,降低氧化应激,促进肿瘤转移。一些研究表明,癌细胞中的ERS可以调节T细胞、树突状细胞、自然杀伤(NK)细胞等的功能,协调各种免疫逃逸机制以及介导肿瘤生长和转移。内质网在一定程度上调节脂质的合成代谢和分解代谢以及脂质的分布。脂质代谢重编程和ERS都可以与其他细胞功能相互作用,促进疾病的发展。
胰腺癌是高度转移性的,肿瘤转移是一个复杂的过程,由肿瘤细胞的内在特性和肿瘤细胞与肿瘤微环境中的其他免疫细胞、基质细胞和细胞外基质之间的串扰的组合驱动。PDAC的特点是复杂的肿瘤微环境,是免疫浸润最少的癌症之一。肝脏不仅是PDAC病例远处转移的主要场所,也是代谢的主要场所。代谢重编程和肿瘤免疫微环境的异质性在肿瘤发展和肝转移中均起重要作用。目前,驱动PDAC肝转移的分子机制尚未完全阐明,需要进一步研究,以有助于开发相应的治疗方法和改善PDAC患者的预后。
本研究基于生物信息学和机器学习方法,筛选出ERS和脂质代谢相关基因以及肝转移基因,并开发了一个新的7个基因PDAC患者预后模型,为PDAC肝转移患者的诊断和预后提供了一个潜在的生物标志物。单细胞转录组分析结果显示,与原代上皮细胞相比,肝转移上皮细胞中细胞周期、嘌呤代谢、嘧啶代谢和代谢途径上调,提示PDAC肝转移恶性进展。预后模型在测试集和TCGA、ICGC队列中得到验证。结果表明,在预测患者生存时间方面,风险评分比临床特征(如年龄、性别和分期)具有更好的作用。单变量和多变量Cox回归分析也表明,在PDAC,风险评分可以作为一个独立的预后指标。与之前发表的七个模型进行比较,包括广泛的代谢信号、缺氧信号、免疫相关信号、铜下垂信号、铁下垂信号、胆固醇代谢相关信号和涵盖各种研究方向的多组学信号,我们发现新的ERS_脂质特征在PDAC的预后准确性和稳健性方面表现出显著的优势。这突出了机器学习综合筛选方法的优越性,并强调了ERS_脂质在PDAC的发生和发展中的实质性作用以及预后潜力。高风险和低风险亚组之间的进一步基因富集分析也表明,在高风险组中,癌症中的途径增加,并且肿瘤的标志与风险评分显著相关。高风险组患者倾向于具有更大的TMB,这为该预后模型的准确性提供了证据,并表明具有高风险评分的患者具有更高的遗传异质性。药敏分析发现,高、低风险组患者对不同药物的敏感性差异显著,可为临床用药提供一定的指导。
筛选出的7个预后基因分别是APOE、ADH1C、RAP1GAP、NPC1L1、TNFSF10、SOD2和P4HB,其中APOE、ADH1C、RAP1GAP和NPC1L1的基因组合是PDAC预后的保护性因素,而TNFSF10、SOD2和P4HB的基因组合是其预后的危险因素。这些模型基因的差异表达水平和预后值也是显著的(图10和附加文件1:图S8)。载脂蛋白E(APOE)是一种参与脂蛋白代谢和胆固醇转运的分泌蛋白。已经证明APOE在调节MDSC的丰度和抗肿瘤免疫中起作用。Pencheva等人也报道了APOE分别通过吸引肿瘤细胞LRP1受体和内皮细胞LRP8受体来抑制黑色素瘤的侵袭和血管生成。乙醇脱氢酶1C(ADH1C)是乙醇脱氢酶家族的一员,代谢乙醇、脂肪醇和脂质过氧化产物。ADH1C与肝癌和肺腺癌的不良预后有关。在结直肠癌中,ADH1C充当肿瘤抑制基因。关于ADH1C与多种肿瘤相关性的许多研究结果是重要的,但不一致。ADH1C在胰腺癌中的作用很少报道,需要进一步研究。肿瘤抑制基因RAP1GAP,因其调控区高度甲基化而失活,可引起甲状腺肿瘤。RAP1GAP的沉默促进了子宫内膜样腺癌细胞的迁移和侵袭。NPC1L1是一种胆固醇转运蛋白,在胆固醇的肠道吸收中起着至关重要的作用。NPC1L1促进维生素E的吸收,能与脂质过氧化自由基相互作用,防止氧化应激。TNFSF10在调节乳腺癌细胞转移中具有抑制功能,但有报道称TNFSF10在体外可增强PDAC细胞的侵袭,在体内可增加胰腺肿瘤的远处转移。Huang等人用紫衫利尔或衣霉素处理巨噬细胞以诱导ERS反应,并观察到TNFSF10表达上调。在Jiang等人的另一项研究中,注意到TRAIL促进细胞因子表达并激活ERS依赖性NF-κB途径。这些发现共同表明肿瘤坏死因子F10和ERS有密切联系。超氧化物歧化酶2(SOD2)是一种在活性氧信号传导中起重要作用的酶。该研究发现,沉默SOD2显著降低了PDAC的生长和转移特性,如迁移和集落形成能力。此外,抑制SOD2显著促进ERS,表明SOD2抑制可能通过促进氧化应激进一步增强ERS。脯氨酰4-羟化酶β多肽(P4HB)是一种具有氧化还原酶活性的内质网分子伴侣蛋白。尽管在大量RNA-seq数据集中观察到P4HB的下调,但在单细胞转录组数据集中它的上调是明显的。此外,本研究的实验结果表明,在PDAC,高P4HB表达与不良预后相关。LGALS9和P4HB之间的高度活跃的相互作用也表明它们在促进PDAC中起着至关重要的作用。
高、低风险组免疫景观显示,高风险组CD8+ T细胞、M1巨噬细胞和NK细胞等抗肿瘤免疫细胞以及调节性T细胞浸润水平降低,而高风险组活化CD4+ T细胞和Th2 CD4+ T细胞浸润水平上调。这表明PDAC肿瘤微环境中免疫浸润细胞的变化非常复杂,包括抗肿瘤相关免疫细胞的减少,负性免疫调节细胞的增加,以及正性免疫细胞的增加。通过对肿瘤微环境中免疫浸润细胞的分析和免疫功能的分析,我们发现免疫抑制的影响在高风险组中更加明显。通过进一步研究高ERS组和低ERS组的细胞间通讯,我们发现在高ERS组,上皮细胞与单核细胞、巨噬细胞和T细胞的相互作用减少,但整体而言细胞间通讯的数量和强度增加,包括三个有趣的信号通路,分别是MIF、APP和SPP1信号通路。MIF受体由与信号转导CD44偶联的配体结合CD74信号复合物组成。当配体与MIF结合时,可以启动下游信号转导,以促进炎症和细胞存活。APP可能通过sAPP信号促进胰腺癌细胞的生长,并作为胰腺癌的新治疗靶点。SPP1+巨噬细胞在肿瘤组织中的富集与淋巴细胞浸润呈负相关,表明存活率差且对免疫疗法有抗性,这表明复杂的细胞间通讯可以激活肿瘤微环境中的下游信号通路,从而在肿瘤进展中发挥重要作用。此外,在肝转移组中,在T细胞中观察到牛磺酸代谢的显著降低。研究表明,增加牛磺酸水平可以增强效应和记忆T细胞的反应,而抑制牛磺酸的摄取可能会诱导T细胞死亡。这些发现与我们的研究结果一致,表明胰腺癌肝转移过程中代谢重塑介导的T细胞免疫耐受现象。在原发性肿瘤的高ERS组中牛磺酸和低牛磺酸代谢显著上调,而在肝转移细胞中则相反。众所周知,牛磺酸在维持正常的电子传递链、增强抗氧化反应、增加膜稳定性和防止钙积累方面发挥着重要作用。这些结果表明,在胰腺癌肝转移过程中,肿瘤细胞内可能发生ERS和稳态失衡的适应性变化。
结论
总之,我们的研究基于机器学习方法构建了一个新的预后模型,以探索和阐明ERS和脂质代谢对胰腺癌预后、免疫微环境和代谢的重要影响。












