大家上午好!今天小编和大家分享一篇23年7月发表在Journal of Translational Medicine(IF:7.4)杂志的文章《Single-cell analysis of white adipose tissue reveals the tumor-promoting adipocyte subtypes》。作者通过生物信息学分析与临床数据的结合,分析了几种癌症相关的脂肪细胞亚型,为未来治疗的关键预后预测指标和潜在靶点提供了理论基础。
背景:
脂肪组织是一种高度代谢的器官,可调节体内的能量平衡。在癌症的背景下,脂肪组织可以在肿瘤附近发现,肿瘤可以在脂肪组织附近生长或转移到脂肪组织,这有助于形成独特的肿瘤脂肪微环境(TAME)。肿瘤脂肪微环境的特征是脂肪细胞富集,被认为是支持癌症进展的特殊生态系统。然而,TAME中脂肪细胞的异质性和多样性知之甚少。
方法:
我们对小鼠和人白脂肪组织(WAT)中的脂肪细胞进行了单细胞RNA测序分析,以评估它们作为预后因子的潜力。通过在临床样本中进行体外功能测定和免疫组织化学(IHC)来验证乳腺癌中典型脂肪细胞亚型的肿瘤促进作用。
研究结果:
1 小鼠和人类WAT的单细胞图谱
为了全面了解TAME的细胞组成,我们编制了小鼠和人类WAT样品的单细胞转录图谱。图谱包括48个人类样本(19个VAT样本和29个SAT样本)的scRNA-seq数据和46个小鼠样本(18个VAT样本和28个SAT样本)的snRNA-seq数据。在对每个样本进行严格的质量过滤后,将数据集整合为四组:小鼠VAT(mVAT)、人类VAT(hVAT)、小鼠SAT(mSAT)和人类SAT(hSAT)。接下来,对数据集进行MNN集成,以减少批量效应。所得到的质量控制的VAT单细胞图谱包括121349个单核和53152个单细胞,基于典型谱系标记进行将他们聚类,并使用UMAP图进行可视化。聚类分析和标记基因注释揭示了不同的细胞簇,包括成熟脂肪细胞、ASPCs、内皮细胞、上皮细胞、间皮细胞和免疫细胞(T细胞、B细胞和髓细胞)。在SAT的单细胞图谱中,低质量过滤留下158977个单核和144965个单细胞。UMAP和标记基因注释了主要的细胞群,包括成熟脂肪细胞、ASPCs、血管细胞(周细胞和内皮细胞)、上皮细胞、间皮细胞和免疫细胞(T细胞、B细胞和髓细胞)。mVAT、hVAT、mSAT和hSAT图谱中细胞类型的分布没有表现出显著差异。
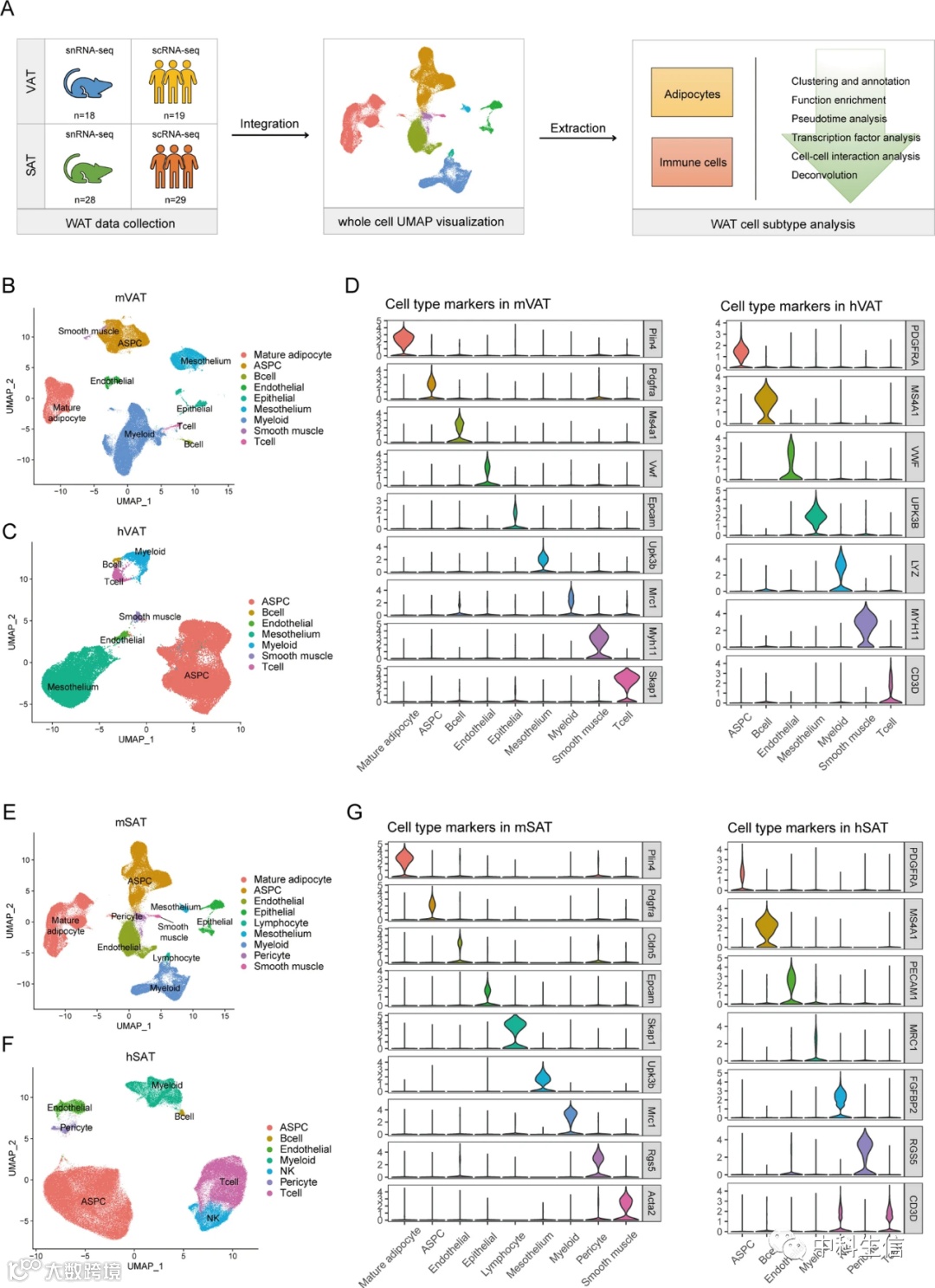
2 小鼠和人WAT脂肪细胞群的景观
接下来,我们对VAT和SAT中的脂肪细胞群(包括ASPC和成熟脂肪细胞)进行了详细分析。先前对小鼠的研究表明,ASPC可分为三个群体。第一个群体是脂肪干细胞(ASCs),是自然界中最像干细胞的群体,其标志是干细胞相关基因的表达,如Pi16、Dpp4和Adamts16。第二个群体,前脂肪细胞(PreAs),表达几种脂肪生成相关基因,如Lpl和Plin2。前脂肪细胞处于细胞状态,致力于脂肪生成。第三类群体是脂肪生成调节因子(Aregs),由F3(编码CD142)的表达定义,能够抑制其他ASPC的成脂分化。成熟的脂肪细胞被认为在功能上基本一致,尽管最近的一些研究并不认同这一观点。
3 VAT包含不同的脂肪细胞亚群
在mVAT中,我们检测到七个不同的ASPCs亚群(以Pdgfra标记)和三个成熟脂肪细胞亚群(由Plin4标记)。基于先前的结论和新生成的基因表达谱,我们将七个ASPC亚群注释为mA1:Pparg+PreA(Pparg,Fgf10,Frem1)、mA2:Fabp4+PreA)(Fabp4,Cd36)、mA3:Dpp4+ASC(Dpp4)、mA4:Rgs6+ASC(Rgs6,Adamts16)、mA5:B2m+ASC(Ly6a,B2m)、mA6:Fmo2+Areg(Fmo2和Gria4)和mA7:Mgp+Areg(Mgp和Clec11a)。我们还通过上调其标记基因的表达,鉴定了成熟脂肪细胞的三个亚群,即Cfd+、Lep+和Prune2+成熟脂肪细胞。与小鼠脂肪细胞相比,人类脂肪细胞表现出更大的个体变异性和更少的异质性。人类脂肪细胞的亚聚集显示了三个群体,包括hA1:CIDEC+PreA、hA2:PTN+PreA和hA3:DPP4+ASC。未检测到Aregs和成熟脂肪细胞。
众所周知,肥胖会严重影响脂肪细胞的丰度和基因表达。因此,研究了高脂肪饮食(HFD)和正常对照饮食(NCD)mVAT样本之间每个亚群的分布。比较分析显示,HFD诱导的肥胖导致mA1、mA2和mA7细胞的相对数量增加,而mA3和mA6细胞的相对数目减少。值得注意的是,成熟脂肪细胞比ASPCs更容易受到饮食的影响,因为HFD喂养后Cfd+脂肪细胞的相对比例大大降低,而Lep+脂肪细胞则观察到相反的趋势。值得注意的是,大多数样本中都存在所有脂肪细胞亚群,这表明这些亚型是稳定的,不反映样本特异性变化。
一个关键的问题是脂肪细胞亚群是否具有不同的功能。为了了解这个问题,我们首先通过进行通路富集分析来探索每个亚群的功能。成熟脂肪细胞的三个亚群具有相对较少的特异性标记,并且它们的特征是通用的。为了进行更详细的分析,我们重点研究了mA1–mA7亚群。mA1和mA2都表达高水平的成熟脂肪细胞标记基因,但它们的功能不同。mA1亚群对Hippo信号通路具有独特的富集作用,表明脂肪细胞处于去分化状态。已知Hippo通路介导脂肪组织纤维化中脂肪细胞从能量储存向细胞外基质重塑的转变。相比之下,mA2脂肪细胞的特征是脱铁、细胞凋亡、胆固醇代谢和PPAR信号通路显著富集。
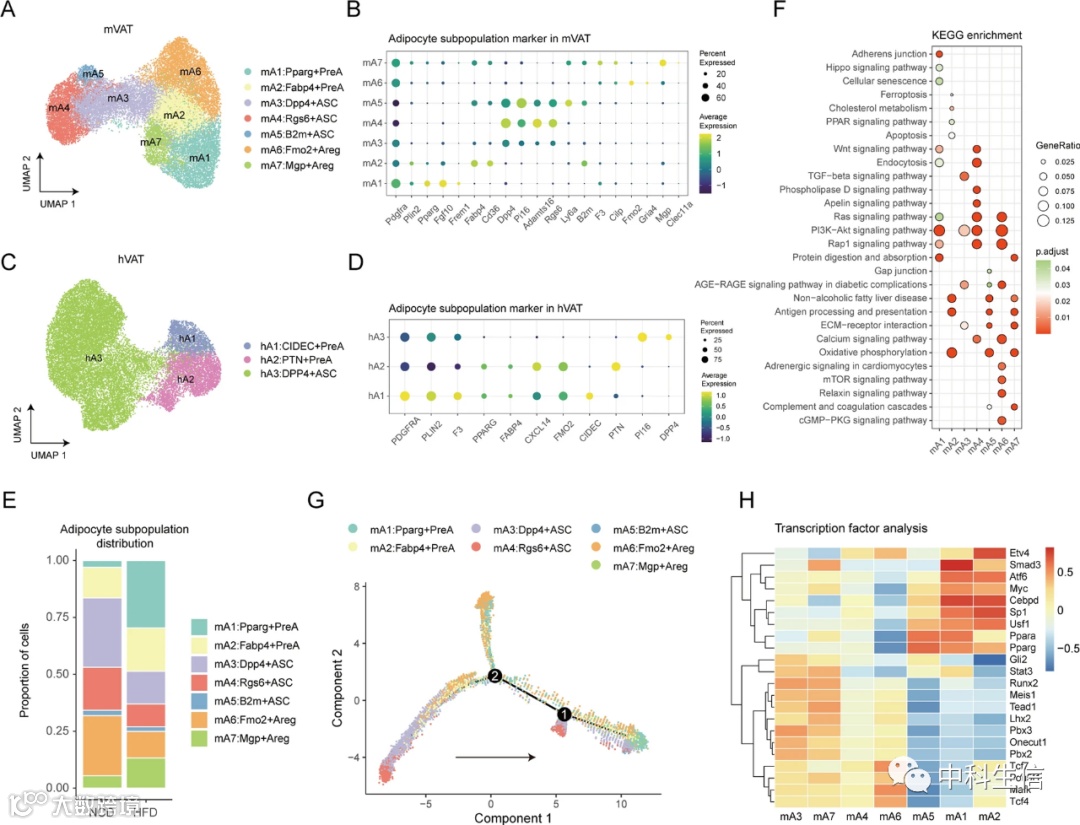
4 SAT包含不同的脂肪细胞亚群。
按照类似的程序,在mSAT中鉴定了六个不同的ASPCs亚群和两个成熟脂肪细胞亚群。值得注意的是,除了mVAT中的mA7和Prune2+成熟脂肪细胞外,所有脂肪细胞亚群都存在于mSAT中,这表明这些亚型的稳定性。基于不同的基因表达模式还鉴定了四种人类脂肪细胞亚群,即hA1:DEPP1+PreA、hA2:KCND2+PreA、hA3:DPP4+ASC和hA4:ADIPOQ+脂肪细胞(Adi)。表达APOD和F3的hA1和hA2被归类为PreA。hA1特异性表达DEPP1,hA2表达KCND2和KAZN。根据PI16和DPP4的表达,hA3被鉴定为ASC。有趣的是hA4亚群,其通常表现出与成熟脂肪细胞相关的基因表达模式,如ADIPOQ、LPL和FABP4。样品与正常和肥胖状态的比较显示,HFD诱导的肥胖导致mA1和mA4细胞的相对数量显著增加,同时mA2和mA5细胞的比例显著降低。此外,观察到成熟脂肪细胞中脂肪细胞亚型的饮食依赖性变化。
另外,一个重要的问题是mSAT和mVAT之间脂肪细胞亚群的功能特性是否一致。为了解决这个问题,对每个亚群的标志物进行了通路分析。mA1在FcγR-介导的吞噬作用中显著富集,而mA2在细胞凋亡、TNF信号通路和IL-17信号通路中富集。在包括mA3-5在内的ASCs中,mA4亚群的特征在钙信号通路、间隙连接和apelin信号通路显著富集。mA5在抗原处理和呈递方面具有显著的富集,表明其具有免疫相关特征。mA6是唯一的Areg亚群,在松弛素信号通路和Wnt信号通路中高度富集。接下来,对脂肪细胞亚群进行了细胞轨迹分析。结果表明,mA5是mSAT中最具干细胞样的亚群。mA5细胞可以通过第一分支点转变为mA3和mA4细胞,然后这些细胞可以通过第二分支点分化为mA6细胞。最终,它们产生mA1和mA2-PreA亚群。最后,对这些亚群进行了TF分析。在结果中,mA1显示出相对特定的转录状态。Bhlhe22、Zeb2和Zfp263在mA1亚群中具有独特的活性。此外,Atf6、Esr1和Rreb1在mA2亚群中富集。为了进一步了解每个亚群的独特功能,我们对DEG进行了分析,随后进行了KEGG信号通路富集,揭示了三个亚群之间的功能差异。例如:hA4亚型在PPAR信号通路、脂肪酸代谢、AMPK信号通路、丙酸代谢胰岛素信号通路和脂肪细胞脂解调节中富集显著。

总之,本研究确定了小鼠中全范围的脂肪细胞亚型,并介绍了人类每种脂肪细胞亚型的分子谱。这些发现为TAME中各组分之间的相互作用提供了有价值的见解,并为进一步研究个体亚群在代谢疾病中的作用提供了基础。
5 脂肪细胞亚群与免疫细胞之间的信息交流
脂肪细胞亚群与来自TAME内成分的不同介质进行信息交流,尤其是免疫细胞。因此,我们从mVAT和mSAT中提取了免疫细胞群,以进一步了解脂肪细胞和免疫细胞之间复杂的相互作用。mVAT(n = 34698)产生了9个亚群。我们进行了差异表达分析,并将三个亚群注释为巨噬细胞(表达Adgre1和Mrc1),而其余六个亚群则注释为单核细胞(表达Fn1)、树突状细胞(表达Flt3)、中性粒细胞(表达Csf3r和Klra2)、肥大细胞(表达Cpa3和Kit)、T细胞(表达Themis和Skap1),和B细胞(表达Ms4a1和Ighm)。为了注释巨噬细胞亚群,我们将其表达谱与最近的巨噬细胞分类研究进行了比较。发现,Lgals3+巨噬细胞亚群表达高水平的Lpl和Plin2,这与HFD喂养期间出现的脂质相关巨噬细胞(LAMs)一致,并在清除死亡脂肪细胞中发挥作用。
对喂食NCD或HFD的小鼠mVAT样本中每种细胞类型的频率的分析显示,HFD诱导的肥胖小鼠样本中Lgasls3+巨噬细胞的比例增加,从几乎不存在增加到最丰富的亚群。相反,在HFD小鼠样品中,Folr2+巨噬细胞、Cd163+巨噬细胞、单核细胞、B细胞和T细胞的比例降低。鉴于VAT中免疫细胞类型的分布和组成发生了重大转变,我们接下来探讨了这些变化在多大程度上影响了细胞通讯。然后,我们研究了所有免疫细胞和脂肪细胞中配体和受体之间的相互作用。我们发现,在Folr2+巨噬细胞中,免疫细胞和脂肪细胞亚群之间的配体-受体配对数量明显更大,但Lgals3之间的相互作用强度 + 巨噬细胞和脂肪细胞,特别是mA1和mA3更强。
按照类似的步骤,我们对9个免疫细胞亚群进行了注释,这些亚群与mVAT样本中注释的亚群一致。然而,对正常和HFD诱导的肥胖状态之间的免疫细胞组成的比较显示,Lgals3+巨噬细胞和Folr2+巨噬细胞的比例降低。我们发现,在所有脂肪细胞亚群中,免疫细胞和脂肪细胞之间的配体-受体配对数量在mA5和mA6中显著更大,尤其是mA5:B2m+ASC亚群。在mA4/mA5和Lgals3+巨噬细胞之间以及在mA1和Cd163+巨噬细胞之间检测到强信号。

我们的发现与先前的研究一致,表明巨噬细胞是WAT的主要免疫细胞类型。此外,我们发现Folr2+巨噬细胞在内脏和皮下脂肪组织中的作用相似,但Folr2之间的相互作用+ 巨噬细胞和脂肪细胞并不紧密。
6 反卷积分析预测了癌症相关脂肪细胞亚型
为了评估hVAT脂肪细胞亚型,我们使用单细胞特征估计了胰腺癌症(PAAD)和肾透明细胞癌(KIRC)患者的个体亚型比例。TCGA的样品根据个体亚型比例分为四组,包括hA1、hA2、hA3和混合物。混合物组包括具有多种亚型成分的样品。PAAD队列分别包含36.46%、46.42%、7.73%和9.39%的hA1、hA2、hA3和混合物组。hA3组与胰腺癌症中的低OS相关。此外,为了验证每种亚型的独立影响,我们根据每种亚类型的估计得分对样本进行分组,并进行生存分析。在PAAD队列中,hA2亚型与预后相关,而hA3与不良预后相关。在KIRC队列中,hA1是优势亚型,在52.16%的样本中发现,16.78%、7.81%和23.36%的样本表现出hA2、hA3和混合物。其中,与hA1组相比,hA2组的OS较差。在每种亚型的单独验证中,hA1亚型与良好的预后相关,而hA2和hA3与不良预后相关。
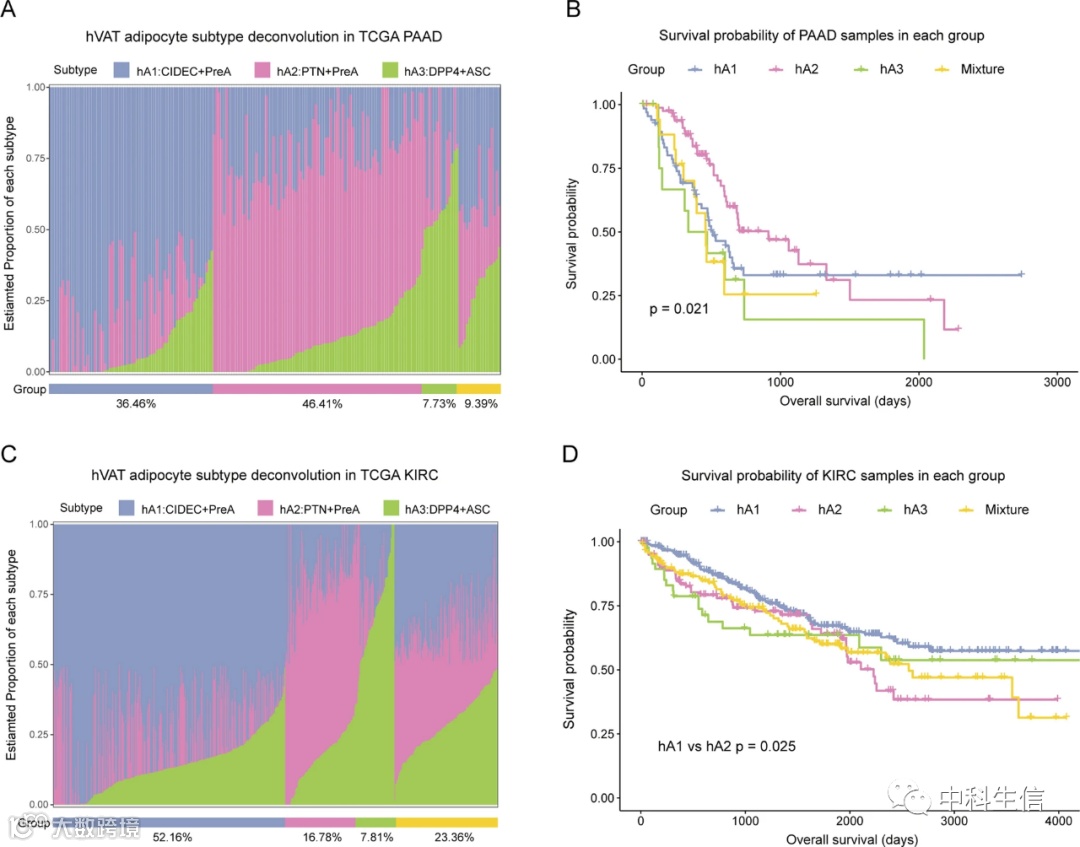
在hSAT脂肪细胞亚型的情况下,选择来自TCGA的黑色素瘤和癌症(BRCA)队列作为模型。根据相同的规则,所有黑色素瘤病例被分为五组,包括hA1、hA2、hA3、hA4和混合物。与hA1组相比,hA4组的生存率较低(p = 0.0032)。在每种亚型的单独验证中,hA1亚型与良好的预后相关,而hA3和hA4亚型与不良预后相关。同样,所有癌症病例被分为五组。对于生存率分析,hA4组与最差生存率相关(p < 0.0001)。hA4亚型在黑色素瘤和癌症队列中具有显著最差的预后。因此,我们推测了靶向癌症hA4亚型的潜在药物。我们发现hA4亚型对SCH772984、曲美替尼、selumetinib、PD0325901、ulixertinib、米托蒽醌和foretinib等药物更敏感,对sapitinib、afatinib、lapatinib、OSI-027、ULK1_4989、acetaxasm和ipatasertib等药物更具耐药性。hA1亚型具有与hA4亚型相似的药物敏感性状态。

总之,我们提供了在四种典型的癌症类型中识别CAA亚型的见解。DPP4+ASC亚型与PAAD和KIRC患者的不良预后有关,而ADIPOQ+Adi亚型与黑色素瘤和BRCA患者的不良生存率有关。目前的研究结果表明,曲美替尼、selumetinib和ulixertinib可能是靶向癌症患者hA4亚型的有用药物。
7 AdipoR1和AdipoR2介导的乳腺癌症发展
上述分析表明,肥胖和糖尿病患者中ADIPOQAdi亚型的比例升高,并且与乳腺癌和黑色素瘤患者的低生存率有关。为了进一步研究其调控机制,我们重点关注脂联素(由ADIPOQ编码)受体,特别是AdipoR1和AdipoR2(由ADIPOR1和ADIPOR2编码)。
首先,我们在DepMap的癌细胞系百科全书(CCLE)数据集中筛选了乳腺癌细胞系。结果表明,MCF7和ZR-751细胞系对ADIPOR1和ADIPOR2均具有高表达。然而,在CRISPR筛选获得的基因依赖性数据集中,细胞系MDA-MB-231的存活/增殖,取决于ADIPOR1。因此,我们选择了MDA-MB-231,MCF7和ZR-751细胞系进行体外实验。我们的蛋白质印迹分析结果表明,sh-2在降低AdipoR1的蛋白质水平方面更有效,而sh-3在降低AdipoR2的蛋白质水平方面更有效。为了验证AdipoR1 / 2在乳腺癌细胞活力中的作用,我们在三种细胞系中进行MTT测定。结果表明,AdipoR1/2的敲低降低了MDA-MB-231细胞系中的增殖,但MCF7和ZR-751细胞系中的增殖却没有减少。因此,我们选择了MDA-MB-231细胞系进行下游分析。
流式细胞术分析显示,敲低AdipoR1/2促进了MDA-MB-231细胞系中的细胞死亡。然后我们研究了AdipoR1/2对乳腺癌症细胞侵袭性的影响。Transwell测定结果表明,在敲低AdipoR1或AdipoR2后,细胞侵袭性被显著抑制。此外,我们在临床癌症样本中验证了我们的结论。我们分析了113例术前癌症患者的样本,并进行IHC以评估AdipoR1和AdipoR2的水平。IHC结果显示,不同患者的AdipoR1和AdipoR2水平不同。然后,我们根据估计的IHC评分将患者分为AdipoR1/2阴性组和AdipoR11/2阳性组。两组患者的生存率分析显示,AdipoR2与癌症患者RFS差显著相关(P = 0.011)。此外,AdipoR1也显示出与RFS的负相关性,但这种相关性并不显著。我们还使用METABRIC乳腺癌症数据集验证了这一发现。ADIPOR1和ADIPOR2的表达与不良OS显著相关。最后,我们获得了83例术前癌症患者的血清样本,发现超重组(BMI:25-29.9)的脂联素水平低于正常组(BMM:18.5-24.9),但差异不显著(p = 0.13)。

总之,我们的研究结果为AdipoR1和AdipoR2在体外肿瘤增殖和侵袭中的阳性调节提供了证据,并在IHC样本和公共数据集中证明了AdipoR1/2与低生存率之间的关联。这些结果表明,ADIPOQ+CAA通过AdipoR1和AdipoR2发挥肿瘤促进作用。



