大家上午好!今天小编和大家分享一篇22年12月8日发表在Frontiers in Endocrinology(IF:5.2)杂志的文章《Machine learning to construct sphingolipid metabolism genes signature to characterize the immune landscape and prognosis of patients with uveal melanoma》。研究从TCGA和GEO数据库中筛选出4个与葡萄膜黑色素瘤(Uveal melanoma,UVM)患者预后显著相关的鞘脂代谢基因(SMGs),并通过逐步多因子cox构建了4个SMGs的预后模型。CIBERSORT等平台分析了高危和低危患者的4-SMGs免疫浸润水平。ImmuCellAI和TIP门户网站评估了4个SMG基因对UVM患者免疫治疗和免疫检查点阻断(ICB)反应的预测。
背景:
葡萄膜黑色素瘤(UVM)占所有眼部黑色素瘤的85%,是成人最常见的原发性眼内恶性肿瘤。大约85%的肿瘤病例起源于脉络膜,其余病例起源于虹膜(3-5%)和睫状体(5-8%)。超过50%的UVM患者发展为全身性转移性疾病,其中肝脏是UVM 中最常见的转移部位。此外,患者很少能通过手术获得良好的治愈效果。因此,UVM患者预后很差,5年死亡率为31%,15年死亡率为45% 。为了提高UVM患者的生活质量,需要新的预后生物标志物和分子靶点来预测UVM患者的预后,指导个体化治疗。
鞘脂类是生物膜结构的重要组成部分,维持着细胞膜的屏障功能和流动性。随着对动物和酵母的深入研究,鞘脂及其代谢物被发现是一类重要的生物活性分子,参与调节许多重要的信号过程,如细胞生长、分化、衰老和程序性细胞死亡。越来越多的证据表明,鞘脂代谢广泛参与了肿瘤的增殖、转移、血管生成和耐药性,并在肿瘤免疫微环境中起着关键作用。有研究认为鞘脂可能是一种潜在的肿瘤相关抗原,与UVM患者的肿瘤进化和肝转移密切相关,SMGs在UVM中的预后价值和肿瘤免疫微环境的作用尚不清楚。
因此,本研究旨在开发一种基于SMGs的新方法来准确预测预后和描述UVM患者的免疫状态,以实现疾病的精准治疗。
技术路线:
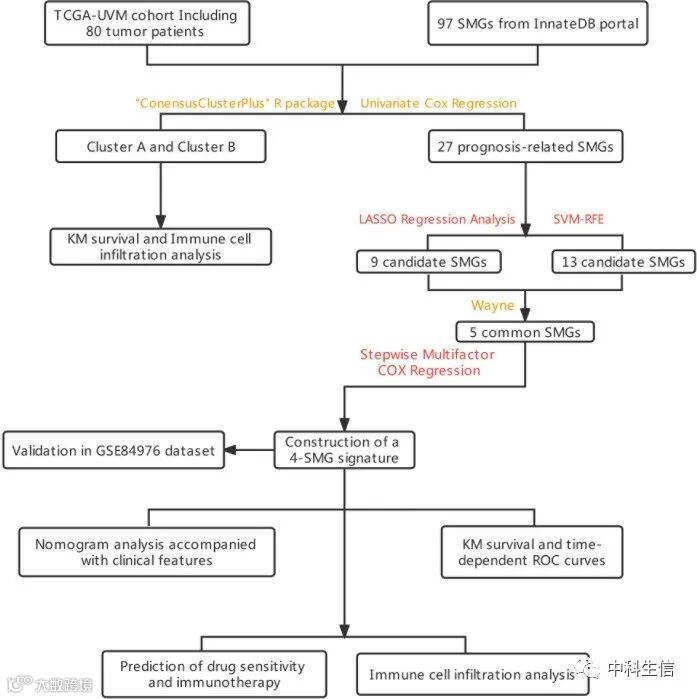
研究结果:
1.共识聚类确定了SMG的分子亚型
我们绘制了对应于共识矩阵的颜色编码的热图,发现当 k = 2时,它表现出高组内相关性和低组间相关性,这强烈表明将UVM患者分为两个亚型(簇 A和簇 B)是非常合适的(图2C)。为了确定不同组别患者生存预后的差异,根据 ClusterSurvival R 软件包计算组间 OS的差异。与B组患者相比,A组患者的生存预后有所改善(P < 0.001)(图2D)。根据不同的分组,A组和B组患者表现出显著的差异(图2E)。除此之外,我们进一步探讨了簇A,B 和 SMG之间的代谢差异,热图显示簇B在SMG中具有更高的表达差异和临床特征(图2F)。为了阐明潜在的生物学途径,我们进行了KEGG富集分析,并确定了与各种癌症相关途径的关系,如凋亡,转运蛋白,细胞粘着分子和造血细胞谱系(图2G)。我们使用 ssGSEA 算法计算了两个群组中的免疫细胞浸润水平。结果发现,与 A 组相比,B 组大多数免疫细胞的浸润水平较高(图2H)。根据研究结果,SMG 风险评分模型可将不同的免疫亚型分类,从而影响对免疫疗法的反应。此外,由于免疫检查点对于肿瘤免疫疗法的有效性非常重要,而且免疫检查点是肿瘤微环境(tME)的重要特征之一。我们研究了两组之间免疫检查点表达的差异,最终发现乙组患者的免疫检查点基因表达显着上调。基于上述分析,我们得出结论,乙组对免疫疗法具有更高的有效性和敏感性(图2I)。

2、4-SMG标记的构建和验证
我们使用两种机器学习方法来识别候选 SMG。对于 LASSO 回归分析,从27个具有显著预后特征的 SMG 中筛选出9个候选基因(图3A,B)。对于 SVM-RFE 算法,当特征数为13时,误差最小(图3C,D)。通过韦恩图获得了上述两种方法的五个相交基因(图3E)。最后,通过逐步多变量 Cox分析确定了4个 SMG 作为独立的预后因素,包括 ARSH,GBA2,GLA 和 GLB1。我们进一步探讨了这些4-SMG 的表达与风险评分之间的相关性,发现所有4-SMG 都与风险评分密切相关。其中,ARSH、 GBa2和 GLB1与风险评分有显著负相关,而 GLA 与风险评分则有显著正相关(图3F)。此外,我们计算了每个患者的预后风险评分,并根据评分中位数将 UVM 患者分为高风险组和低风险组。(图3G)显示4-SMG 在高风险和低风险组中的分布,ARSH,GBA2和 GLB1在高风险组患者中低表达,GLA 在高风险患者中高度表达。在 TGCA-UVM 队列中,UVM 患者的死亡率随着风险的增加而增加(图3H,I) ,低风险组的预后更好(P < 0.001)(图3J)。当基于一个风险模型时,高风险和低风险患者表现出显著的差异,并显示出明显的分离(图3L)。在 GSE84976队列中,我们显示了与 TCGA-UVM 队列相同的结果。UVM 患者的死亡率随着风险的增加而增加(图3M,N)。KM 生存分析显示低风险患者比高风险患者预后更好(P < 0.001)(图3O)。随时间变化的 ROC 曲线显示2年 AUC 为0.783,3年 AUC 为0.789,5年 AUC 为0.893,8年 AUC 为0.929,10年 AUC 为0.927(图3P)。PCA 分析显示,低风险和高风险患者表现出明显的差异,表现出明显的分离(图3Q)。基于这些结果,我们可以得出结论,我们的预测模型的建设是相当优越的。

3、 SMG 与UVM 患者的临床相关性及生存分析
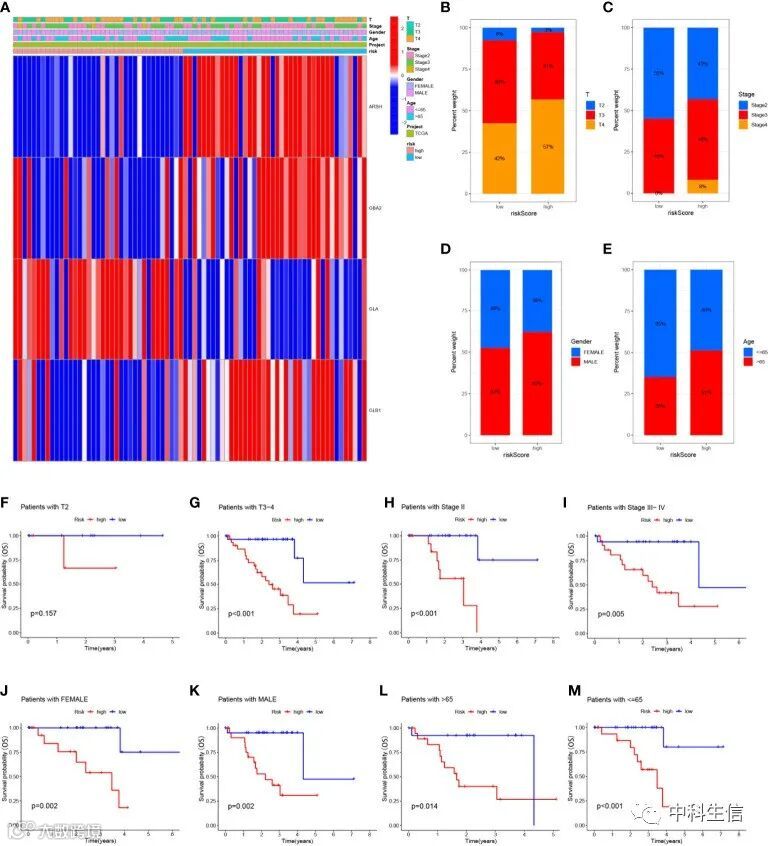
为了分析高风险组和低风险组与临床特征之间的相关性,根据临床特征,风险评分和4-SMG的表达绘制热图,热图显示在预后风险模型中鉴定的4-SMG 与年龄,性别,临床分期,T分期和所有UVM患者样本的风险评分 TCGA (图4A)。此外,我们进一步分析了高风险组和低风险组之间具有各种临床病理特征的患者比例的差异,发现SMG对具有不同临床病理特征的患者比例有显着影响(图4B-E)。为了更好地了解不同临床亚组患者的预后是否不同,进行进一步的生存分析。在所有亚组中,高危患者的生存时间明显短于低危患者(图4F-M)。目前确定的 SMG 风险模型似乎也能够根据其临床特征可靠地预测某些 UVM 亚组的预后。
4、结合临床特征建立列线图
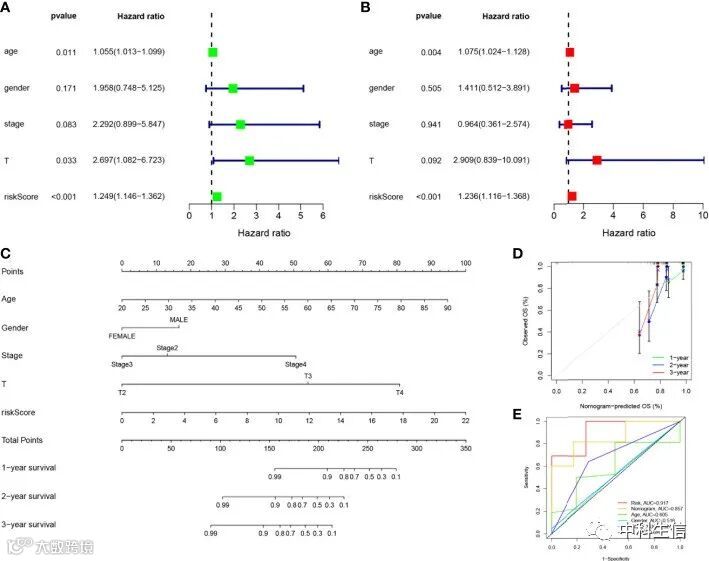
考虑到构建的风险模型与不良预后之间的强相关性,我们将 UVM 患者的 OS 及其临床特征结合在单变量和多变量 Cox 分析中,以确定我们基于4-SMG 构建的预后特征是否可以用作预后的独立预测因子。根据变量,年龄,阶段,性别,T 和风险评分的单因素分析结果,发现 UVM 患者的风险评分与预后显着相关(P < 0.001)(图5A)。同样,在多因素分析后,风险评分仍然是队列中最可靠和独立的预测因子(P < 0.001)(图5B)。为了扩展所构建的风险模型的临床应用和可用性,我们根据年龄、性别、临床分期、 T 分期和风险评分构建了 Nomgram 图,作为 UVM 患者1年、2年和3年预后生存概率的预测因子。因此,从模型结果中观察到,风险评分对预测 OS 的影响最大,表明基于 SMG 的风险模型可以更好地预测 UVM 的预后(图5C)。校准曲线还显示了一个更令人满意的共识之间的预测值和观察值的概率 OS 在1年,2年和3年(图5D)。再次比较 Nomgram,风险和常见临床病理特征,风险(AUC = 0.917)以及 Nomgram (AUC = 0.857)是 UVM 预后的更好预测因子,而不是年龄,性别,临床分期和 T 分期(图5E)。这意味着我们构建的 SMG 特征的预测性能明显优于其他临床特征。
5、SMG 的功能富集分析
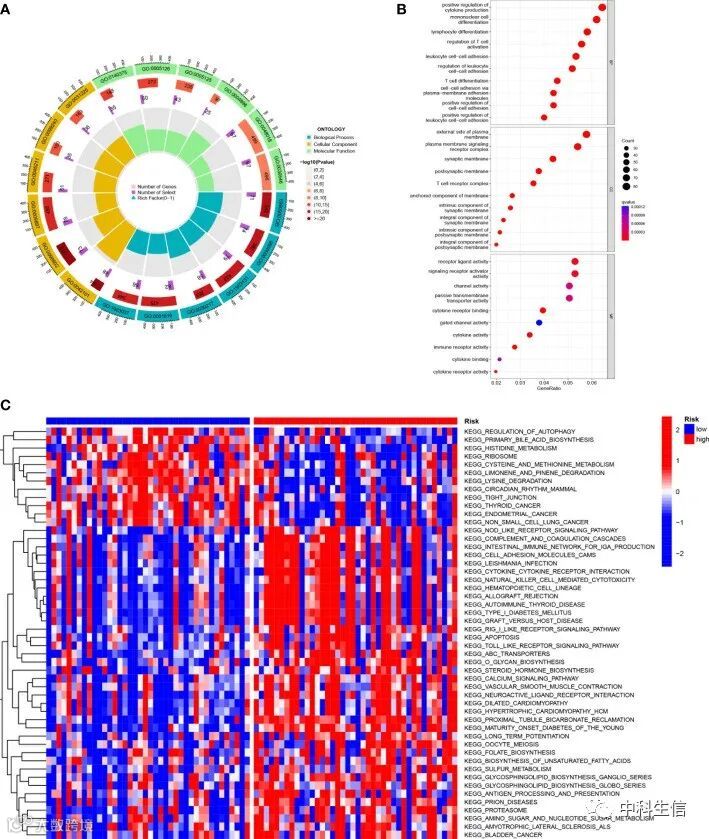
进行 KEGG 富集分析和 GO 功能分析以评估 UVM 中的差异基因,以阐明生物活性和信号通路与风险评分的相关性。阈值 FDR < 0.05和 P < 0.05用于选择显着富集的项目(图6A,B; 补充表3)。生物过程主要包括淋巴细胞和 T 细胞分化、白细胞粘附等。细胞成分主要包括胞膜信号转导变异受体复合体、突触膜内在成分和胞膜信号转导变异受体复合体。分子功能主要包括受体配体活性、免疫受体活性、细胞因子结合和信号受体活化剂活性。GSVA 分析发现发现富集分析结果与免疫反应之间有很强的相关性,因此我们对 UVM 患者的免疫状况进行了系统分析。
6、SMGs风险评分预测TME和免疫细胞浸润
首先,根据 XCELL,TIMER,QUANTISEQ,MCPCOUNTER,CIBERSORT,CIBERSORT-ABS和EPIC算法,我们探讨了风险评分与浸润性免疫细胞丰度之间的相关性,其中CD8 + T细胞,NK细胞浸润都与风险评分呈正相关(图7A)。然后,我们使用 CIBERSORT 算法独立评估UVM中高风险组和低风险组之间的免疫细胞浸润,结果显示高风险组中浆细胞、幼稚 B 细胞、单核细胞和肥大细胞的表达显着更高(图7B)。鉴于检查点免疫疗法的重要性,我们分析了高风险组和低风险组免疫检查点基因的表达。发现大多数免疫检查点基因在高危组中显着上调,包括 IDO1,CTLA-4,TIGIT,KIR3DL1,BTLA,CD28等(图7C) ,表明高危组患者可能具有更好的 ICB 疗效。我们对免疫功能的 ssGSEA 评分进行了比较,高风险组的多种免疫功能评分显着高于低风险组(图7D)。由于浸润性免疫细胞是 TME 的重要组成部分和特征之一,免疫细胞类型表达的改变导致 TME 组成的变化,因此我们分析了 UVM 样品的 TME 组成。结果显示,与高危组相比,低危组的免疫评分(P < 0.001) ,ESTIMATE 评分(P < 0.001)和基质评分(P < 0.001)较低,表明高危组的总体免疫水平和 TME 免疫原性较高(图7E)。更重要的是,我们通过免疫免疫疗法门户获得了 UVM 患者的反应结果,发现风险评分较高的患者更有可能受益于免疫疗法(图7F) ,并且对4-SMG 签名具有更好的预测性能(图7G)。由于 ICB 反应在免疫检查点治疗中起重要作用,我们进一步分析了风险评分与 ICB 反应特征之间的相关性(图7H,J) ,发现其中,全身性红斑狼疮,碱基切割修补,p53信号通路,蛋白酶体和细胞因子-细胞因子受体相互作用显着正相关,而与酒精中毒和剪接体显着负相关。风险评分和肿瘤免疫周期步骤之间的相关分析也进行了研究,发现只有 MDSC 招募,Th2细胞招募和大单核细胞招募(步骤4)与风险评分没有显着相关性,而其他免疫周期步骤与我们的风险评分呈正相关(图7I,K)。

7、药物敏感性分析
根据风险评分,我们进一步评估了4-SMGs 在通过GdSC数据库预测化疗敏感性方面的潜在价值,以提高准确药物疗法。图8显示了九种常见的抑制剂或药物。KRAS (g12C)抑制剂 -12,Daporinad,塞鲁美替尼,端粒酶抑制剂 IX,Trametinib,Uprosertib 和 Vincristine 在高危人群中的 IC50相对较高。相比之下,高危人群的雷帕霉素和雷帕霉素的IC50较低。

8、平滑肌肌电图与肿瘤微环境的相关性
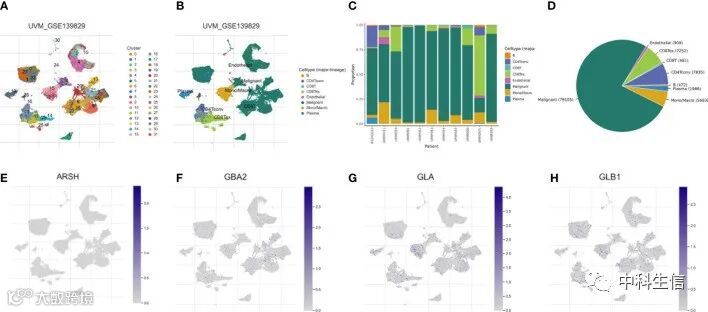
我们使用来自 TISCH 数据库的单细胞数据集 UVM _ GSE139829来分析免疫微环境中4-SMG 的表达。在 UVM _ GSE139829数据集(图9A,B)中有31个细胞群和8种免疫细胞类型,显示各种细胞类型的分布和数量(图9C,D)。免疫细胞中每种 SMGs 的表达水平在免疫微环境中的 ARSH 中几乎不表达(图9E) ,而在各种免疫细胞中表达 GBA2,GLA 和 GLB1(图9F-H)。GLA 主要在 Mono/Marco 中表达。
虽然我们的研究对 UVM 患者的预后评估和治疗方案的选择具有更大的临床意义,但我们的研究仍然有一些局限性。首先,我们的研究是一项回顾性研究,需要在未来的前瞻性研究中进行验证。其次,SMGs 影响 UVM 患者预后的机制需要在更多的活体内和体外实验中探索。最后,TCGA-UVM 队列中的主要种族是白人,缺乏亚洲人或黑人的数据。这使得在未来的研究中纳入其他种族成为关键。



