今天小编和大家分享一篇2024年1月发表在Frontiers in Endocrinology杂志的文章《Network pharmacology combined with Mendelian randomization analysis to identify the key targets of renin-angiotensin-aldosterone system inhibitors in the treatment of diabetic nephropathy》。
背景
糖尿病肾病(Diabetic Nephropathy,DN)是糖尿病的微血管并发症之一。尽管肾素-血管紧张素-醛固酮系统(Renin-Angiotensin-Aldosterone System,RAAS)抑制剂为当前的肾保护疗法提供了基本原理,但关于早期靶向RAAS是否能预防肾脏疾病的研究有限,目前尚无关于RAAS抑制剂关键靶点与DN之间因果关系的研究,因此迫切需要合理的方法来进一步阐明上述关系的潜在性质和意义。RAAS抑制剂治疗DN的潜在靶点有待探索。
流程图
方法
1.训练集(GSE96804包含41个2型DN女性和20个肿瘤肾切除术未受影响的人肾小球组织)和验证集(GSE1009包含3个DN和3个正常的人肾小球组织)从GEO公共数据库下载。6039个在DN中与RAAS抑制剂相关的靶点基因(DRGs)来自Swiss Target Prediction database,GeneCards database,Online Mendelian Inheritance in Man (OMIM)database。
2.差异表达分析
3.富集分析【Gene Ontology (GO)和Kyoto Encyclopedia of Genes and Genomes (KEGG)】和蛋白-蛋白相互作用(protein-protein interaction,PPI)网络构建
4.孟德尔随机化分析(Mendelian randomization,MR)
5.列线图的构建
6.组织定位、亚细胞定位和富集分析(Gene Set Enrichment Analysis,GSEA)
7.活性成分-关键基因靶点-疾病通路网络以及多维调控网络的构建
8.分子对接
结果
一、训练集中差异表达基因(Differently expressed genes,DEGs)的筛选和功能富集
在训练集的正常组和DN组之间共发现2,671个DEG,其中1,278个上调基因和1,393个下调基因。为了更好地解释DEGs的潜在生物学作用,进行了GO和KEGG富集分析,GO结果显示,DEGs主要参与“小分子分解代谢过程”和“α-氨基酸代谢过程”。KEGG富集分析显示,DEGs主要参与“糖尿病并发症中的脂肪酸降解”和“AGE-RAGE信号通路”。
图2
二、候选基因的鉴定和潜在生物学功能的探索
2671个DEGs和6039个DRGs取交集,得到60个候选基因。GO结果显示候选基因参与“白细胞迁移”和“对氧化应激的反应”。KEGG结果显示,候选基因主要参与“肾素-血管紧张素系统”和“PPAR信号通路”。并构建了包含57个节点和216条边的PPI网络,其中CASP3、ITGA5和MMP14之间的作用关系较强。
图3
三、CTSC和PDE5A被鉴定为DN的保护因子
筛选得到了与DN有因果关系的6个候选基因,分别是ALPL、CETP、CTSC、FOS、ITGA5和PDE5A,他们的IVW算法的P值>0.05,并且水平多效性分析的P值>0.05。此外,在疾病和对照组中CTSC和PDE5A的表达水平显著升高,因此,CTSC和PDE5A被选为关键靶点。并且CTSC和PDE5A是DN的保护因素(P<0.05,OR<1)。散点图显示CTSC和PDE5A与DN呈负相关(斜率<0)。在森林图中,MR整体效应小于0,表明CTSC和PDE5A是DN的保护因子。两个关键靶点的漏斗图显示,MR分析符合孟德尔第二定律的随机分组。为了评估MR结果的可靠性,进行了敏感性分析。Cochrane's Q检验的P值>0.05,表明暴露和结局的两个样本数据集之间没有异质性。同时,水平多效性检验的P值>0.05,表明不存在混杂因素的干扰。LOO分析显示,IV的效应值没有显著偏差。
表1

表2
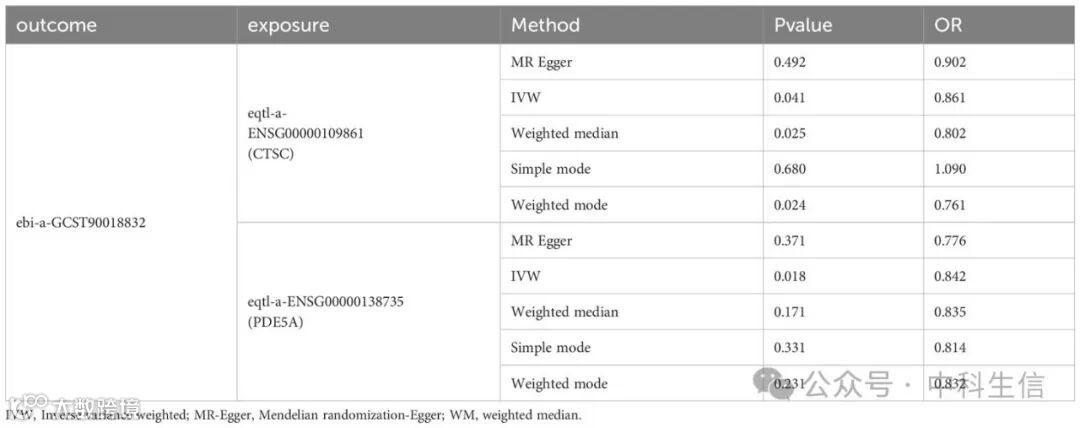
表3

表4
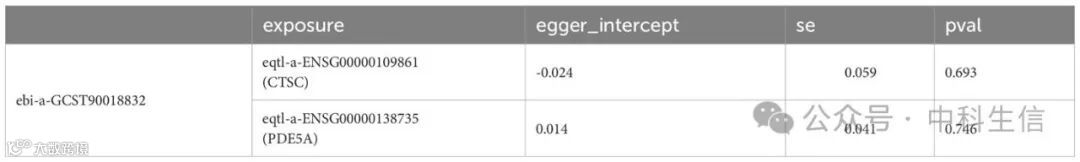
图4
四、CTSC和PDE5A在DN中的诊断价值
为了预测DN患者的患病率,在训练集中基于2个关键靶点建立了列线图,列线图的ROC曲线的AUC值大于0.7,表明列线图的预测准确性很高。校准曲线的斜率接近1,表明列线图具有相当的预测效率。此外,临床决策曲线的结果表明,列线图的净收入高于单个因素。这些结果反映了列线图的预测DN发生的准确率。
图5
五、探索CTSC和PDE5A的潜在结合位点
总共有12个器官或组织与CTSC相关,包括肺、平滑肌和CD56+_NK细胞。并且有11个器官或组织与PDE5A有关,包括肾上腺,心脏和肝脏。亚细胞定位分析显示,CTSC在细胞质中的比例最高,PDE5A在细胞核中的比例最高。此外,CTSC显著参与“细胞因子细胞因子受体相互作用”、“核糖体”、“ECM受体相互作用”、“焦点粘连”和“氧化磷酸化”。苯海拉明可能通过影响CTSC的这些途径在DN中发挥作用。同时,PDE5A显著参与“帕金森病”、“过氧化物酶体”、“亨廷顿病”、“ECM受体相互作用”和“氧化磷酸化”。非甾体抗炎药、卡托普利、氯氮卓、马来酸依那普利、西拉普利、缬沙坦和伊那奎隆可能通过PDE5A影响这些通路在DN中发挥作用。
图6
图7
图8
六、研究关键靶点与其他类型分子之间的调控机制
为了进一步探究CTSC和PDE5A的潜在机制,我们通过在线数据库和构建的调控网络预测了CTSC和PDE5A的靶向TFs、miRNAs和lncRNA。总共预测了44个与CTSC相关的TF,其中11个与PDE5A相关的TF,其中CTSC和PDE5A受E2F6、MAZ、CTCF和TCF12调控。此外,还建立了一个包含12个miRNA、45个lncRNA、CTSC和PDE5A的调控网络,其中SNHG5通过has-miR-216a-5p调控CTSC,SNHG5通过has-miR-181a-5p调控PDE5A。
图9
七、通过分子对接预测活性成分-关键靶点结合能力
为了确定核心活性成分与关键靶点之间的结合能力,进行了分子对接。分子对接分析表明,核心活性成分苯海拉明与CTSC的对接亲和力为-5.3 kcal/moL,表明结合能力良好。核心活性成分NSAID与PDE5A形成共价键。NSAID与PDE5A的对接亲和力为-5.32 kcal/moL,表明结合能力良好。
图10
八、PTGS2、ITGA4和ANPEP与急性肾损伤(AKI)有因果关系
为了研究在RAAS抑制剂临床联合给药中观察到的导致肾损伤的潜在因素,我们对RAAS抑制剂对AKI的核心靶点进行了孟德尔随机化分析。我们的研究结果表明,PTGS2、ITGA4、ANPEP和AKI之间存在因果关系。
表5
结论
CTSC和PDE5A是RAAS抑制剂治疗DN的关键靶点,对DN的诊断和治疗具有一定的临床意义。在RAAS抑制剂的靶点中,PTGS2、ITGA4和ANPEP与AKI有因果关系,值得进一步临床研究。

















