GTF2H5 Identified as a crucial synthetic lethal target to counteract chemoresistance in colorectal cancer
GTF2H5 被确定为对抗结直肠癌化疗耐药性的关键合成致死靶点
一区 Translational Oncology IF:4.5
摘要
背景:合成致死(Synthetic lethality,SL)作为一种新概念正在被探索用于对抗癌症进展和传统疗法的抗药性。尽管化疗对部分结直肠癌(CRC)病例有疗效,但仍有相当一部分患者面临挑战,导致 CRC 患者预后不良。与 CRC 相关的 SL 基因为确定治疗靶点提供了潜在的途径。
方法:CRC 相关 SL 基因来自 SynLethDB 数据库。从 UCSC 和 GEO 数据库中获取治疗和未治疗的 CRC 患者的大量 RNA 测序数据、突变数据和临床信息。肿瘤免疫学单细胞中心数据库是收集和分析单细胞RNA测序数据的资料库。实验验证了 SL 基因和化疗药物对耐药细胞的协同杀伤作用。
结果:本研究利用 WGCNA 确定了与化疗耐药性相关的关键 SL 基因,并根据这些基因将 CRC 患者分为两组。组间差异最明显的是与细胞外基质重塑相关的通路。此外,通过整合突变数据,还发现了五个潜在的 SL 基因,这些基因在 TP53 或 KRAS 基因突变时高度表达,导致严重的不良预后。随后的时间序列分析表明,在 CRC 细胞从敏感向耐药过渡的不同阶段,GTF2H5 的表达逐渐升高。最后,实验初步验证了 GTF2H5 可能在驱动 CRC 细胞耐药转变的过程中发挥了关键作用。
结论:鉴定与化疗药物相互作用的 SL 基因可为解决 CRC 患者的化疗耐药性问题提供新的思路。而 GTF2H5 在诱导 CRC 化疗耐药性方面具有根本性的影响,这为 CRC 提供了一个潜在的治疗靶点。
Figure1

获得与化疗反应性相关的 SL 基因。A:使用差异度量(1-TOM)对基因进行聚类的树状图。B:针对不同的软阈值幂(β)选择最佳无标度拟合指数。C:SL 基因与化疗反应的相关性热图。D:四个SL基因集(251个CRC相关SL基因以及27个参与常用的CRC 化疗药物(5-氟尿嘧啶、亚叶酸、奥沙利铂)作用的SL基因)的维恩图。E:筛选关键22个SL基因的桑基图。
Figure2
构建基于 SL 基因的 CRC 患者亚型并进行功能分析。A:图示 k = 2 时的最佳共识聚类结果。B:两种患者亚型的DEGs表达水平的火山图。C:DEGs 的蛋白-蛋白相互作用(PPI)网络。D-F:DEGs 的 GO 和 KEGG 富集分析。
Figure3

不同 SL 亚型的免疫和基质细胞情况。A:两种亚型的基质、免疫和ESTIMATE评分的小提琴图。B:不同 SL 亚型之间 21 种免疫细胞的浸润水平。C:基于 GSE19860、GSE69657 和 GSE106584 数据集的化疗耐药 CRC 患者共有的显着富集基因集。
Figure4
鉴定导致突变型 CRC 患者预后不良的 SL 基因。A:显示了CRC中经常突变的基因和SL基因。B-F:ABCG2 (B)、CAMK2G (C)、SORBS1 (D)、GTF2H5 (E) 和 TPM1 (F) 的表达预测了 CRC 患者的生存率。根据 TP53 或 KRAS 状态对队列进行分层显示,这些 SL 基因的高表达预示着 TP53 或 KRAS 突变型而非野生型 CRC 患者的生存率较低。
Figure5

肿瘤条件下 SL 基因的表达谱。A:GEPIA 数据库中 ABCG2、CAMK2G、SORBS1、GTF2H5 和 TPM1 在 CRC 组织和正常组织中的表达情况。B:根据 GSE35602 数据集确定的五个 SL 基因在 CRC 配对基质组织中的表达水平。C:根据 GSE35602 数据集确定的五个 SL 基因在配对的 CRC 上皮组织中的表达水平。
Figure6

通过单细胞测序鉴定主要位于上皮细胞和成纤维细胞的五个 SL 基因。A:根据 GSE166555 和 EMTAB8107 数据集绘制的 CRC 不同细胞群的 UMAP 图。B、 C:基于 GSE166555 数据集(B)和 EMTAB8107 数据集(C),ABCG2、CAMK2G、SORBS1、GTF2H5 和 TPM1 在已识别细胞类型中的表达水平。D:由 SL 基因组成的特征基因在不同细胞群中的表达水平的 Violin 图。ns:无显著性,*P < 0.05,⁎⁎P < 0.01,⁎⁎P < 0.001。
Figure7
单细胞水平功能分析和时间序列基因表达分析。A、B:不同细胞群中上调或下调的富集途径。C:不同细胞间的细胞-细胞相互作用。D:成纤维细胞与其他细胞之间的相互作用。E:药物治疗后不同时期 SL 基因的变化。F:药物治疗后SL基因在器官组织中的表达 ns:无显著性,*P < 0.05,**P < 0.01,***P < 0.001。
Figure8

验证敏感或耐药细胞中 SORBS1、GTF2H5 和 TPM1 的表达水平。A、B:HCT8(A)和 HCT 15 细胞(B)暴露于不同浓度 FOLFOX 的剂量-反应曲线。C、D:PCR 实验验证敏感(C)或耐药(D)HCT8 或 HCT15 细胞经不同浓度 FOLFOX 处理 48 小时后 SORBS1、GTF2H5 和 TPM1 的表达变化。
Figure9

GTF2H5 对维持 CRC 细胞的增殖能力至关重要。A:GTF2H5在耐药的HCT8和HCT15细胞中的蛋白表达水平。B:通过 qPCR 和 Western 印迹检测耐药 HCT8 和 HCT15 细胞中 GTF2H5 蛋白表达下调。C、D:用 si-GTF2H5 或对照组转染耐药 CRC 细胞 48 小时,然后用流式细胞术评估细胞凋亡水平(C),用 CCK-8 检测法评估细胞增殖(D)。E:成纤维细胞中 α-SMA 和 Vimentin 阳性标记物的免疫荧光检测。
Figure10
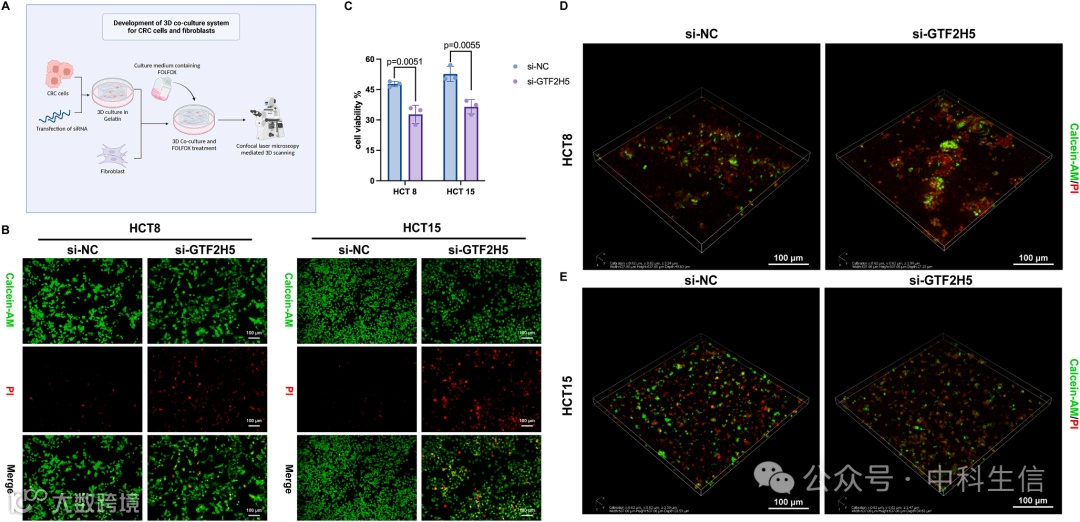
GTF2H5 在 CRC 耐药性的形成过程中起着关键作用。A:CRC细胞与成纤维细胞共培养过程示意图。B:在二维细胞培养条件下,耐药的 HCT8 和 HCT15 细胞经 FOLFOX 处理 48 小时,绿色荧光表示活细胞,红色荧光表示死亡或垂死细胞。C:三维共培养实验显示了敲除 GTF2H5 后耐药 HCT8 或 HCT15 细胞的存活率;每组随机选择三个视野,进行活细胞和死细胞计数,然后计算细胞存活率。D、E:用共聚焦显微镜进行三维层扫描,绿色荧光代表活细胞,红色荧光代表死亡或濒死细胞。图示为 HCT 8 细胞(D)和 HCT 15 细胞(E)的代表性图像。


