点击蓝字 关注我们
基于当时的预测,到2025年其规模有望达到120亿至150亿美元,年均复合增长率(CAGR)保持在7%-10%的较高区间。市场增长主要源于三方面:
一是人口结构与疾病谱变化,印尼拥有超2.8亿人口,已进入老龄化社会(65岁以上人口占比约7%),高血压、糖尿病等慢性病负担日益加重;二是政府政策强力驱动,印尼将医疗健康列为优先发展产业,并通过全民医保计划(JKN)、强制药品国产化率(TKDN)政策以及全民免费体检等具体项目,持续加大投入;三是供应链本土化与产业升级,TKDN政策鼓励本地生产以减少进口依赖,同时政府正通过提升本土医疗服务质量和发展医疗旅游,以减少每年百万人规模的医疗旅游外流。
医药健康产业已被印尼政府列为重点产业,享受投资激励政策。在全球供应链重构趋势下,印尼凭借庞大市场体量、多样化需求及东盟门户地位,成为中国药企出海的战略要地。本文聚焦药品(限于篇幅不包括中药,择期阐述)注册核心要求、审批路径与战略建议,助力企业高效合规开拓这一高潜力市场。
印尼药品监管体系全景
1、药品监管条例
《健康法》(Law No. 17 of 2023):印尼卫生健康领域的综合性基础法律,确立了包括药品监管在内的卫生健康事务的基本原则和框架。
2、药品监管机构
印尼食品和药品监督管理局(BPOM)是直接向总统报告并与印尼卫生部密切协作的独立监管机构,成立于2001年,统一负责药品注册、GMP检查、上市后监测等全生命周期监管。
3、药品注册的关键步骤
印尼的药品注册是一个数字化、以e-CTD系统为核心的电子化流程。整个过程强调资料的完整性、国际协调性以及申请人的责任。根据BPOM《药品注册指南》及相关法规,药品注册呈现如下步骤:
预审→缴费→技术评估→沟通→批准/拒绝
步骤一:预审
目的:形式审查,检查申请是否完整。
关键点:(1)所有申请必须通过BPOM的e-CTD系统提交;(2)文件需按东盟通用技术文件(ACTD)格式准备,此格式为BPOM强制要求。
步骤二:缴费
目的:支付官方审核费用。
关键点:(1)形式审查通过后,需在指定窗口期(通常10-15个工作日)内缴费,逾期视为撤销;(2)费用一旦支付,概不退还;(3)费用因申请类型而异。
步骤三:技术评估
目的:对申请进行科学、质量和法规层面的实质性审查。
关键点:缴费确认后,申请将根据其所属的“审评路径”进入评估队列。印尼BPOM主要依据以下三条路径设定法定审评时限:
路径I (Path I):适用于用于治疗严重或危及生命的疾病的产品。审评时限为100个工作日。
路径II (Path II):适用于已在FDA、EMA、PMDA等印尼BPOM认可的参考监管机构批准的新药。审评时限为150个工作日。
路径III (Path III):适用于其他申请。其中,新药/生物制品的审评时限为300个工作日;仿制药的审评时限为100-150个工作日(视BE研究等因素)。
步骤四:沟通
目的:解决审评中发现的问题。
关键点:(1)对于复杂产品,多次问答是标准流程。(2)申请人收到质询后,有最多2个月的时间提交补充资料,否则申请可能被关闭。可根据合理理由(如需补充长期稳定性数据等)通过系统正式申请延期,延期时长由BPOM审评部门酌情批准。(3)所有正式沟通均通过e-CTD系统进行。
步骤五:批准/拒绝
批准:(1)批准后系统分配唯一的注册号(NA Number)。BPOM实施电子证书系统,注册信息通过官方渠道发布。(2)注册有效期5年,需在到期前6个月内申请再注册。
拒绝:(1)拒绝通常基于数据不足,申请人可在收到通知后45个工作日内提交书面上诉。(2)若因安全或效能原因被拒,产品1年内不得重新提交申请;但若在此期间于参考监管机构(如FDA、EMA、PMDA)获批,则可立即重新提交。
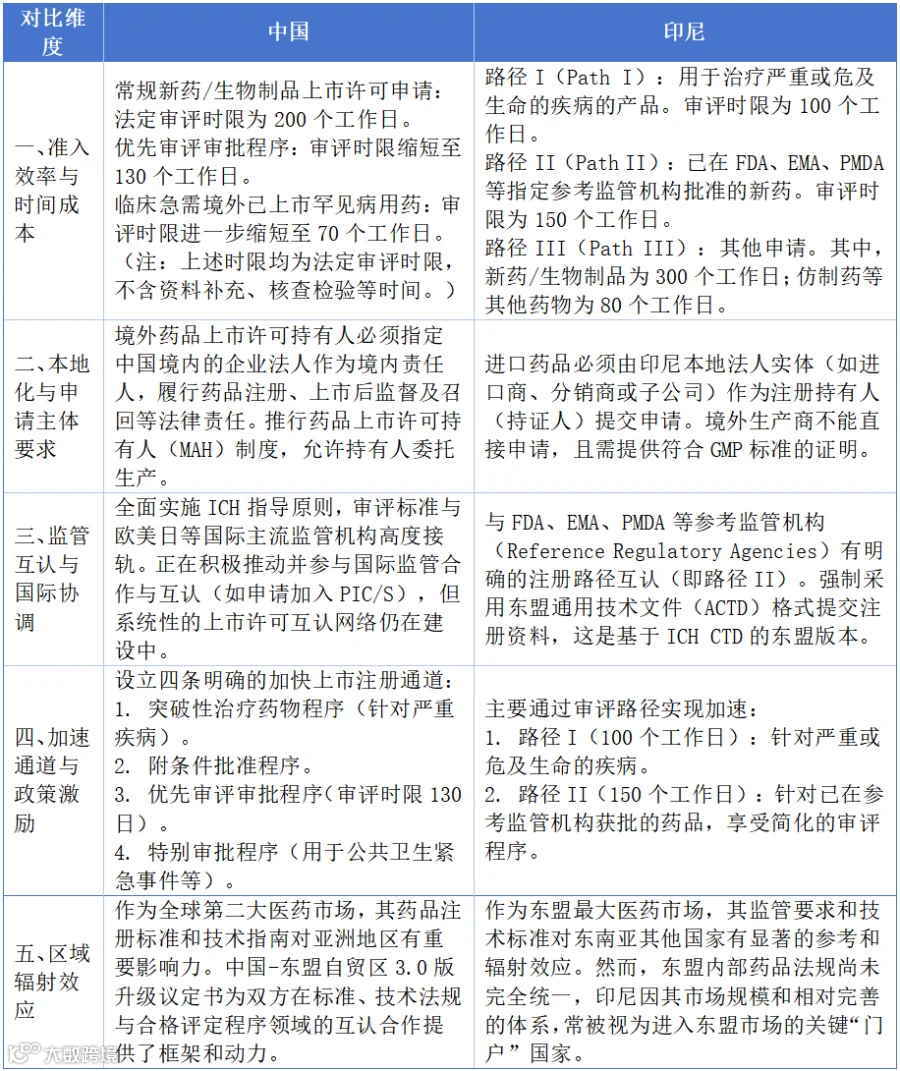
中国与印尼药品注册制度的比较
以下是从五大关键维度对中国与印尼药品注册制度的系统性对比,以表格形式清晰呈现,便于快速把握两国监管差异与战略机会:
中国药企布局印尼市场的关键建议
面对印尼医药市场的人口红利与政策窗口期,中国药企若要高效、合规地实现本地化落地,需在以下四方面重点发力:
1. 精准选择注册路径,规划全球申报序列
对于已在美国FDA、欧盟EMA、日本PMDA等印尼BPOM认可的参考监管机构获批的成熟产品,应优先选择路径II(Path II)进行申报,其法定审评时限为150个工作日,能大幅压缩审批时间并降低重复研究成本。对于仿制药,则适用路径III(Path III),审评时限为80个工作日。建议企业在产品全球开发早期就将印尼纳入东盟首批申报市场,统筹规划注册策略。
2. 审慎选定本地注册持有人,筑牢合规根基
根据印尼法规,所有进口药品的注册持有人(Marketing Authorization Holder, MAH) 必须是印尼本地法人实体(如进口商、分销商或子公司)。该持有人不仅承担注册申请、GMP符合性声明、药物警戒等全部法律责任,还在供应链管理、医保谈判和税务事务中扮演核心角色。务必选择兼具深厚医药行业经验、可靠政府事务能力及完善分销网络的本地合作伙伴,避免因代理人能力不足导致注册失败或上市后运营中断。
3. 深度适配ACTD格式与e-CTD系统,追求一次性通过
印尼强制采用东盟通用技术文件(ACTD) 格式提交注册资料。其模块逻辑与ICH CTD相似,但在文件编排、数据呈现等细节上有其特定要求。技术资料(质量、非临床、临床)通常可使用英文撰写,但产品标签、说明书等必须提供印尼语版本。强烈建议企业提前组建或委托熟悉ACTD及印尼BPOM审评习惯的专业团队,对注册资料进行预审和优化,确保通过e-CTD系统首次提交即满足形式与技术的双重标准,从而规避因补正回复超期(通常为2个月)而导致申请失效的风险。
4. 锚定国家战略发展赛道,善用政策与资本红利
《印尼黄金2045愿景》将医疗健康(包括制药产业)列为国家优先发展的战略领域之一,并配套了税收减免、土地优惠等投资激励政策。中国药企可结合自身优势,聚焦于糖尿病、心血管疾病、传染病等印尼高发疾病领域。同时,积极探索与本地医疗机构、大学合作开展真实世界研究(RWS),这些数据不仅能支持医保准入,还能增强产品在区域内的医学影响力。
结语
印尼正从人口大国向区域医疗强国迈进。其日益与国际接轨的监管框架、清晰的注册路径,为中国创新药与高质量仿制药提供了极具潜力的“东盟门户”。然而,机遇总与挑战并存——法规细节的本地化解读、供应链的稳健布局、以及商业文化差异,都要求中国企业以长期主义的心态和专业化的运营深入耕耘。
未来五年,将是中印尼医药合作从“产品贸易”迈向“产业与生态共建”的关键阶段。唯有将全球领先的技术、质量体系与对本地市场的深刻洞察相结合,方能在这片高速增长的市场中行稳致远,真正实现“立足印尼、辐射东盟”的战略蓝图。

声明:①本公众号内容仅用于信息交流,素材均来源于公开渠道。如您认为相关内容涉嫌侵权,请通过微信:huli22646520提交书面通知(请注明“侵权投诉”),我们将在24小时内核查并依法处理。②商务合作及内容转载授权,请联系上述微信(添加时请备注事由)。


