研究背景



骨关节炎(OA)作为全球主要致残原因之一,影响超5.95亿成年人,其核心病理特征是关节软骨渐进性降解,给患者与社会带来沉重负担。当前临床软骨修复策略(如微骨折、自体软骨细胞移植等)存在修复周期长、效果欠佳等局限——传统生物材料修复依赖内源性细胞募集与增殖,往往导致修复过程迁延;而软骨类器官(COs)作为干细胞定向分化形成的微型三维组织,兼具天然软骨的结构与功能特性,无需依赖内源性细胞,有望大幅缩短修复周期,成为软骨再生的新型策略。

基本信息



DOI:10.1186/s40779-025-00625-z
论文题目:Accelerating cartilage regeneration with DNA-SF hydrogel sustained release system-based cartilage organoids
发表期刊:Military Medical Research
研究总结



本研究基于甲基丙烯酰化丝素蛋白(SilMA)水凝胶,通过丙烯酰化聚乙二醇NHS酯(AC-PEG-NHS)共价接枝葡萄糖胺(Glu)与TD-198946,构建DNA-丝素蛋白(DNA-SF)水凝胶缓释系统(DSRGT),结合投影式光固化生物3D打印技术,实现骨髓间充质干细胞(BMSCs)定向分化为毫米级软骨类器官(COs)。
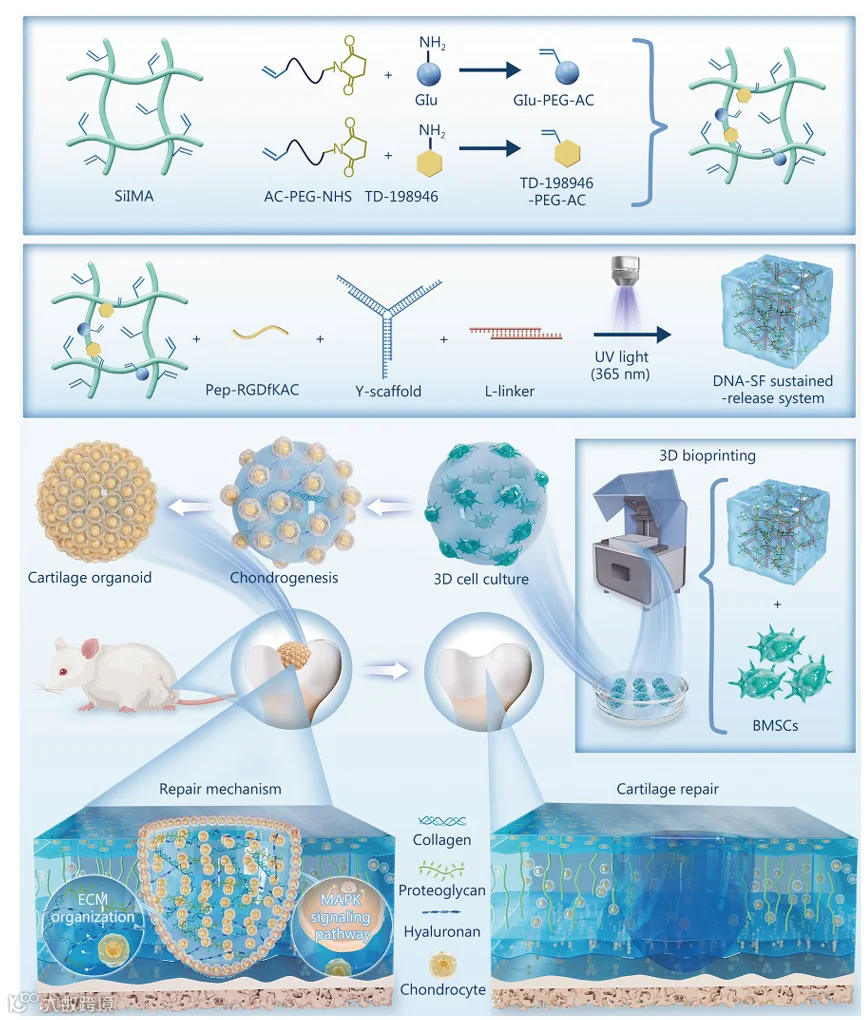
DSRGT水凝胶与软骨类器官具有以下特点和优势:
(1)精准药物递送:AC-PEG-NHS共价接枝实现Glu与TD-198946长效缓释,避免传统物理包裹的药物暴释问题,28天内持续支持软骨分化。
(2)优异仿生性能:DNA-SF双网络结构模拟软骨ECM,孔隙率达56.44±3.88%,孔径约277.6±18.75μm,保障细胞迁移与营养交换;力学性能匹配关节环境(储能模量G′>损耗模量G″,压缩模量适配软骨生理需求)。
(3)高效软骨再生:4周龄COs移植后8周,软骨缺损修复评分(ICRS)达10.08±0.79,表面粗糙度(Ra)与健康软骨无显著差异,再生组织中ColⅡ与ACAN表达显著高于对照组。
(4)高生物安全性:体内毒性评估显示,DSRGT与COs对大鼠心、肝、脾、肺、肾无损伤,血常规及肝肾功能指标正常,无系统性毒性。

EFL合作产品

产品型号 |
产品名称 |
|
EFL-SilMA-001 |
|
|
EFL-AC-PEG-NHS-2K |
|
|
EFL-BP8601 Pro |
|
研究参考



1. DSRGT水凝胶与软骨类器官(COs)的制备
(1)DSRGT水凝胶制备
原料配比:在pH 7.4的PBS中,37℃下溶解并混合以下成分:10 wt% SilMA、0.25 wt% LAP、5 wt% Pep-RGDfKAC、100 nmol/L TD-198946(预溶于DMSO)、10 mmol/L Glu、4.5 wt% AC-PEG-NHS、500,000 nmol/L单链DNA(ssDNA)。
共价接枝机制:AC-PEG-NHS的NHS酯基团与Glu、TD-198946的氨基反应,丙烯酸酯基团与SilMA反应,实现两种活性分子在DNA-SF水凝胶网络的稳定接枝。
光交联与3D 打印:DSRGT前驱液经365 nm紫外光(20 mW/cm²,17 s)交联成胶;采用DLP 3D打印机打印直径2.5 mm的球形支架,层厚100 μm,保障结构均一性。
(2)软骨类器官(COs)构建
细胞接种:将第3代大鼠BMSCs(1×10⁶ cells/mL)与DSRGT前驱液混合,通过DLP系统打印成细胞负载微球。
成软骨诱导培养:在含1 mmol/L丙酮酸钠、10 ng/mL TGF-β3、0.1 μmol/L地塞米松、1% ITS、1 μmol/L抗坏血酸-2-磷酸的诱导培养基中培养,每2天换液,分别收集1、2、4、6周龄COs进行表征。
2. DSRGT水凝胶与COs的表征验证
(1)水凝胶结构与性能
形态与孔隙:FE-SEM显示DSRGT呈均匀多孔结构,表面与内部孔隙连通,孔隙率56.44±3.88%,孔径277.6±18.75 μm,利于细胞黏附与营养交换;与DSR(无Glu/TD-198946)、DSRG(仅含Glu)、DSRT(仅含TD-198946)相比,孔隙参数无显著差异,证明接枝分子不破坏网络结构。
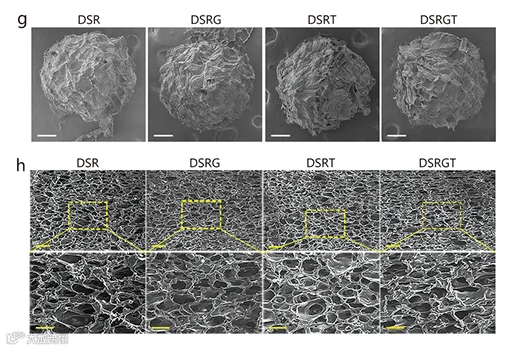
图1 在DLP系统中打印出的带有DSR、DSRG、DSRT和DSRGT的球体的场发射扫描电子显微镜(FE-SEM)图像
力学与流变性能:频率扫描显示DSRGT的储能模量(G′)始终高于损耗模量(G″),呈现典型水凝胶弹性特征;剪切变稀行为(黏度随剪切应力降低)利于3D打印,且PEG分子引入使黏度适度降低,提升打印流畅性。
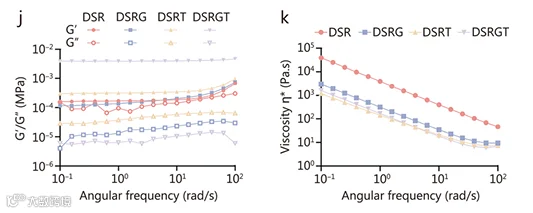
图2 DSR、DSRG、DSRT和DSRGT的流变曲线以及粘度曲线
缓释与降解:DSRGT在PBS中28天内实现Glu与TD-198946平稳释放,前3天快速释放42.26±3.67%,21天累积释放89.85±2.98%,28天达95.94±2.59%;降解实验显示6周内残留质量45.28±8.85%,降解速率匹配COs发育周期,避免过早失去支撑或长期残留。
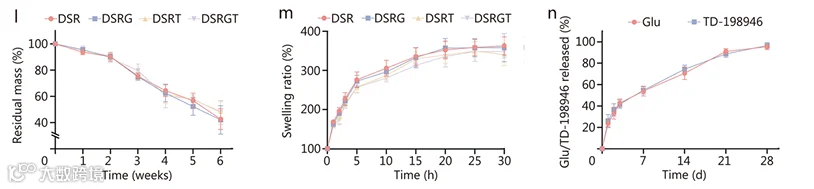
图3 DSR、DSRG、DSRT和DSRGT的降解速率、膨胀率以及Glu和TD-198946在DSRGT中的释放曲线
(2)生物相容性验证
活死染色:BMSCs与DSR、DSRG、DSRT、DSRGT共培养1、3、5天,活细胞比例均> 90%,死细胞极少,各组无显著差异,证实水凝胶无细胞毒性。
细胞增殖与迁移:CCK-8实验显示各组BMSCs增殖活性随培养时间上升;划痕实验与Transwell实验证实,DSRGT组12小时细胞迁移率达55.09±1.08%,显著高于其他组,归因于TD-198946激活Notch3信号通路促进迁移。
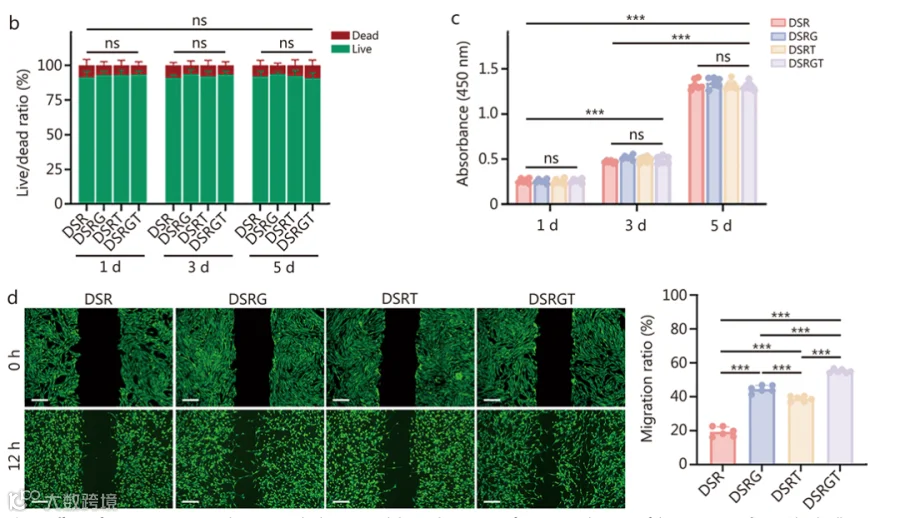
图4 DSR、DSRG、DSRT和DSRGT对骨髓间充质干细胞的生物相容性和迁移性的影响
3. COs的体外生物活性评估
(1)成软骨分化能力
基质合成检测:阿尔新蓝染色显示,DSRGT组7、14天成软骨诱导后糖胺聚糖(GAG)染色最强;DMMB法与ELISA定量证实,14天时DSRGT组GAG含量(归因于Glu)与ColⅡ含量(归因于TD-198946)显著高于其他组。
基因与蛋白表达:qRT-PCR显示,DSRGT组14天SOX9、ColⅡ、ACAN mRNA表达最高,ColⅠ、ColⅩ表达最低;Western blot验证ACAN(250 kDa)、ColⅡ(180 kDa)、SOX9(56 kDa)蛋白表达水平在DSRGT组最优,证实其抑制纤维化与肥大的能力。
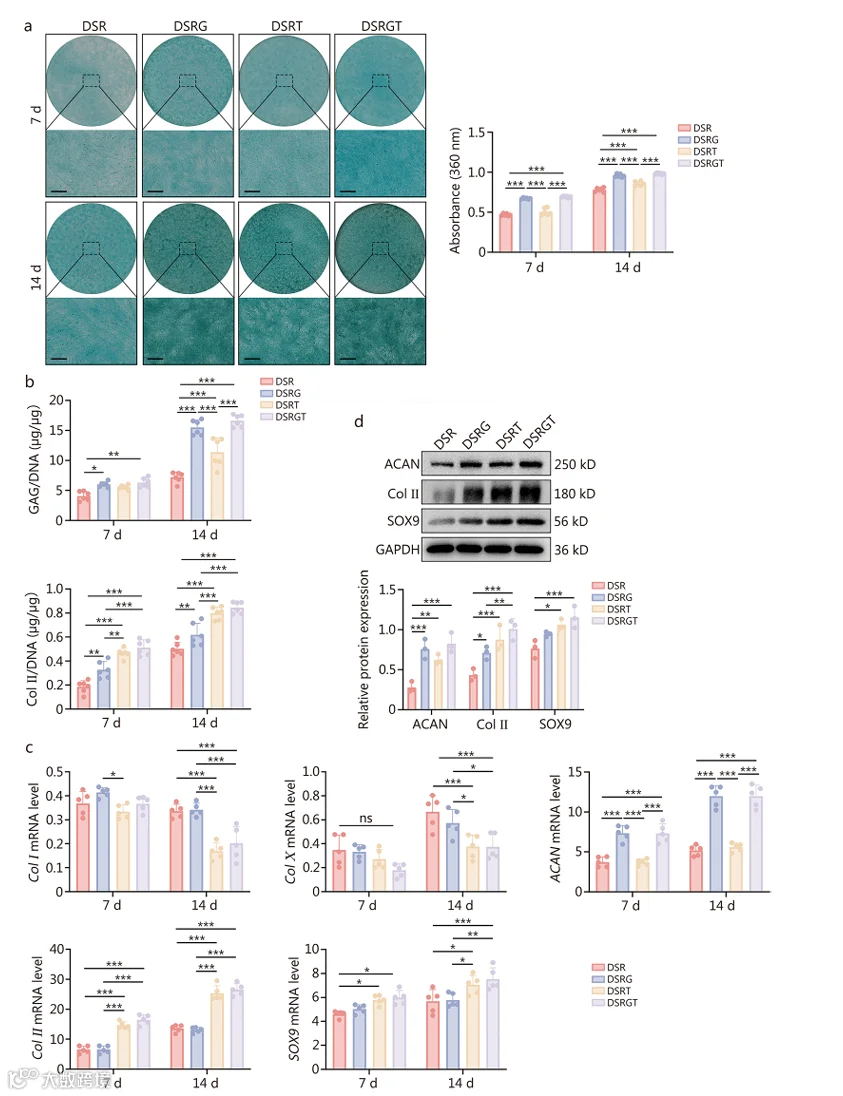
图5 骨髓间充质干细胞通过DSR、DSRG、DSRT和DSRGT实现的成软骨分化能力
(2)COs发育周期优化
形态与染色分析:1周龄COs无明显形态变化,SOX9表达强(早期成软骨标志);2周龄表面细胞致密,4周龄形成多层结构,GAG含量最高(阿尔新蓝与番红O/固绿染色最强);6周龄因药物释放完毕、营养交换受阻,内部出现凋亡空泡。
免疫荧光验证:4周龄COs ColⅡ、ACAN表达最高,ColⅠ、ColⅩ表达最低,证实为最优透明软骨表型,故选择4周龄COs进行体内实验。
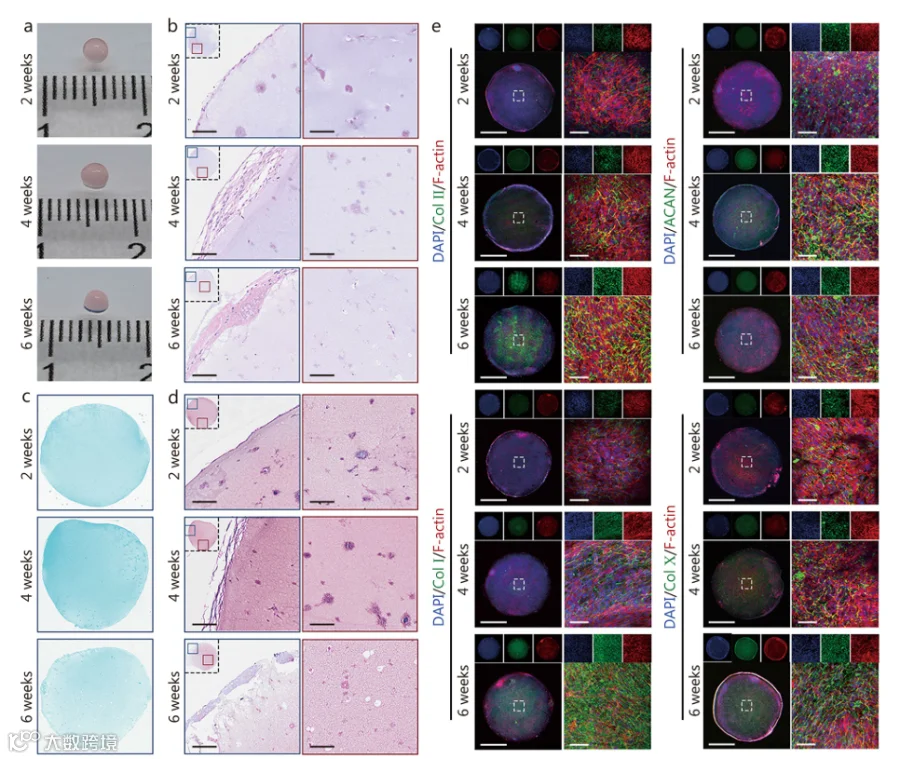
图6 对培养2周、4周和6周的细胞系进行评估
4. COs的体内治疗效果评估
宏观与表面性能:8周时CO组缺损填充完整,表面光滑(ICRS评分10.08±0.79),原子力显微镜(AFM)显示表面粗糙度(Ra)与Sham组无显著差异,显著低于对照组与DSRGT组。
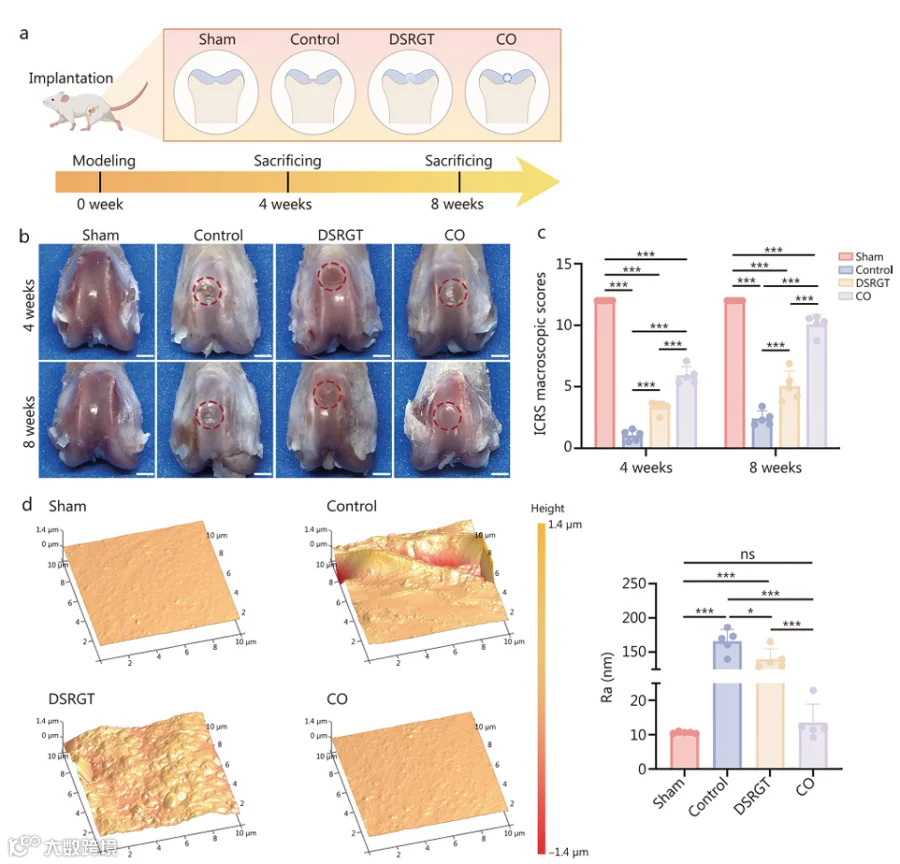
图7 治疗后4周和8周时再生软骨的宏观评估
机制验证:Western blot显示CO组p-p38(38 kDa)、p-ERK(42 kDa)、p-JNK(46 kDa)蛋白表达显著升高,证实MAPK信号通路激活是软骨再生的关键机制;加入ERK抑制剂PD98059后,COs的ACAN、ColⅡ表达显著降低,进一步验证通路作用。
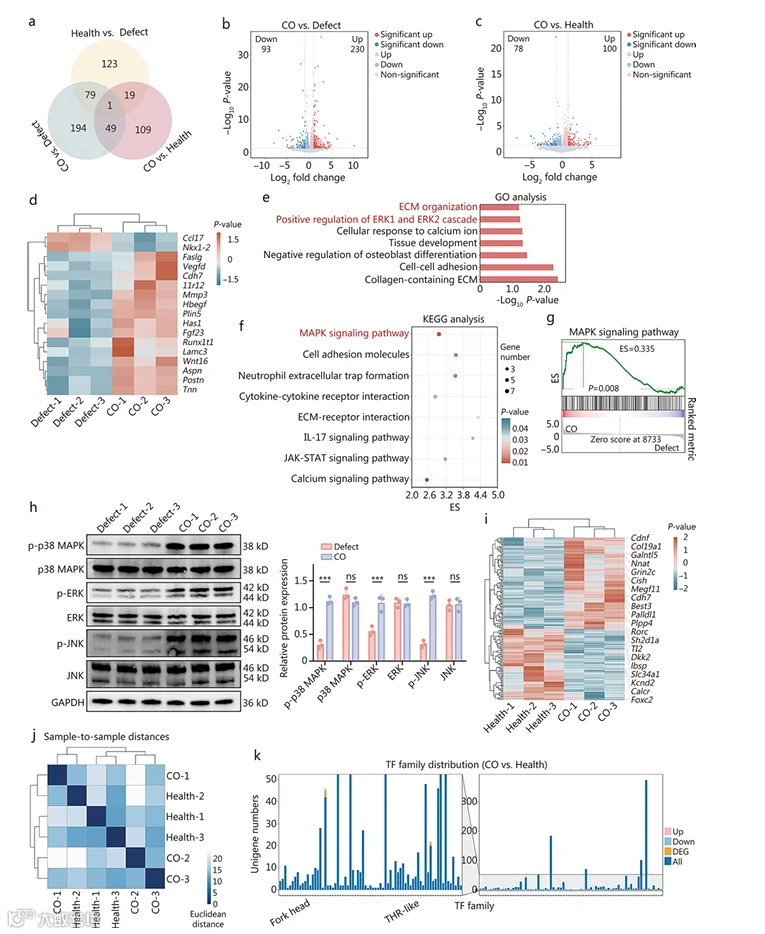
图8 对缺损组、对照组和健康组再生的软骨进行mRNA分析

EFL新媒体矩阵



联系我们