

 全文速览
全文速览
 背景介绍
背景介绍
 本文亮点
本文亮点
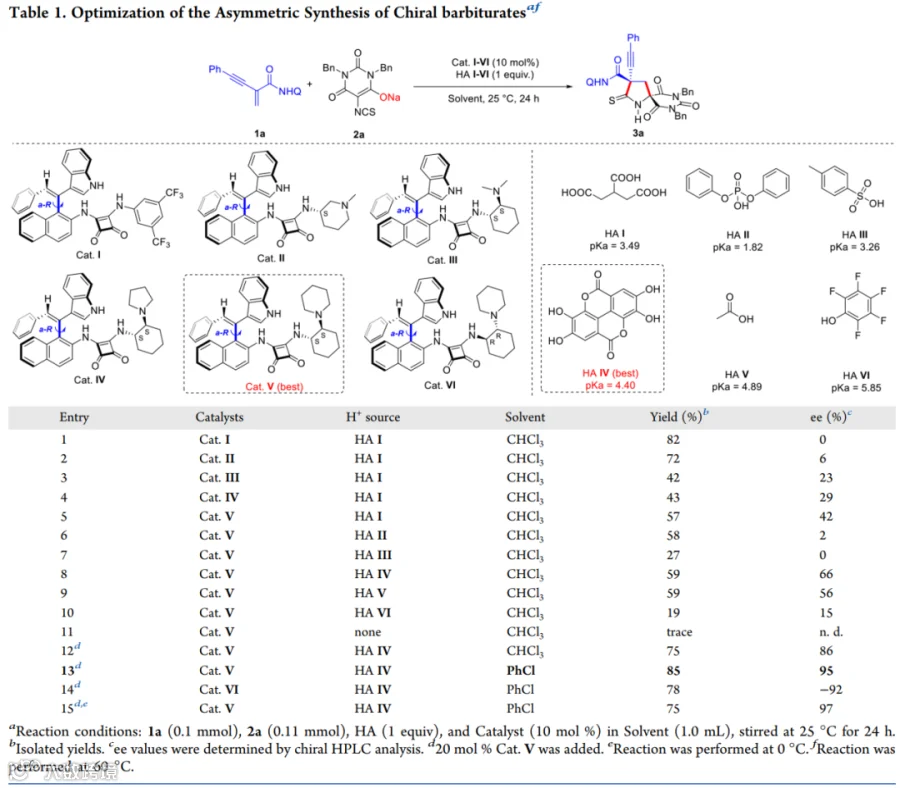
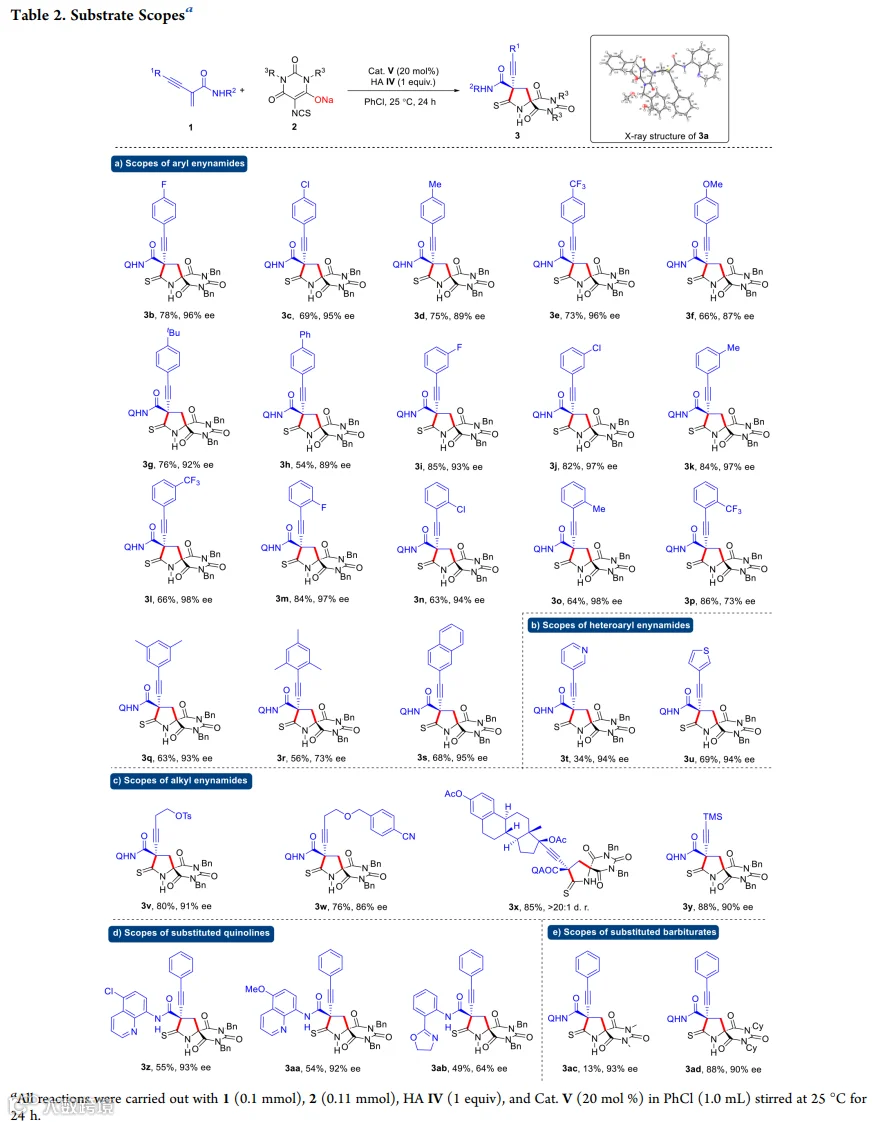
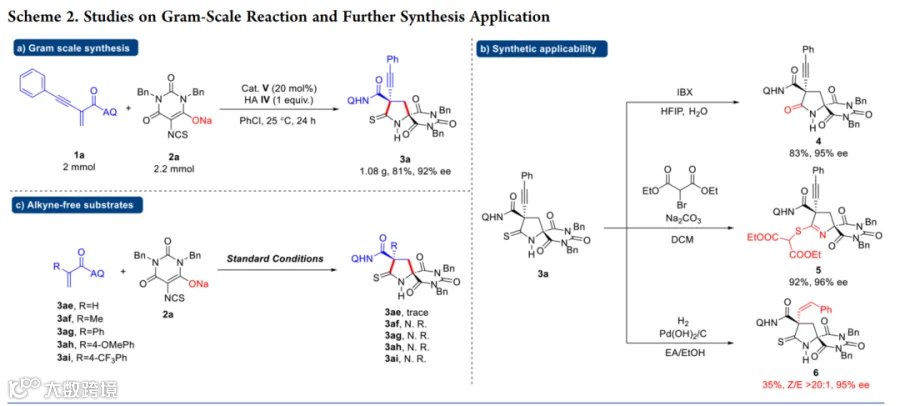
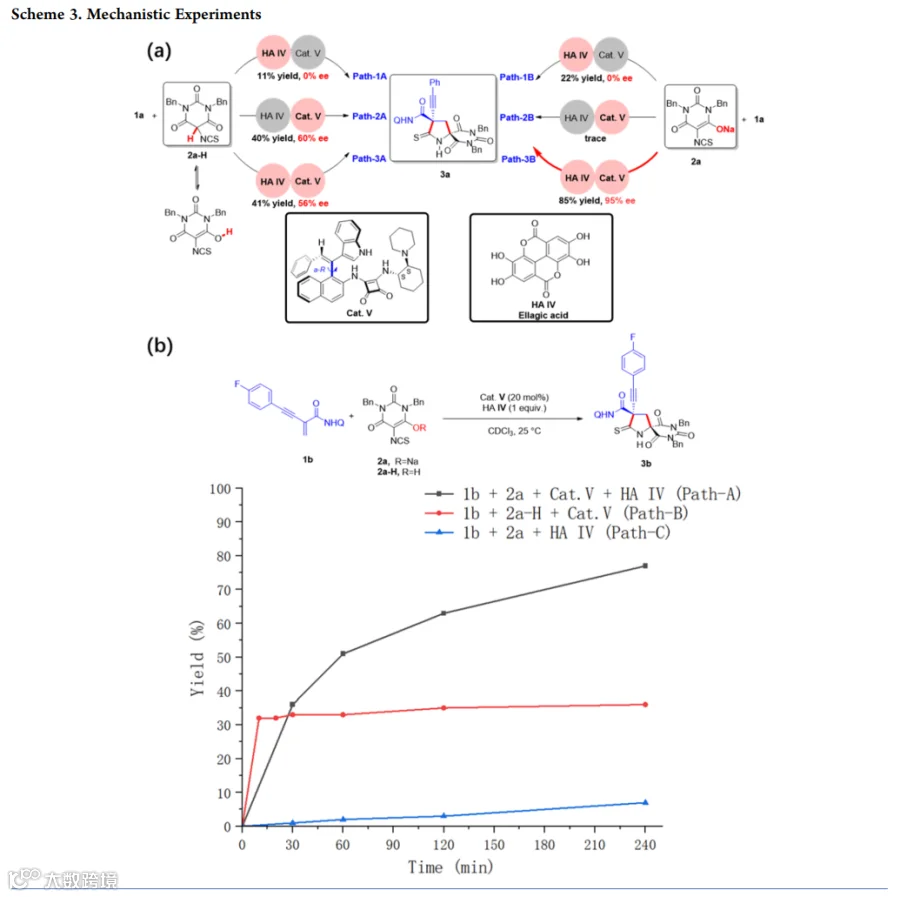
 图文解析
图文解析
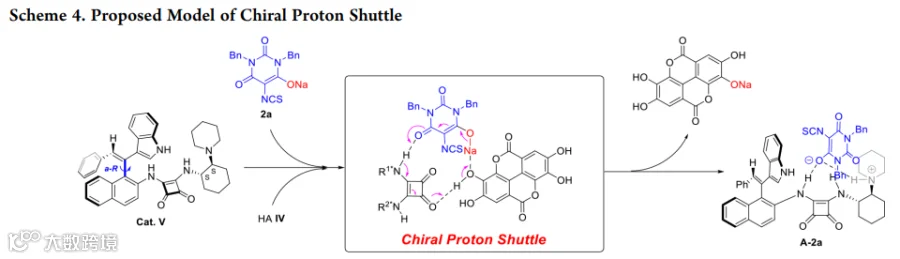
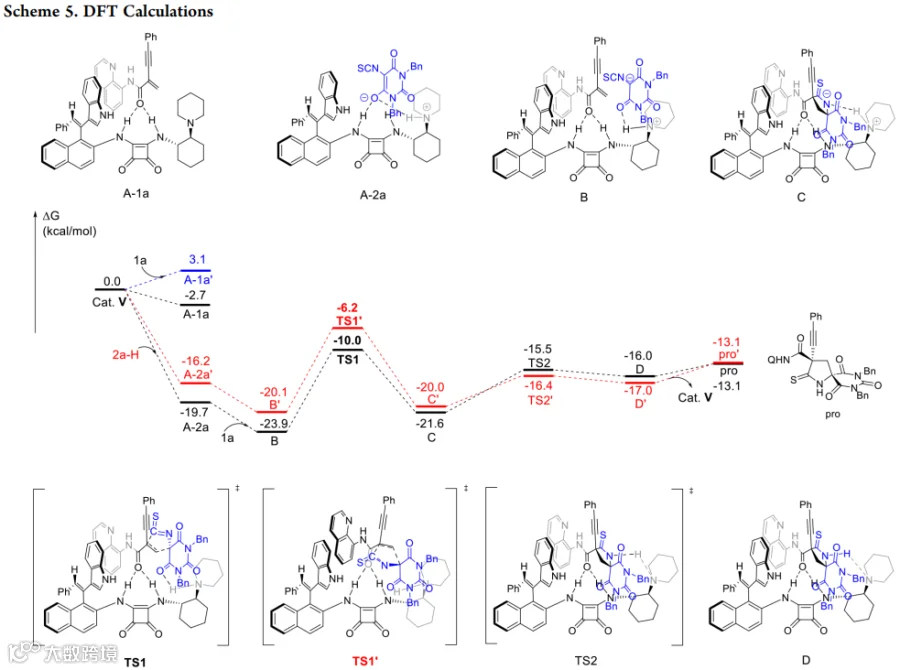
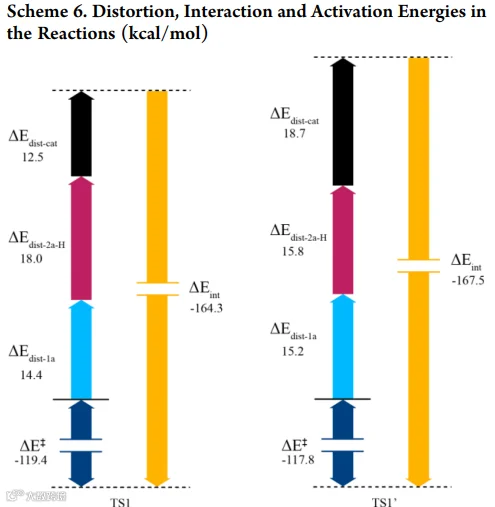
 总结与展望
总结与展望
 研理云服务器
研理云服务器
业务介绍
● 配置多样(单台塔式、两台塔式、多台机架式),按需定制,质量可靠,性价比高。
扫码添加客服微信



 研之成理
研之成理

 全文速览
全文速览
 背景介绍
背景介绍
 本文亮点
本文亮点
 图文解析
图文解析







 总结与展望
总结与展望
 研理云服务器
研理云服务器
业务介绍
● 配置多样(单台塔式、两台塔式、多台机架式),按需定制,质量可靠,性价比高。
扫码添加客服微信




