
苏州晶云主办的CMC系列线上课程将于2020年4月17日-5月22日在药渡大学平台上线。课程邀请国内外药物研发领域知名专家进行分享和互动。点击图片查看课程详情。
第二期课程回顾
药物多晶型,控制策略
及其在制剂设计中的应用
4月29日,晶云加拿大子公司Candoo Pharmatech的CEO、拥有17年制剂研发生产和管理经验的李永强博士就“药物多晶型对制剂设计的影响”这一主题与广大学员进行了深入交流。李博士从药物制剂设计的原则出发,以终为始地介绍了药物多晶型在制剂设计中应用的方方面面。下面,小编将汇总李博士课程中的关键内容,以飨读者。

内容导览
制剂设计的基本原则
药物多晶型对制剂设计的影响
多晶型药物制剂设计
Candoo研发服务介绍

制剂开发的QbD

制剂设计的三个支柱
药物多晶型对制剂设计的影响直接体现在不同的晶型可能具有不同的物理化学性质、不同的固态性状、不同的流动性、不同的吸湿性以及不同的机械性质,进而影响制剂性能和生产工艺。
物理化学性质方面,晶型会影响熔点、固有溶出速率(关联生物等效性)、不同温度/湿度/机械力条件下的固态稳定性等。
固体性状方面,不同晶型可能具有差异显著的颗粒形貌,如球状、块状、片状和针状等,对加工性能直接产生影响。
流动性方面,不同晶型样品可能具有不同的堆密度和振实密度,从而导致流动性上的差异并对辅料选择产生影响。
吸湿性方面,不同晶型对水分的吸附能力不同,影响制剂产品的生产工艺和产品质量。
机械性质方面主要体现在可压性上,例如小分子药物Acetaminophen的晶型II相比于晶型I具有更好的可压性,使其在制剂上更具优势。
既然药物晶型对制剂性能和生产工艺具有关键性的影响,那么如何控制药物晶型也就成为了制剂开发过程需要重点关注的环节。通常可以从以下几方面入手:
药物多晶型对制剂设计策略的影响也体现在药物知识产权保护方面。常见的药物知识产权(专利)包括四大类:化合物专利,晶型专利,配方专利和使用方法专利。
鉴于药物晶型对制剂设计的重要影响,在多晶型药物制剂设计中有哪些主要的考虑因素,想必就是大家非常关心的问题了。下面将以难溶性药物(BCS II类和IV类)为例作一概要介绍。
根据溶解度(solubility)和渗透性(permeability)的高低,可以将药物划分为I-IV四个类别,即BCS分类系统(Biopharmaceutics Classification System)。随着高通量筛选和组合化学等技术的发展,现在开发的候选药物分子中属于难溶性药物的比例越来越大。如何使难溶性药物(BCS II类和IV类)获得合适的生物利用度,成为了药物开发中需要解决的一个难题。尤其是对于难溶性药物的仿制药,低溶解度往往是制约其与原研药达到生物等效(bioequivalence,BE)的关键因素。从制剂的角度进行思考,是解决此类问题的一种常用策略。

药物BCS分类系统
当药物在体内释放,溶解并被吸收进入人体后,通过血液循环进入身体组织并发挥药效,同时也会通过代谢和排泄被清除出体外。因此,影响药物临床药效最重要的因素之一便是药物的生物利用度,即药物被吸收进入人体的速度和程度。对于最常见的口服制剂,吸收过程主要发生在小肠中。通过制剂设计,可以在很大程度上控制药物的体内释放和溶解,从而对其生物利用度产生有效的干预,这也是制剂性能最主要的体现。
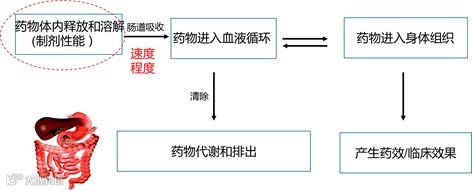
药物在人体内的吸收及作用过程

Tips
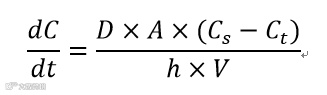
Noyes-Whitney方程
在难溶性药物的增溶措施中,药物晶型起着不可忽视的作用。尤其是对于仿制药质量一致性评价,多晶型更是一个需要重点关注的因素。例如,假设药物的渗透性保持恒定,对于相同晶型而言,控制其粒径分布就可能对制剂溶出产生显著影响。对于不同晶型而言,需要关注其IDR差异,差异大于10%就要当心其生物等效性问题。由于口服药物的吸收窗口主要集中在小肠(约3小时),譬如空腹状态下在胃中溶解的弱碱性药物分子进入小肠后,可能重结晶转变成低溶解度的稳定晶型而导致吸收变差。

在难溶性药物的增溶措施中,药物晶型起着不可忽视的作用。尤其是对于仿制药质量一致性评价,多晶型更是一个需要重点关注的因素。例如,假设药物的渗透性保持恒定,对于相同晶型而言,控制其粒径分布就可能对制剂溶出产生显著影响。对于不同晶型而言,需要关注其IDR差异,差异大于10%就要当心其生物等效性问题。由于口服药物的吸收窗口主要集中在小肠(约3小时),譬如空腹状态下在胃中溶解的弱碱性药物分子进入小肠后,可能重结晶转变成低溶解度的稳定晶型而导致吸收变差。

IVIVC研究流程
不同类型的药物在制剂开发中面临的挑战也是不相同的。对于BCS II类药物而言,其主要挑战在于低溶解度带来的低生物利用度。对于BCS IV类药物而言,其在体内的吸收受到体内溶出和小肠粘膜渗透性的双重影响。另外,对于用难溶性药物的亚稳态晶型开发的制剂产品,还要考虑如何保证亚稳态晶型在制剂中保持足够长时间的稳定性(例如24个月)。
(1) 药物的晶型及其稳定性;
(2) 药物晶型的溶解度;
(3) 药物晶型的固有溶出速率;
(4) 药物晶体颗粒的粒径、性状和流动性;
(5) 药物晶型的吸湿性和可压性;
(6) 辅料的种类和比例;
(7) 表面活性剂的种类和用量;
(8) 崩解剂的种类、比例和内外加方式;
(9) 制剂生产工艺。
如前面提到的,在设计制剂产品的配方时需要对所用成分(原料药和辅料)的关键材料属性(CMA)和关键工艺属性(CPP)进行风险评估,以确定其对关键质量属性(CQA)的影响,并定义出每一个关键变量的可接受范围。对于多晶型药物的制剂设计,同样遵循上述原则。对于原料药和辅料,需要考察的关键质量属性包括:含量、含量均匀性、溶出和杂质。在原料药和辅料中对这些关键质量属性产生影响的因素各不相同,前者涉及晶型、粒径分布、吸湿性、固有溶出速率、流动性、杂质和稳定性,后者包含性状及粒径分布、流动性、溶解度、吸湿性、过氧化物含量、原辅料兼容性以及可压性。

多晶型药物制剂设计的CMA风险评估
当用于制剂的药物晶型确定后,需要考察配方变量对关键质量属性的影响,涉及的考察因素包括粒径分布、原料药含量、填充剂含量、表面活性剂含量、崩解剂含量、润滑剂含量和助流剂含量。

多晶型药物制剂设计的配方因素风险评估
当制剂配方确定后,进入生产工艺开发阶段时就要对生产工艺的选择及风险进行评估,重点关注晶型转变和生产单元两个要素。不同的因素产生的风险高低等级不同,具体的控制方案需要在实践中结合目标和成本等方面进行综合考量。

多晶型药物制剂设计的 生产工艺风险评估
针对多晶型药物制剂开发中的关键问题,李博士在课程中用六个典型案例进行了进一步的深入讲解和分析。由于篇幅所限,本文就不再具体列出这些案例,感兴趣的朋友可点击文末阅读原文观看李博士课程视频回放。
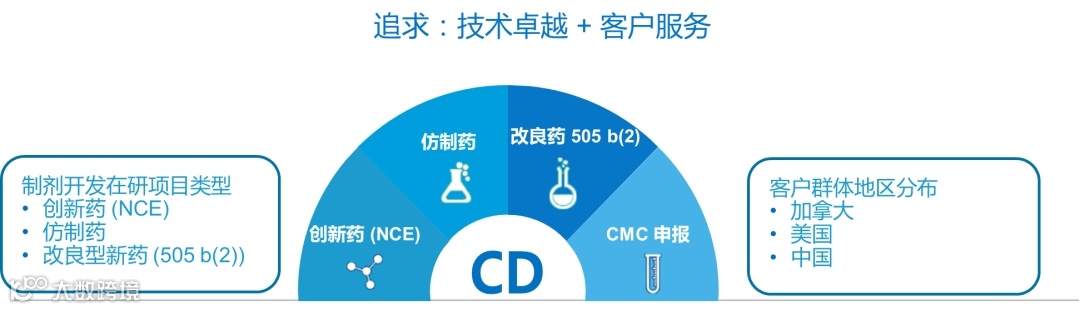
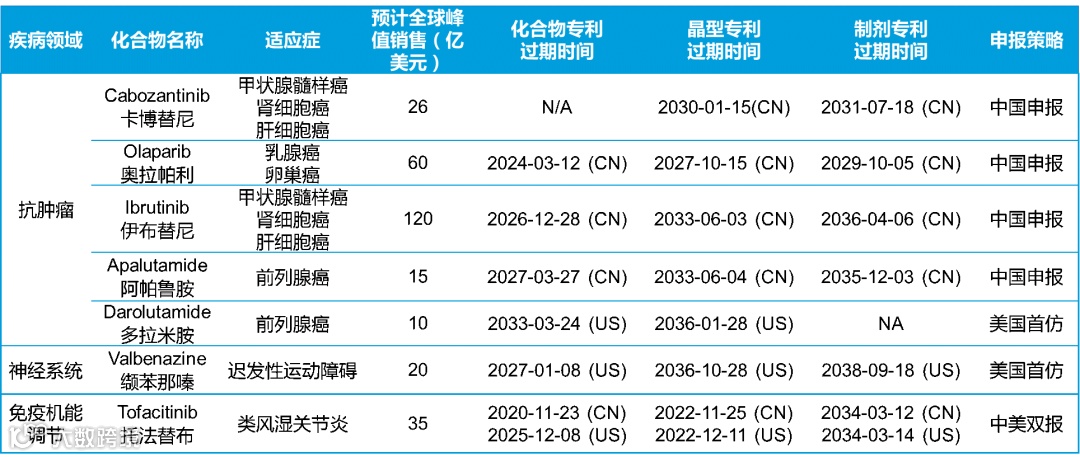
Candoo高端仿制药合作项目

【问答精选】第一期 新药研发中的关键晶型问题
【课程预告】第二期 由工业视角谈药物结晶
【问答精选】第二期 由工业视角谈药物结晶
【课程预告】第三期 药物多晶型,控制策略及其在制剂设计中的应用
【课程预告】第四期 关于突破性治疗药物的CMC及固态研究思考
本公众号
聚焦药物研发,促进分享交流
晶“云”:点评全球药湖风云
晶“耘”:分享晶云技术耕耘
欢迎关注我们!

点击"阅读原文",回看第三期课程



