
如果说前段时间哪部剧最火,小伙伴们十有八九会说到《权游》。维斯特洛大陆上的刀光剑影和阴谋权术,从第一季交织到第七季,演奏出了一个个动人心魄的故事。好不容易迎来了最终季,本期待着烈火与玄冰的相逢将会迸发出怎样的精彩,结果它却烂尾了。。。烂尾了。。。烂尾了。。。
荧幕上的故事结束了,但生活终究还是要继续。话说回来,冰与火这两种属性近乎相反的物质,给人的第一感觉就是无法好好儿相处,正所谓“水(冰)火不容”、“冰火两重天”。文学上借助冰与火这对抽象化的矛盾体来刻画冲突、塑造人物和推动情节,那么现实世界中冰与火又有怎样的故事呢?
说来真巧,这个世界上还真有一种物质融合了冰与火的性质,让二者完美地共存,这就是“可燃冰”。等等,冰能够燃烧?这明显违背常识的事,该不会是在骗人吧?耳听为虚眼见为实,大家可要看仔细咯。

图1. 燃烧的“冰”(USGS Gas Hydrates Lab) [3]
图1中正在燃烧的物质是一种特殊的冰,它主要由水分子与甲烷构成,学名叫做“天然气水合物”(natural gas hydrate),俗称“可燃冰”。可燃冰在外观上与通常的冰没有明显差异,但若设法点着它,则会产生橙色火焰,来源于可燃冰中释放出的甲烷气体的燃烧。
冰与火这一对冤家在可燃冰身上完美地融合在了一起。如此离奇的身世不禁勾起了我们的好奇心。它究竟从何处来,又要到何处去,今天咱们就来一探究竟。

图2. 可燃冰的燃烧[2]

从何处来

笼型水合物最早由Humphry Davy在1811年报道,随后Michael Faraday在1823年确认了其成分。笼型水合物由水分子和其他一些小尺寸的客体分子(通常小于0.9 nm)在低温和高压条件下生成。由于大多数客体分子是气体分子,因此常常又被称为气体水合物(gas hydrate)。
笼型水合物在晶体结构上最大的特征是由水分子构成的“笼子”。水分子之间通过氢键相连,形成具有凸多面体特征的笼型结构。笼子的每一个顶点是一个水分子,每一条棱是连接相邻两个水分子的氢键。笼子内的空腔可以容纳一定大小和数量的客体分子,如甲烷、二氧化碳等。

图3. 水分子形成的氢键“笼子”[6]
水分子之间通过不同的几何连接能够形成不同类型的笼子,它们都满足凸多面体欧拉定理(Euler's convex polyhedra theorem):面数-棱边数+顶点数=2。我们通常用Xn这个符号来区别不同类型的笼子。其中,X表示笼子中某种面的边数,n表示笼子中这种面的数量。例如,512意味着笼子由12个五边形构成,即五边十二面体;51262表示笼子由12个五边形和2个六边形构成。其他类型的笼子以此类推。

图4. 水分子形成的不同类型笼子[7]
不同类型的笼子具有不同大小的空腔,因此可以容纳不同尺寸和数目的客体分子。一般来说,小尺寸的笼子(如512和435663)可以装一个较小的客体分子(如甲烷、二氧化碳和氧气分子等);大尺寸的笼子(如51264和51268)则可以容纳一个较大的客体分子(丙烷、金刚烷等)或者多个较小的客体分子。
笼子内的客体分子与水分子之间主要通过范德华力发生联系。客体分子最主要的作用是填充笼子内的空腔,防止笼子塌陷(尤其是在正压条件下)。这与空纸盒在外力下容易被压瘪是一个道理。但是,笼型水合物晶体中并非每一个笼子都会被客体分子填充。例如,甲烷水合物(可燃冰)通常能够达到的填充率在90%左右,目前已经观察到的最大填充率不超过96%。
不同类型的水分子笼子按照一定的空间对称性规律组合在一起,就会产生笼型水合物晶胞。由于组合方式不同,笼型水合物也存在多晶型现象。最常见的笼型水合物晶型有三种:I型、II型和H型。
每一种水合物晶型都是由两种或以上的水分子笼子构成。比如,I型水合物的每个晶胞中含有2个512笼子和6个51262笼子,可以容纳诸如甲烷、乙烷和二氧化碳等分子。II型水合物的晶胞由16个512笼子和8个51264笼子构成,能够装载丙烷和异丁烷等客体分子。H型水合物的结构相对更复杂一些,每个晶胞中包含有3种类型的笼子(512,3个;435663,2个;51268,1个)。其中,大尺寸的51268笼子里能够填充较大的客体分子,如新己烷和正庚烷。
除了上述3种常见晶型外,笼型水合物还存在其他晶型(TS-I、HS-IQ、S-III等)。结晶过程中具体会生成何种晶型的水合物,一方面取决于客体分子的种类,另一方面受结晶温度和压力等因素的影响。


图5. 三种常见的笼型水合物晶型及主要的客体分子类型[8]
笼型水合物由于其晶体结构不走寻常路,因而具有一些独特的性质。一般而言,液态水对气体的溶解度要远高于固态水(冰)。而一旦生成笼型水合物后,气体在固态水中的“溶解度”会急剧增大,这就为某些种类气体的储存和运输提供了一种新的手段。
笼型水合物通常在低温和高压环境下生成,升高温度或降低压力都会让它们变得不稳定,从而自发分解并释放出气体。这可以解释为什么甲烷水合物(可燃冰)在常温常压条件下一点就燃。但在某些情况下,笼型水合物的分解会在其表面产生一层冰晶体并阻碍气体分子向外扩散,从而反常地提高水合物的稳定性(self-preservation效应)。

到何处去

笼型水合物种类繁多性质独特,是科学研究中的宠儿。这个家族中的绝大多数成员都诞生于实验室中,在自然界里难觅踪迹。但有一位成员不仅在自然界中分布十分广泛,而且与工业生产以及我们的日常生活关联密切,这就是甲烷水合物,又叫天然气水合物,俗称可燃冰。
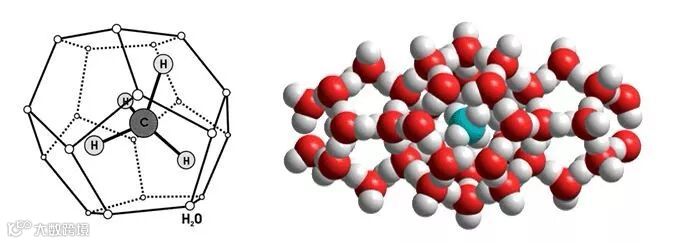
图6. 甲烷水合物晶型I [7, 10]
甲烷水合物能够以前面介绍的3种常见晶型存在,即晶型I、II和H。当压力在120 MPa以下时,晶型I是最主要的形态。压力超过120 MPa后,晶型I转变为晶型II。当压力升高到约600 MPa时,晶型II转变为晶型H。继续升高压力至3 GPa,水合物分解生成固态甲烷和冰(晶型VII)。
甲烷水合物的生成需要较低的温度(一般接近0 ºC或以下)和中等以上的压力(通常大于0.6 MPa),当然还要有充足的甲烷来源。目前地球上自然存在的甲烷水合物主要分布在两种地质环境中——靠近大陆边缘水深几百米的海底,以及靠近北极的永久冻土层。这两种地质条件能够提供足够的低温和压力,同时有相对丰富的甲烷来源,因此孕育了地球上绝大多数的甲烷水合物矿藏。
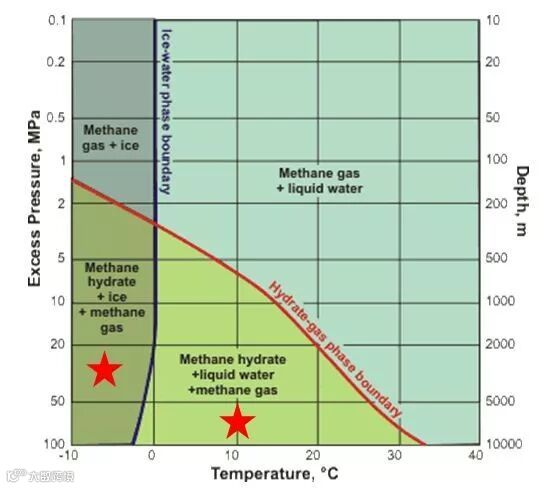
在自然界中,约99%的甲烷水合物存在于大陆边缘海底的沉积物中,水深通常有500米或更深。这里的沉积物中含有大量的有机碳化合物,通过微生物分解产生甲烷。同时从海床下更深处的天然气矿层中还可能有甲烷通过裂缝溢出。这些甲烷与寒冷高压的海水接触后生成水合物晶体。相比之下,只有一小部分甲烷水合物存在于永久冻土层中,它们多产生于数十万年前的冰川时期。这些永久冻土层大多数分布在阿拉斯加和西伯利亚地区。
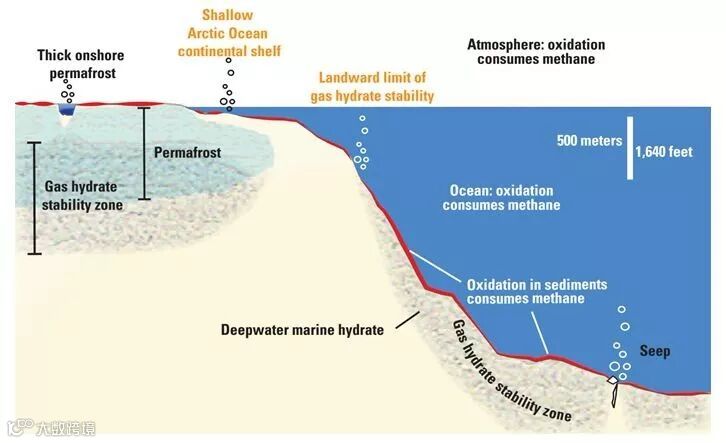
甲烷水合物是一种新的天然气来源。一千克甲烷水合物在常温常压条件下完全分解后大约能产生190升甲烷气体。从20世纪80年代开始,对于地球上天然存在的甲烷水合物的研究及开采利用逐渐增多。到目前为止的研究表明,甲烷水合物在地球上分布广泛,几乎全球所有大洲都有储量。其储存的甲烷折合成标准状态下的体积约为3~24.8×1015立方米,远高于传统形式的天然气矿藏。由于储量巨大,甲烷水合物已成为未来最有希望的清洁能源之一。

与传统形式的天然气矿藏相比,甲烷水合物由于其生成条件特殊且性质独特,开采手段也有所区别。针对甲烷水合物晶体在高温或低压条件下不稳定的特点,可以向矿井中注入热水或热蒸汽(thermal injection),使水合物分解从而释放甲烷;也可以采用减压的方法促进水合物分解。另一种手段是向矿井中注入水合物抑制剂(如甲醇盐水),破坏水合物晶体的氢键网络并释放甲烷气体。除上述方法外,还可以利用二氧化碳水合物比甲烷水合物更稳定的特点,用二氧化碳将甲烷置换出来。

尽管甲烷水合物是现在新兴的一种能源形式,但人类与之打交道的历史比其作为能源的历史要早得多。在传统的石油天然气开采过程中,油气管道中常常会出现油/气/水的多相流动。当温度压力条件合适时,管道中就会大量生成水合物晶体并造成管道堵塞。其中一种可能的情形是,石油中挟带着大量乳化的水滴,当水滴与天然气接触后逐渐转变为水合物晶体颗粒并最终聚并在一起堵塞管道。


据统计,全球石油工业每年在处理由水合物生成而导致的管道堵塞问题上的花费以十亿美元计。为了防止在油气开采和输运过程中产生水合物,一种常用的做法是向管道中加入水合物抑制剂,包括热力学抑制剂、动力学抑制剂和抗凝聚剂。
热力学抑制剂最常用的是甲醇和乙二醇。它们会改变水合物的相图,使水合物的生成需要更低的温度和更高的压力,从而避免在通常条件下产生水合物晶体。动力学抑制剂主要是一些水溶性高分子,其作用的基本原理是抑制水合物晶体的成核和生长。抗凝聚剂一般使用的是表面活性剂类的物质,如季铵盐等。它们能够阻止水合物晶体颗粒的聚并和结块,确保油气管道中有足够的流动性。
甲烷水合物除了会堵塞石油天然气管道造成损失外,还可能引发地质灾害。在近海海床的沉积物中存在巨量的甲烷水合物。在正常条件下,这些水合物稳定且坚固,能够有效地支撑海底沉积物。若这些水合物由于某些原因发生分解,原先坚固的海底沉积物就会因为失去支撑而崩塌,造成海底滑坡。同时,这个过程中会释放出大量的甲烷,导致大范围的海底天然气渗漏,对局部的海洋化学环境产生显著影响(例如海水酸化),甚至引发生态灾难。

图12. 海底沉积物中的甲烷水合物(电子显微镜照片) [17]
能够引起海底甲烷水合物分解的原因有很多,既有自然因素也有人为因素。海底地震甚至全球变暖导致的海水升温都有可能使水合物变得不稳定并诱发分解。由于甲烷水合物一般都存在于较浅的海底(通常水深几百米),人类的活动如海底钻探和管道铺设等有可能会降低海底沉积物的地质稳定性,进而导致水合物分解。

图13. 海底甲烷渗漏形成气泡流[11]
甲烷水合物被禁锢在海底,已经沉睡了成千上万年。看似与世无争,但实则是个不安定的家伙。全球气候变暖使得海水升温、永久冻土层消融,原本稳定的甲烷水合物受其影响正变得越来越躁动不安。甲烷一旦被释放到大气中,就会加剧温室效应,从而进一步让地球升温。

图14. 常见温室气体:水蒸气、氮氧化物、二氧化碳、甲烷[26]
“温室效应”是导致全球变暖的一个重要因素。地球大气层对于来自太阳的短波辐射几乎是透明的。地表被太阳短波辐射加热后,以长波辐射的形式向外释放热量。如果没有大气层,这些长波辐射会重新回到宇宙空间中。地球大气中的二氧化碳、氮氧化物、甲烷以及水蒸气等气体会强烈地吸收地表的长波辐射,使大气变暖,对地表产生保温作用,这就好比给地球盖上了一层保暖的被子。与二氧化碳等气体相比,甲烷是一种“超级温室气体”,其产生的温室效应是相同体积二氧化碳的15至20倍,这可能相当于薄凉被和加厚羽绒被的区别。

图15. 温室效应:温室气体吸收地面长波辐射使近地面大气升温[27]
当前大气中的甲烷只占温室气体的很小一部分(约2%),对温室效应的影响还不显著。但不可忽视的是,甲烷水合物中保存了地球上全部碳元素的10%~15%,就像一颗不定时的炸弹。当水合物不稳定时,这些巨量的甲烷就可能被释放进入到全球碳循环中,从而对地球气候和生态产生剧烈影响。现阶段的科学模型还难以准确预测这一过程的可能性大小和进展快慢,但毫无疑问这是悬在人类头顶上的一柄达摩克里斯之剑。也许,地球上很难找到第二种晶体像甲烷水合物一样,其稳定性对人类的生存具有如此显著的影响。
后记
可燃冰的故事到这里就暂时告一段落了。它就如希腊神话中的Janus一样有着多副面孔,既讨人喜欢,又让人畏惧,就像冰与火这两种截然相反的性质却在它身上完美融合一样。维斯特洛大陆上的冰与火之歌已迎来最终章,但现实世界里的冰与火之歌则会继续书写属于它的传奇。
参考资料
1.Sloan E D and Koh C A. Clathrate Hydrates of Natural Gases (3rd ed.), CRC Press, 2008.
2.Demirbas A. Methane Gas Hydrate, Springer, 2010.
3. https://geology.com/articles/methane-hydrates/
4.Davy H. Philos. Trans. R. Soc. Lond. 1811,101: 1-35.
5.Faraday M. Philos. Trans. R. Soc. Lond. 1823, 113: 160-165.
6.Ludwig R. Angew. Chem. Int. Ed. 2001, 40: 1808-1827.
7.http://www1.lsbu.ac.uk/water/clathrate_hydrates.html
8.Sloan E D. Nature 2003, 426: 353-359.
9.Koh C A. Chem. Soc. Rev. 2002, 31: 157-167.
10. Beauchamp B. C.R. Geoscience 2004, 336: 751-765.
11.Gas Hydrate in Nature, from U.S. Geological Survey (USGS), 2018.
12.Collett T, et al. J. Chem. Eng. Data 2015, 60: 319-329.
13.Sum A K, et al. Ind. Eng. Chem. Res. 2009, 48: 7457–7465
14.Makogon Y F. J. Nat. Gas. Sci. Eng. 2010, 2: 49-59.
15.Boswell R, et al. Methane Hydrates in Future Energy, Elsevier, 2014.
16.Ruppel C and Kessler J. Rev. Geophys. 2017, 55: 126-168.
17.The U.S.Geological Survey’s Gas Hydrates Project, from U.S. Geological Survey (USGS), 2018.
18.Natural Gas Hydrates—Vast Resource, Uncertain Future, from U.S. Geological Survey (USGS), 2001.
19.Englezos P. Ind. Eng. Chem. Res. 1993, 32: 1251-1274.
20.Kvenvolden K A. Rev. Geophys. 1993, 31: 173-187.
21.Chou I-M, et al. P. Natl. Acad. Sci. USA 2000, 97: 13484–13487.
22.Servio P, et al. Top. Catal. 2005, 32: 101-107.
23.Ruppel C. Elements 2007, 3: 193-199.
24.Ruppel C. Nat. Edu. Knowledge 2011, 3: 29-39.
25.Li X-S, et al. Appl. Energ. 2016, 172: 286-322.
26.https://climate.nasa.gov/causes/
27.http://www.esa.int/kids/en/Multimedia/Paxi_animations/English/The_greenhouse_effect
本公众号
聚焦药物研发,促进分享交流
晶“云”:点评全球药湖风云
晶“耘”:分享晶云技术耕耘
欢迎关注我们!



