苏州晶云主办的CMC系列线上课程将于2020年4月17日-5月22日在药渡大学平台上线。课程邀请国内外药物研发领域知名专家进行分享和互动。点击图片查看课程详情。
第五期课程回顾
无定形药物和固体分散体
随着药物筛选技术的不断发展,基于新靶点的化合物结构越趋复杂,开发管线中难溶性候选药物分子所占的比重也越来越大,溶解性问题愈发成为制约一款药物能否顺利开发和最终成功上市的重要因素。在学术界和工业界持续的理论研究及实践探索中,涌现出了多种多样的药物增溶手段。其中无定形药物是近年来发展迅猛的一项新技术,在难溶性药物增溶领域展现出了广阔的应用前景。

内容导览
难溶性药物与无定形制剂
无定形药物的分子运动与结晶因素
无定形固体分散体
固体分散体的物理稳定性
固体分散体的溶出行为
难溶性药物与无定形制剂
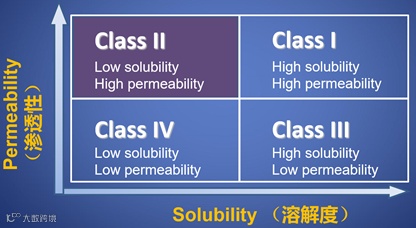
BCS 分类系统
改变处方工艺
降低药物粒径 (如采用微粉化、纳米晶体或使用崩解剂等措施),使用微粒给药系统 (如常见的脂质体纳米粒和胶束等)
改变化学性质
将药物成盐、形成离子化前药或者制备成可溶性包合物 (如环糊精包合物)等
改变固体形态
将药物制备成亚稳态晶型、共晶、溶剂合物或者无定形等

结晶态SiO2 (石英)与无定形态SiO2 (玻璃)

(Chen X, et al. J. Am. Chem. Soc. 2002)
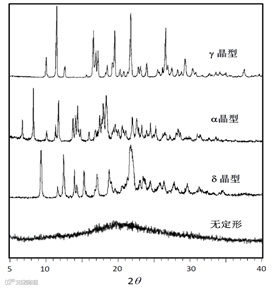
吲哚美辛的结晶态与无定形态
ΔGV = G2 – G1 = RTln(C2/C1)
ΔGV = (ΔHf•ΔT•T)/Tm^2
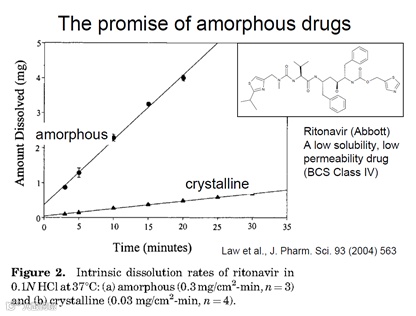
利托那韦无定形态与结晶态的溶出速率比较
(Law D, et al. J.Pharm. Sci. 2004)



无定形罗替戈汀透皮贴剂的结晶现象
(Rietveld I B and Ceolin R. J. Pharm. Sci. 2015)
无定形药物的分子运动与结晶因素

无定形药物结晶过程中的自由能变化
受分子量、构象熵、刚性和对称性等因素的影响,不同的药物分子其自身结晶趋势可能会存在显著差异。利用循环DSC测试,可以将药物按自身结晶趋势的强弱分为三类:
结晶趋势强 (Class I,高风险),熔体降温过程中即发生结晶;
结晶趋势中等 (Class II),熔体降温过程中不发生结晶,二次升温中发生冷结晶;
结晶趋势弱 (Class III,低风险),熔体降温及二次升温过程中均不发生结晶。

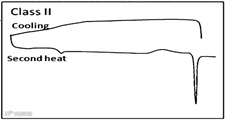
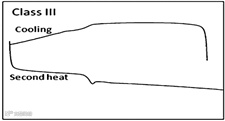
药物自身结晶趋势的分类
(Baird J A, et al. J.Pharm. Sci. 2010)
温度是影响无定形药物结晶行为的一个重要因素。一般来说,随着温度的升高,药物分子运动能力增强,结晶能力会随之提高。具体而言,在不同的温度区间内药物的结晶机理有所不同,因此具体的结晶行为也会有差异。
以灰黄霉素 (Griseofulvin)为例,在玻璃化转变温度以下是玻璃态晶体生长机制,在中间温度范围内晶体生长受分子扩散控制,在高温下晶体生长则主要受热力学控制。

不同温度下无定形灰黄霉素的结晶速率
(Shi Q, et al. Cryst.Growth Des. 2016)
相同条件下同种药物的不同晶型可能表现出不同的结晶动力学特征,从而对无定形药物的结晶行为产生显著影响。
以灰黄霉素为例,其三种已知晶型 (Form I/II/III)在无定形态下生长的结晶动力学存在显著差异,其中Form I和Form II的结晶速率在某些温度下可相差100倍之多。

灰黄霉素三种晶型的生长动力学
(Su Y, et al. Chem.Commun. 2018)
表界面因素对无定形药物结晶的影响主要体现在,位于体相和表面的药物分子在运动能力上存在显著差异,从而导致截然不同的结晶行为。
一般而言,位于无定形药物表面的分子在运动时所受到的限制相较于体相分子要小得多,因此其结晶能力更强,从而在无定形药物的表面出现快速结晶行为。
一旦发生表面结晶,一方面晶体可能继续向体相中生长最终使整个样品发生结晶,另一方面在无定形药物表面的晶体会阻碍药物释放,削弱无定形药物的增溶效果。
仍以灰黄霉素为例,当其处于玻璃态时,分子在表面的扩散速率要比在体相中的扩散速率快好几个数量级,使得分子在表面发生快速扩散并导致晶体的快速生长。除了玻璃态样品的外表面,其内部的裂纹也会产生新的固-气相界面,促进药物结晶。此外,在过冷液体中若存在气泡,由此产生的液-气相界面也会导致晶体快速生长。


表界面对无定形灰黄霉素结晶的影响
(左:玻璃态;右:过冷液体)
(Shi Q, et al. Cryst.Growth Des. 2016)
因此,表界面的存在会显著加快无定形药物的成核和结晶速率,从而降低无定形药物的物理稳定性。无论是在过冷液体中的液-气相界面,或是玻璃态中的固-气相界面,在无定形药物开发过程中都应予以关注。
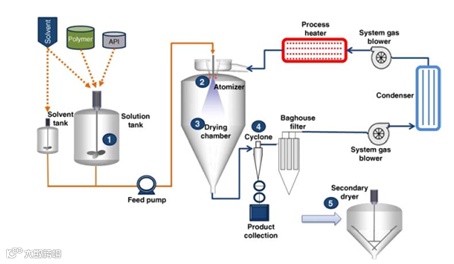
无定形药物的加工工艺对其物理稳定性和结晶行为有不可忽视的影响。根据不同的原理,无定形药物的常见制备途径有:
破坏晶格 (研磨、机械力作用)、溶液析出 (喷雾干燥、反沉淀)、熔融冷却 (热熔挤出)和升华凝华 (气相沉积)等。
不同的制备途径可能会影响到无定形药物的微观结构,进而影响其稳定性。例如,用冷冻研磨法制备的无定形辛伐他汀 (Simvastatin)在1天内就会迅速结晶,而通过熔融冷却方法制备的无定形则能在42天内保持稳定。
除加工工艺的影响外,制剂工艺过程中导致的无定形药物结晶也是不可忽视的。
具体来说,粉碎过程中的机械力和热量等因素以及增加的表面积可能导致结晶加速;混合过程中辅料的影响 (包括辅料中含有的水分等以及与环境中水分接触等因素)可能导致结晶加速;湿法制粒中的水分和干法制粒中的压力因素可能导致结晶加速;压片过程中机械力和热量可能诱导结晶;包衣过程中的溶剂、温度和包衣材料等因素也会影响药物结晶。
无定形药物的结晶包括成核和晶体生长两个阶段。成核速率是其中需要考量的一个重要因素。
经典成核理论认为药物分子会通过运动和碰撞相互结合形成团簇,当团簇超过一定的临界尺寸时会形成晶核,最终生长形成晶体,而未达到临界尺寸的核会溶解,所以成核是一个动态过程。
成核速率受温度、晶型、表界面 (异相成核)、水分和添加剂等因素的影响。
由于在药物的生产和储存过程中水分几乎无处不在,其对无定形药物结晶行为的影响也需要认真考量。
通常认为无定形药物相比于结晶态药物具有更多的自由体积,因此具有更强的吸湿性。

无定形和结晶态吲哚美辛的吸湿能力
(Andronis V, et al. J. Pharm. Sci. 1997)
水分对无定形药物结晶的影响主要是通过塑化作用。水分可以看做是一种极强的塑化剂,它能够加快分子运动,加快分子初级、次级弛豫以及扩散等,从而加速无定形药物的体相和表面结晶。
水分对分子运动性的影响可以通过测定分子弛豫时间来进行定量研究。
经验结论是,1%的吸水就可能使分子运动性加快两个数量级。因此严格控制无定形药物的含水量是保持其物理稳定的一种重要手段。
前面已经提到,影响无定形药物结晶行为的因素有很多,它们有各自不同的作用机理。
其中,通过加入辅料和添加剂来抑制药物结晶以获得稳定的无定形药物制剂,是目前研究和应用的一个主流方向,即通常所说的无定形固体分散体 (Amorphous Solid Dispersion,ASD)。
无定形固体分散体

各代固体分散体的特点

FDA批准的固体分散体药物
(张杰,蔡挺.药学进展,2018)
固体分散体的处方和制备
聚乙烯吡咯烷酮 (如PVP K30)
无定形聚合物,易与药物发生氢键相互作用,粘度较大,抑制药物结晶能力较强
乙烯吡咯烷酮-醋酸乙烯酯共聚物 (如PVP VA64)水溶性高分子,吸湿性较低,可用于替代PVP
聚乙烯己内酰胺-聚醋酸乙烯酯-聚乙二醇接枝共聚物 (商品名SOLUPLUS)
特点是玻璃化转变温度低,毒性小,热稳定性好,是一种新型固体增溶剂,可作为非离子型表面活性剂
醋酸羟丙甲纤维素琥珀酸酯 (HPMCAS)
具有两亲性和pH依赖性,具备较好的抑制药物结晶的能力。
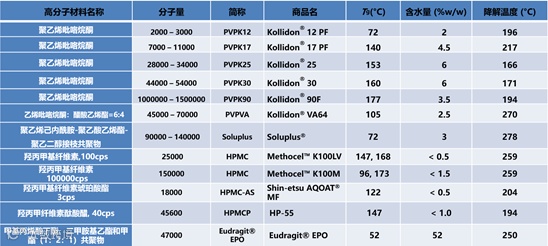
固体分散体常用高分子载体的基本性质

固体分散体工业化制备方法的决策图
固体分散体的物理稳定性

无定形固体分散体的相分离和结晶


典型的药物-高分子二元相图
(Huang Y and Dai W-G. Acta Pharm. Sin. B 2014)
在理想的无定形固体分散体中,药物与高分子在分子尺度上均匀混合,形成一个均相“溶液”。因此可以通过药物与高分子之间的互溶性来评估无定形固体分散体的物理稳定性。
一种常用的手段是借助于Flory-Huggins理论,通过特征的相互作用参数来判断药物与高分子之间的相互作用强弱以及互溶性。
具体操作如下:
1. 首先利用熔融焓和熔融温度等热力学参数来估算药物在高分子载体中的活度,
ln a = (ΔHm/R)(1/Tm – 1/T)
其中ΔHm和Tm分别代表纯药物晶体的熔融焓和熔融温度,T代表药物在高分子载体中的溶解温度 (可通过测试熔点降低来获得,melt point depression)。
2. 通过Flory-Huggins理论对获得的活度进行拟合,
ln a = ln vdrug + (1 – 1/x)vpolymer + χvpolymer^2
其中vdrug和vpolymer分别代表药物和高分子的体积分数 (假设体积分数与质量分数相等),x代表高分子与药物的分子量比值,χ即是Flory-Huggins相互作用参数,该参数可反映药物和高分子的相互作用强弱和互溶性。
通常来说,χ值为负值 (表示药物与高分子之间具有一定的相互作用),且绝对值越大表明二者之间的相互作用就越强,互溶性就越好。
例如,硝苯地平与PVP K12、PVP VA64和PVAc三种高分子的相互作用参数分别为-2.5 ± 0.2、-1.8 ± 0.2和-0.02 ± 0.2,表明三种高分子与硝苯地平的互溶性顺序为PVP K12 > PVP VA64 > PVAc,因此使用PVP K12作为载体制备的无定形固体分散体的物理稳定性将会优于其余两种高分子。


利用高分子来稳定无定形药物的机制
固体分散体的溶出行为

固体分散体溶出过程的物理图像


固体分散体溶出过程中的结晶途径
(Alonzo D E, et al. Pharm. Res. 2010)

固体分散体溶出过程中,维持溶液中较高的过饱和度是提高生物利用度的关键。
固体分散体中的高分子载体经常可以抑制溶出过程结晶或相分离,稳定过饱和溶液中液体/液体或无定形相/液体的相分离,抑制过饱和溶液结晶等作用。
固体分散体的溶出行为与载药量、溶出过程中的表界面、固体分散体的均匀性、高分子性质、药物-高分子相互作用等因素密切相关。
表面活性剂可能会增强过饱和体系的稳定性从而提高生物利用度,也有可能与高分子发生竞争性的相互作用,从而降低过饱和体系的稳定性和固体分散体的增溶效果。


【课程回顾】第三期 药物多晶型,控制策略及其在制剂设计中的应用
【问答精选】第三期 药物多晶型,控制策略及其在制剂设计中的应用
【课程回顾】第四期 关于突破性治疗药物的CMC及固态研究思考
【问答精选】第四期 关于突破性治疗药物的CMC及固态研究思考
本公众号
聚焦药物研发,促进分享交流
晶“云”:点评全球药湖风云
晶“耘”:分享晶云技术耕耘
欢迎关注我们!

点击"阅读原文",回看第五期课程