点击上方刊名关注我们↑↑↑
PI3K/AKT/mTOR信号通路对细胞的增殖、分化和凋亡等过程起着重要作用,在许多肿瘤细胞中存在过度激活的现象,并被发现可促进肿瘤细胞耐药性的产生。而抑制该信号通路的激活能够促进肿瘤细胞凋亡,也能恢复肿瘤细胞对药物的敏感性。因此,开发小分子PI3K/AKT/mTOR信号通路抑制剂成为抗肿瘤药物的研究热点之一。去氢枞酸(DHA)是一种重要的三环二萜类天然树脂酸,也是传统中药松香的成分之一,主要由松香经歧化反应后分离获得。其性质稳定且具有与甾类分子类似的结构,目前已被广泛用于荧光试剂和药物中 间体的合成与开发。去氢枞酸及许多它的衍生物表现出良好的抗肿瘤活性。近期报道显示,去氢枞酸的1H苯并[d]咪唑类衍生物对PI3Kα有抑制效果,能够下调磷酸化AKT的表达。我们的研究也发现,部分B环改性的去氢枞酸衍生物能够降低磷酸化的PI3K、AKT、mTOR表达水平,同样也能降低其下游效应器S6和4EBP1的磷酸化水平。虽然不同去氢枞酸衍生物对PI3K/AKT/mTOR信号通路蛋白表现出了一定的抑制作用,但去氢枞酸本身是否具有相应的抑制能力,目前尚不清楚,有待进一步的研究。
大多数化合物通过与蛋白分子的结合产生效应作用,其结合模式和结合能力可通过蛋白晶体解析和蛋白荧光猝灭等手段来验证,但实验周期较长,成本较高。分子对接技术是一种利用计算机进行理论计算预测化合物与受体蛋白结合情况的手段,可根据对接结合能的大小判断化合物与蛋白的结合能力,筛选出潜在的蛋白调节剂;也可通过所得的对接构像和其他的对接评分进行初步的机理研究。此外,了解化合物在人体的吸收、分布、代谢、排泄和毒性等类药性和药代动力学特性可以判断其是否可作为临床治疗的候选化合物。为了降低研究成本,计算机辅助程序已逐渐被用于类药性和药代动力学的初步研究。
因此,本研究利用分子对接技术预测去氢枞酸与该通路关键蛋白的结合能力和结合方式,并用蛋白免疫印迹法验证去氢枞酸的实际抑制情况,进一步利用网络服务器进行类药性与药代动力学的模拟,以初步了解去氢枞酸作为PI3K/AKT/mTOR信号通路抑制剂的潜力,为进一步开发去氢枞酸提供理论依据。


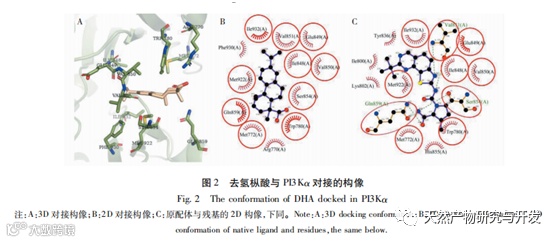


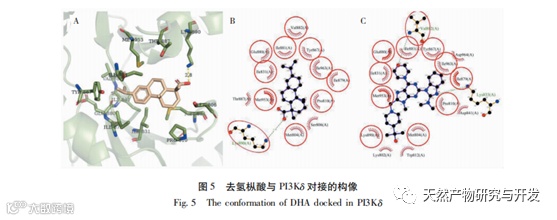

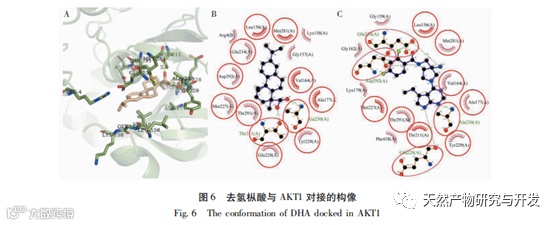






PI3K/AKT/mTOR信号通路对细胞的增殖、分化和凋亡等过程起着重要作用,也是癌症治疗的靶点之一。PI3K主要由催化亚基p110和调控亚基p85构成,经磷酸化激活后,可将其底物3 ,4-二磷酸磷脂酰肌醇(PIP2)转化成3,4,5-三磷酸磷脂酰肌醇(PIP3)。PIP3能够与AKT结合后通过磷酸肌醇依赖性蛋白激酶1(PDK1)促使AKT磷酸化。经磷酸化激活的AKT能够直接或间接的使mTOR磷酸化,从而进一步促进下游效应蛋白4EBP1和S6的磷酸化以调控细胞内生化活动。
本研究基于近年来去氢枞酸抗癌衍生物不断被开发,部分衍生物被报道对PI3K/AKT/mTOR信号通路的部分关键蛋白有抑制作用。为了研究作为原料的去氢枞酸对PI3K/AKT/mTOR信号通路的影响,为去氢枞酸抗癌衍生物的开发提供依据。利用分子对接技术预测了去氢枞酸对通路关键蛋白PI3K、AKT和mTOR的ATP结合位点的结合能力和结合方式,利用蛋白免疫印迹法检验去氢枞酸对通路的抑制效果,通过初步的类药性和药代动力学模拟预测去氢枞酸成为口服药物的潜力。
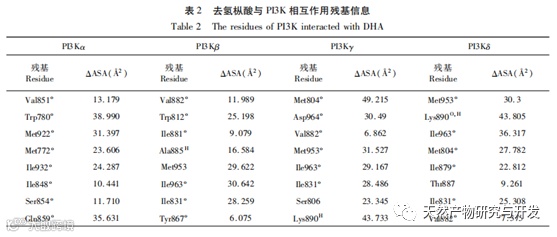
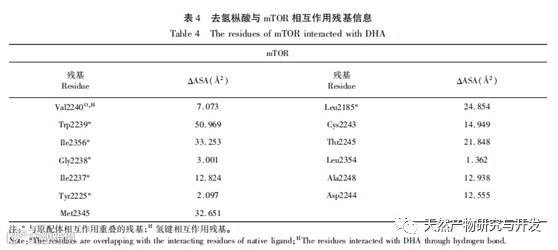
分子对接结果表明,去氢枞酸对各关键蛋白的ATP结合位点均有一定的结合能力,与AKT3的结合最弱,最低结合能为-6.16kcal/mol,与AKT1结合最强,最低结合能为-8.04 kcal/mol。去氢枞酸对通路蛋白的结合能力弱于作为高效抑制剂的原配体, 与我们已合成得到的去氢枞酸基PI3K/AKT/mTOR信号通路抑制分子DBDA相近。在ATP结合位点中,去氢枞酸与蛋白的相互作用残基多为含疏水性残基。除了PI3Kδ的Lys890,其他对配体-蛋白结合起最重要作用的关键残基也均为疏水性残基。说明去氢枞酸可能通过与ATP结合位点的腺瞟吟区结合从而产生抑制作用。各蛋白与去氢枞酸的相互作用残基跟原配体的有着大量的重叠,这表明去氢枞酸可能是以和原配体相近的方式与ATP展开竞争以抑制蛋白作用。此外,没有氢键存在的构像,如去氢枞酸与PI3Kα、AKT2和AKT3,它们的结合能均高于其他存在氢键的构像,这表明氢键对去氢枞酸与蛋白的稳定结合发挥着重要作用。在去氢枞酸结合的构像中,氢键全部在羧基位置产生。但是,异丙基和苯环附近存在多个在原配体中为氢键相互作用的重叠残基。这一特征提示,在设计新的去氢枞酸基PI3K/AKT/mTOR信号通路抑制剂时,可加强羧基位置的亲水能力,并在异丙基和苯环位置引入亲水基团,可能可以提高新化合物与蛋白的结合能力。
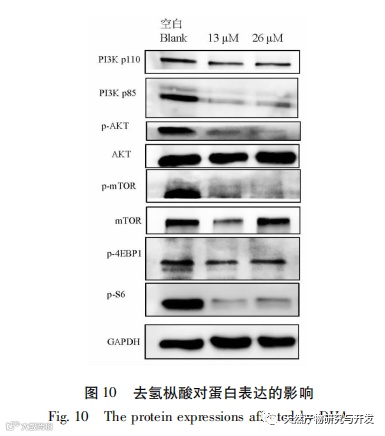
蛋白免疫印迹实验显示,SCC9细胞经去氢枞酸处理后,PI3K调控亚基p85的表达明显降低。p85含量的减少可能使PI3K的生成受阻,并成为减少PI3K下游蛋白AKT磷酸化表达的因素之一。AKT 和mTOR的总蛋白在不同浓度的去氢枞酸作用下与空白组相比没有明显的变化,但其磷酸化蛋白表达均明显减少,说明AKT和mTOR的磷酸化进程受到抑制。处于mTOR下游的4EBP1的磷酸化表达下降较少,可能是因为4EBP1还可经MEK/Erk信号通路激活的原因。而受mTOR调控的另一效应蛋白S6K1下游的S6磷酸化表达明显减少,可能是因为mTOR的磷酸化受阻,导致S6K1激活减少, 从而减少了S6的磷酸化反应。总的来说在SCC9细胞内,PI3K/AKT/mTOR信号通路的表达受到了去氢枞酸的抑制,这与分子对接中预测的结果一致。
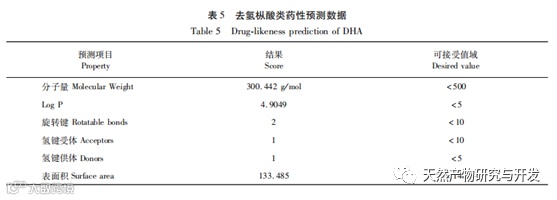
类药性和药代动力学预测中,去氢枞酸的五倍率法则(Lipinski rule of five)分析显示,其分子量、LogP、旋转键、氢键受体、氢键供体的值均在该经验性规则要求的范围内。药代动力学预测对去氢 枞酸在体内的吸收、分布、代谢、排泄和毒性等性能进行模拟,去氢枞酸通过了大部分的测试,说明它可能可以较好的在体内发挥药物作用。
总之,本研究通过分子对接预测、蛋白免疫印迹实验、类药性检验和药代动力学预测,发现去氢枞酸本身可能成为一种候选的治疗药剂,用于抑制PI3K/AKT/mTOR信号通路,以达到缓解肿瘤细胞耐药和抗肿瘤的目的。也可以进一步对去氢枞酸的结构进行修饰,以开发出更有效的去氢枞酸基PI3K/AKT/mTOR信号通路抑制剂。该研究成果发表在《天然产物研究与开发》2021年第4期,欢迎引用(点击左下方“阅读原文”可查看全文)。
引用格式:
李翠萍,陈乃源,李昕宇,等.基于计算机模拟技术分析去氢酸作为PI3K/AKT/mTOR信号通路抑制剂的潜力[J].天然产物研究与开发,2021,33:543-553,576.
Li CP,CHEN NY,Li XY,et.Analysis of the potentiality of dehydroabietic acid as PI3K/AKT/mTOR signaling pathway inhibitor based on computational simulation[J].Nat Prod Res Dev,2021,33:543-553,576.

长按二维码
关注公众号
获取更多内容

电话:028-85210304
官网:http://www.trcw.ac.cn
 点击阅读原文可查看全文
点击阅读原文可查看全文


