(一)丹诺瑞韦+PR方案
丹诺瑞韦(Danoprevir,DNV)为第二代NS3/4蛋白酶抑制剂,入选国家十三五“重大新药创制”科研专项,可抑制丙型肝炎病毒蛋白转录和加工,为多基因型,其疗效、耐药屏障、安全性、药物相互作用较第一代更具优势。
在亚洲慢性丙型肝炎(CHC)人群(包括中国台湾、韩国和泰国)中进行的丹诺瑞韦+PR三联方案的疗效和安全性验证性研究(DAPSANG研究)显示:治疗亚洲基因1b型非肝硬化和肝硬化CHC患者,分别实现97%和92%的SVR12率;其中,治疗中国台湾基因1型非肝硬化和肝硬化CHC患者,可分别获得94%和91%的SVR12率;值得一提的是,治疗中国台湾基因1b型非肝硬化CHC患者,100%实现SVR12,且疗效不受IL28B CC基因型影响(图2)。

图2. DAPSANG研究:台湾基因1b型CHC患者SVR12率
在中国基因1型、初治、非肝硬化慢性丙型肝炎患者中开展的疗效和安全性确证性研究(CTR20150846研究)显示,除1例患者退出外,其余69例患者均于治疗4周和9周获得快速病毒学应答(RVR),获得了100%治疗终点(EOT)病毒学应答率,完成12周治疗并结束4周随访的持续病毒学应答(SVR4)率高达99%(图3)。

图3. CTR20150846研究:病毒学应答率
(二)丹诺瑞韦+瑞维达韦方案
瑞维达韦(Ravidasvir,RDV),为第二代NS5A抑制剂,被国家食品药品监督管理总局药品评审中心纳入的首批优先审评药物之一,且位列DAA第一位,可抑制丙型肝炎病毒复制和装配,为泛基因型,具有高抗病毒活性,对常见耐药突变敏感性好,与第一代相比,其安全性更好。
在台湾基因1型非肝硬化初治慢性丙型肝炎患者中开展的一项多中心、开放、单臂Ⅱ期试验(EVEREST研究)纳入38例患者,主要研究终点是SVR12;结果显示:所有基因1型患者均完成12周丹诺瑞韦+瑞维达韦治疗,其中31例完成12周随访,治疗终点(EOT)病毒学应答率及SVR12率均高达100%(图4);无患者因不良事件退出研究,也无治疗相关严重不良事件的报告。
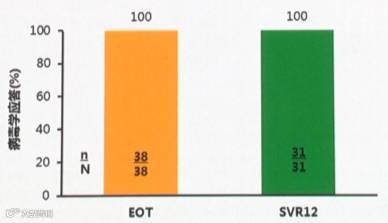
图4. EVEREST研究:EOT和完成12周随访患者的病毒学应答率






相关阅读:



![[APASL STC名师讲演]魏来教授:中国原研DAA 12周治愈更多丙型肝炎患者](https://cdn.10100.com/user/6be31991bfddefed71a23dae399b1f67.png?x-oss-process=style/180x)











