
各位专家同道好,本期CHESS月评(第三十五期)将分享上月PubMed发表的门静脉高压诊疗领域5篇文献(诊断监测3篇和多学科治疗2篇)。本期特邀月评专家:广州市第一人民医院放射科高强教授、保定市人民医院消化科秦维教授和南方医科大学基础医学院徐濛博士。


Tapias EA, Ardevol A, Garcia-Guix M, et al. Short-term hemodynamic effects of β-blockers influence survival of patients with decompensated cirrhosis. J Hepatol. 2020
该研究共纳入403例无出血史的高危食管静脉曲张肝硬化患者,其中190例失代偿期患者和213例代偿期患者,在开始使用β受体阻滞剂前及在治疗1~3个月后(短期)进行全身和肝脏血液动力学评估。
结果表明,失代偿期患者的门静脉压力高于代偿期患者,且处于高动力状态,心输出量(CO)较高、动脉压较低。在β受体阻滞剂作用下,失代偿患者的门静脉压力相比代偿期患者的降幅较低(10±18% vs 15±12%,P<0.05),而心率(P<0.001)和CO降幅更大(17±15% vs 10±21%,P<0.01)。
对于使用β受体阻滞剂的失代偿期肝硬化患者,死亡者与幸存者相比的CO下降幅度更大(21±14% vs 15±16%,P<0.05),且CO可作为独立的死亡预测因素,具有良好的诊断价值(C指数=0.74,95%CI:0.66~0.83)。在失代偿期患者中,CO<5 L/min的患者比CO≥5 L/min的患者死亡风险更高(SHR=0.44,95%CI=0.25~0.77,P=0.004)。
对于预防首次出血的高风险静脉曲张患者,失代偿期肝硬化对β受体阻滞剂的全身血流动力学反应大于代偿期患者,而门静脉压力降低较小。因此,β受体阻滞剂对CO的短期作用可能会对失代偿期肝硬化患者的生存产生不利影响,这提示无创监测CO会对指导用药有所帮助。

简评丨祁小龙
兰州大学第一医院门静脉高压研究所(中心)
本研究保持了巴塞罗那Villanueva团队一贯的高水准,继2019年3月发表于Lancet的PREDESCI随机、双盲、安慰剂对照试验(β受体阻滞剂可有效阻止肝硬化伴临床显著性门静脉高压患者的失代偿事件)后,Villanueva团队本次报道了β受体阻滞剂对于失代偿期肝硬化患者的重要临床发现。
作为降低门静脉压力的一线药物,β受体阻滞剂对于门静脉高压相关并发症的一级预防具有重要作用。当在一定范围内增加使用剂量时,β受体阻滞剂可有效提高患者的应答率,进而改善预后。然而,若“盲目”提高其使用剂量,可造成心率、血压和心输出量的显著降低,甚至危及生命。本研究探讨了β受体阻滞剂对心功能的影响,及其与患者预后的关系。值得注意的是,本研究受试者接受了大剂量药物(普萘洛尔和纳多洛尔从40 mg/天逐步加量至240 mg/天,卡维地洛从6.25 mg/天逐步增加至25 mg/天),这些剂量超过了我国指南推荐和临床实践的剂量。因此,该研究结论对我国临床的指导价值有待进一步验证。
笔者团队以“Carvedilol、Propranolol、Response、HVPG”为关键词,检索了自2015年至2020年间有关β受体阻滞剂应答的临床研究,在检索到的14篇文献中,仅有1篇来自中国:该研究发现,当患者接受普萘洛尔耐受剂量或最大剂量120 mg/天时,患者应答率约为70%。遗憾的是,该研究未分析普萘洛尔不同剂量与患者应答率及心输出量的关系。因此,今后有必要开展针对中国人群的β受体阻滞剂有效剂量与安全剂量的研究。
本研究指出,对于食管胃静脉曲张出血一级预防的肝硬化患者,失代偿期患者在服用β受体阻滞剂后相比于代偿期患者的心输出血量和心率下降幅度更大。这提示我们在临床实践中,应及早发现高出血风险的代偿期肝硬化患者,并尽早使用β受体阻滞剂以取得更好的临床获益。然而,由于代偿期肝硬化患者很难接受定期的胃镜检查,且内镜技术在部分基层医院尚未得到良好质控。为进一步构建适合我国门静脉高压患者出血风险筛查和管理的模式,笔者组织发起了“中国门静脉高压出血风险筛查和管理项目”,旨在利用“CHESS标准”有效避免不必要的胃镜检查,节约医疗成本、降低患者经济负担,最终筛选出代偿期肝硬化高出血风险的患者进行一级预防治疗。
Sartoris R, Lazareth M, Nivolli A, et al. CT-based liver surface nodularity for the detection of clinically significant portal hypertension: defining measurement quality criteria. Abdom Radiol (NY). 2020
近日,来自法国的Sartoris R等人通过基于CT的肝表面结节(LSN)测量方法,建立了非侵入性评估有临床显著性门静脉高压(CSPH)肝硬化患者的测定标准。相关内容发表在Abdominal Radiology (NY)杂志上。
该研究纳入了74例肝硬化连续病例(平均年龄62±13岁),其中30例伴有CSPH(41%),患者接受CT和肝静脉压力梯度测量。三位独立阅片人通过专用软件对每位患者进行15次LSN测量。根据1到15次测量的中位数和平均值计算LSN。使用受试者工作特征曲线(ROC)分析评估诊断CSPH的准确性。通过组内相关系数(ICC)和Bland-Altman图(BA)评估变异性,以最大程度提高LSN的准确性及最小化变异性,确定质控标准。
结果显示,基于1到15次LSN测量的平均值和中位数的AUROC曲线下面积分别为0.79±0.05到0.91±0.04和0.86±0.04到0.91±0.03,配对比较无明显差异(P>0.05)。LSN的AUROC从1到8依次增加,并在8到15次测量中趋于平稳。观察者内部和观察者间的变异性从1到15次测量中有所降低,超过8次测量后仅略有改善。观察者内部和观察者间的一致性较好[ICC=0.90(95%CI 0.84~0.94),ICC=0.93(95%CI 0.89~0.95)],观察者内和观察者间的一致性变异率较低,分别为4.2%(BA偏差)[95%的一致性限值(LoA)(-15.3; + 23.7%)和4.8%LoA(-17.5; + 27.1%)]。
因此,基于CT的LSN测量具有高度的可重复性和准确性。建议至少通过8次有效测量确定检测CSPH的平均LSN值。

简评丨高强
广州市第一人民医院放射科
门静脉高压是肝硬化严重的并发症之一,可引起食管胃静脉曲张出血、腹水或肝肾综合征,也是降低患者生产率的主要原因。肝静脉压力梯度(HVPG)是诊断门静脉高压的金标准,HVPG≥10 mmHg被视为临床显著性门静脉高压(CSPH),CSPH提示肝硬化患者食管静脉曲张和临床失代偿的进展。尽管HVPG对于门静脉高压的诊断和预后具有重要意义,但作为一种侵入性方法,其可替代的无创检测仍然是临床需要的。
近年来,基于CT定量肝脏表面结节(LSN)的方法无创性检测CSPH并评估肝硬化程度成为该领域的研究热点。然而,此前研究大多聚焦在该方法的诊断效能上,忽视了方法的标准化及可重复性。该研究旨在为基于CT定量LSN评估肝硬化CSPH这一无创技术建立质控标准。该研究由三位独立研究人员利用专业软件对每位纳入患者进行15次LSN测量,基于从1到15次测量的中间值和均值计算得出每位患者的LSN值。通过对比HVPG,进而评估LSN值诊断CSPH的准确性和变异性,以最大准确度的LSN和最小的可变性作为质控标准。结果显示,基于CT的LSN测量方法具有高度的可复制性和准确性,并建议至少需要进行8次有效测量才能确定检测CSPH的LSN均值。该研究进一步证实了基于CT的LSN测量来准确判断CSPH的可行性,并为该技术提供了质控标准,具有很好的临床价值。
Yaqoob U, Luo F, Greuter T, et al. GIPC-regulated IGFBP-3 Promotes HSC Migration in Vitro and Portal Hypertension in Vivo Through a β1-integrin Pathway. Cell Mol Gastroenterol Hepatol. 2020TGF-β
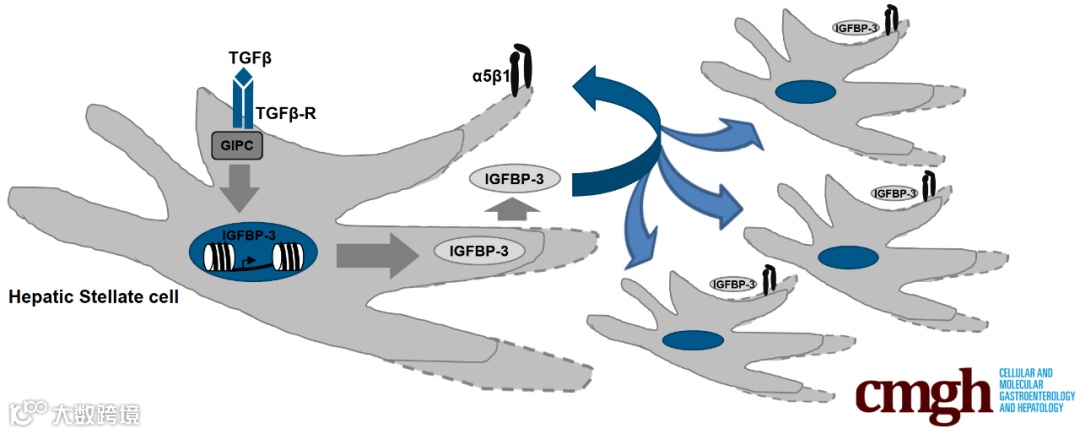
可诱导静止性肝星状细胞(HSC)活化并促进其转化为成肌纤维细胞,是肝纤维化和门静脉高压发病中的关键事件。GIPC(又称为synectin)是TGF-β和其他受体的下游信号激活分子。近日,来自美国梅奥医学中心的Yaqoob U等人研究了TGF-β和GIPC的新靶向基因,并阐明其参与肝纤维化的机制,相关内容发表在Cellular and Molecular Gastroenterology and Hepatology杂志上。
研究者在有无GIPC敲除的情况下,通过对TGF-β刺激的HSC进行mRNA测序分析,发现胰岛素生长因子转运蛋白(IGFBP-3)为TGF-β和GIPC的最活化靶基因,这个结果在qPCR、ELISA和Western blot等实验中得到了进一步证实。
ChIP实验显示,GIPC增加了H3K27乙酰化激活标记,同时降低了H3K27抑制性三甲基化(H3K27m3)标记,与调控基因变化的表观遗传有关。体内研究显示,IGFBP-3敲除小鼠的HSC激活标志物减少,小鼠慢性肝损伤模型中门静脉压力降低。
肝硬化患者的血清分析结果显示,与健康对照组相比,IGFBP-3的表达提高了2倍以上。体外机制研究表明,IGFBP-3可通过整合素依赖性AKT磷酸化促进HSC迁移。
因此,TGF-β可通过GIPC上调IGFBP-3,在体外引起HSC迁移增加,并在体内促进门静脉高压。以上研究支持IGFBP-3作为新的慢性肝病的潜在病理生理靶标或标志物。
简评丨徐濛
南方医科大学基础医学院
肝星状细胞(HSCs)是肝脏特有的一种非实质细胞,在正常肝组织中HSCs常处于静息状态,但是当肝脏受到病理因素刺激发生纤维化/肝硬化的时候,损伤区域会被大量的细胞外基质(ECM)包裹,而因为HSCs是ECM的主要来源,往往将其作为纤维化/肝硬化病变的终末效应细胞进行研究。
以往研究表明IGFBP-3可以作为HSCs活化的一个标志物并且能够参与多种细胞的迁移过程。在本文中,作者在探索二者关联及作用机制时发现,受到GIPC调节的IGFBP-3可以通过PI3K-AKT信号通路调控HSCs的迁移,进而参与到肝脏纤维化的过程中。动物体内实验证实,相比于WT组,全身性敲除IGFBP-3的纤维化模型小鼠其门静脉压力及纤维化程度均得到不同程度的缓解,且血清IGFBP-3水平与纤维化病变呈现一定程度的正相关性。对6例酒精性肝硬化患者血清IGFBP-3水平的检测也发现了其对于肝硬化有很好的指示作用,提示其可以作为临床诊断的一个潜在生物标志物。
对于肝脏纤维化/肝硬化目前临床上没有标准的治疗方案,除了对症处理以外,主要治疗原则是在不影响正常ECM合成的情况下有效减轻过多的胶原蛋白沉积,并且辅以措施去除病因。本文的研究不仅为我们提供了新的肝纤维化/肝硬化干预治疗靶标及可能的血液诊断分子标志物,还可以加深读者对于IGFBP-3调控HSCs的进一步理解,为后续与HSCs功能相关的疾病研究提供有益借鉴。
Simbrunner B, Marculescu R, Scheiner B, et al. Non-invasive detection of portal hypertension by enhanced liver fibrosis score in patients with different etiologies of advanced chronic liver disease. Liver Int. 2020
增强的肝纤维化(ELF)评分包括纤维化和基质重塑的血清标志物,可用于检测肝纤维化。近日,来自奥地利维也纳医科大学的Simbrunner等人探讨了其在无创检测门静脉高压(PHT)中的作用,相关内容发表在Liver International杂志上。
该研究共分析了201例晚期慢性肝病患者[ACLD;即肝静脉压梯度(HVPG)≥6 mmHg]的ELF评分及其单项成分(TIMP1/PIIINP/HA)。肝前和肝后PHT、超出米兰标准的肝细胞癌以及有TIPS操作或肝移植史的患者排除在外。
结果发现,整个研究队列,ELF及其单项成分与HVPG相关:ELF:r=0.443,TIMP1:r=0.368,PIIINP:r=0.332,HA:r=0.419(所有P<0.001)。当患者HVPG较高时,ELF与HVPG间的相关强度有所降低:HVPG为6~9 mmHg时,r=0.569(P=0.004);10~19 mmHg时,r=0.304(P=0.001);≥20 mmHg时,r=-0.023(P=0.853)。
用来检测临床显著性门静脉高压(CSPH,HVPG≥10 mmHg)的ELF评分受试者操作特征下的面积(AUROC)为0.833。重要的是,仅HA的AUROC为0.828。在严格代偿的ACLD(cACLD)患者中CSPH的检测准确性较差:AUROC:0.759(P<0.001)。ELF≥11.1判定CSPH,PPV为98%(敏感性:61%,特异性:92%,NPV:24%),但不能排除CSPH。
ELF用于诊断高危门静脉高压(HRPH;HVPG≥20 mmHg)的AUROC仅为0.677(0.60~0.75; P<0.001),提示ELF无法判定HRPH。但是,当ELF<10.1用于排除HRPH时,NPV为95%(敏感性:97%,特异性:26%,PPV:39%)。
因此,HVPG<20 mmHg时,ELF评分与其有相关性。ELF≥11.1的患者出现CSPH的可能性很高,而ELF<10.1可用于排除HRPH。

简评丨秦维
保定市人民医院消化科
肝静脉压梯度(HVPG)是诊断肝硬化门静脉高压的金标准,其无创替代方法在诊断和监测肝硬化门静脉高压方面有巨大潜力。近日,Benedkikt等人通过增强肝纤维化评分(ELF评分包括三个血清参数:TIMP1、PIINP和HA)对不同病因晚期慢性肝病患者进行门静脉压力的无创检测,研究ELF评分是否能预测患者的CSPH和HRPH,同时也专门研究ELF在代偿期肝硬化中的诊断准确性。
该研究对201例晚期慢性肝病患者的ELF评分及其单组分进行分析。结果显示,在整个队列中ELF及其单个成分与HVPG相关。在较高的HVPG层中,ELF与HVPG之间的相关强度降低。ELF评分的曲线下面积(AUROC)检测临床显著性门静脉高压为0.833,仅HA的诊断价值即为0.828。对于失代偿期肝硬化患者,ELF对于CSPH的诊断准确性有限:AUROC:0.759(P<0.001)。当用ELF≥11.1判定CSPH时,PPV为98%,但不能排除CSPH。当ELF <10.1时,可用于排除HRPH,NPV为95%。因此,ELF与HVPG相关,可用于纳入CSPH(临界值>11.1)和排除HRPH(临界值<10.1)。但是,该方法存在一定的诊断灰区,且ELF无法提供门静脉高压严重程度的临床分层。
Zhao ZL, Wei Y, Wang TL, et al. Imaging and Pathological Features of Idiopathic Portal Hypertension and Differential Diagnosis from Liver Cirrhosis. Sci Rep. 2020
特发性门静脉高压(IPH)在诸多方面可模拟肝硬化。但目前为止,尚无有效的影像学方法来区分这两种疾病。近日,来自我国的Zhao ZL等人分析了IPH和肝硬化的影像学和病理学特征。相关内容发表在Scientific Reports杂志上。
该回顾性研究分析了2015年1月至2019年3月间的共16例IPH和16例肝硬化患者(年龄为39±20岁)的超声、CT和MRI图像和病理结果,以及对照组的16例正常人成像结果。
结果发现,IPH与肝硬化患者的门静脉主干和门静脉矢状部的平均管腔直径、壁厚和厚径比间存在显著差异(P<0.05);在第3段(S3)门静脉、IPH和肝硬化患者之间管腔直径和厚径比之间也存在明显差异(P<0.05)。在IPH患者中,主要影像学改变是门静脉壁增厚、狭窄或闭塞、造影剂延迟期门静脉的较低强化区域以及T1WI的非均匀变化。相应的病理学变化包括小叶间静脉增厚、狭窄、闭塞、门静脉纤维化及肝细胞萎缩或凋亡。肝硬化的主要影像学特征是T1W1表现为结节性改变,相应的病理学改变是假小叶形成。IPH的影像学特征包括门静脉血管壁增厚、管腔狭窄和无弥漫性肝硬化样结节。
因此,两种疾病的影像学特征具有明确的病理学基础,对IPH和肝硬化的鉴别诊断有帮助。

简评丨高强
广州市第一人民医院放射科
目前,尚无关于有效的影像检查鉴别这两种疾病的报道。本研究回顾性总结了IPH与肝硬化的超声、CT及MRI的影像特征,并与相应的病理进行对照分析。结果显示,IPH的影像学和病理学主要表现为Glisson鞘与门静脉系统的破坏,影像学表现为门静脉管壁增厚并轻度延迟强化,门静脉管腔狭窄、闭塞,门静脉周围肝实质不均质表现;病理学表现为门静脉管壁纤维化,门静脉周围肝细胞萎缩、凋亡,病理与相对应的影像表现相吻合。与IPH不同的是,肝硬化门静脉管壁变薄、管腔扩张,肝实质弥漫性再生结节形成,尤其在T1WI-MRI尤为明显;其病理主要特征为肝实质纤维化,小叶间可见纤维间隔,假小叶形成。故IPH与肝硬化在影像学和病理学上都有明显的区别。因此,IPH区别于肝硬化最主要的影像特点是无弥漫性肝硬化结节、增厚的门静脉管壁以及门静脉管腔狭窄,这些影像特征同时加上明确的病理基础,可有效进行两者的鉴别诊断。


扫描二维码
浏览往期文章

(来源:《国际肝病》编辑部)



