

由中国肝炎防治基金会(CFHPC)、美国肝病研究学会(AASLD)主办的“2020中美肝病学院”于2020年12月18日~19日顺利召开。由于受新冠肺炎疫情影响,本次会议采取线上虚拟的形式,汇集了中美两国肝病领域的一流专家对2019年~2020年美国肝病学年会的热点问题和中国肝病防治的最新研究进展进行了分享和交流。
大会的第一天,在主题报告环节,复旦大学附属华山医院的张文宏教授和清华大学附属北京清华长庚医院的魏来教授共同主持了会议,美国密西根大学骆淑芳(Anna S. LOK)教授对2019年~2020年AASLD年会上发布的关于乙型和丁型肝炎的最新研究成果进行了汇报。
骆教授指出,目前,世界范围内与乙型肝炎病毒(HBV)感染相关的死亡率仍然很高,每年HBV相关死亡人数持续增长。而在临床上,治疗HBV感染的药物包括干扰素(IFN)和核苷(酸)类似物(NAs),这些药物在治疗HBV方面存在一定的有效性,包括抑制病毒复制、逆转肝脏炎症和纤维化、预防进展为肝硬化和肝衰竭、降低肝细胞癌(HCC)发病风险;但同时也伴有一定的局限性,包括不能根除共价闭合环状DNA(cccDNA)或整合HBV DNA、低乙肝表面抗原(HBsAg)转阴率、抗病毒治疗时程长及降低HCC发病率但不能完全消除HCC风险。因此,临床上亟需更好的疾病治疗方法。

当前的HBV治疗
●在停用长期NA治疗后,亚洲人的HBsAg转阴率比白种人低
在今年的AASLD会议上,一项基于大样本量队列数据的回顾性研究公布。该研究纳入北美、欧洲和亚洲12个中心停止NA治疗的1541例患者,其中88%为亚洲人。NA治疗开始时,77%的患者为乙肝病毒e抗原(HBeAg)阴性;NA治疗结束时,患者均为HBeAg阴性。而NA停止后12个月内,患者均未使用聚乙二醇干扰素(Peg-IFN)。在第四年,患者HBsAg累积转阴率仅为14%[1]。见图1。

图1 NA停药后的HBsAg转阴率的变化
(引自报告幻灯)
而与HBsAg转阴相关的因素中,白种人是最重要的预测因素,这意味着NA停药并不是一个适用于大多数亚洲患者的策略,因为其HBsAg转阴率相对会更低。另外,在与再治疗相关的因素中,年龄大是最重要的相关因素,但是因为研究没有规定再治疗的标准,所以这不一定代表老年患者与年轻患者有所不同[1](见表1)。所以我们仍需要寻找更好的治疗方法。
表1 与HBsAg转阴和再治疗相关的因素分析
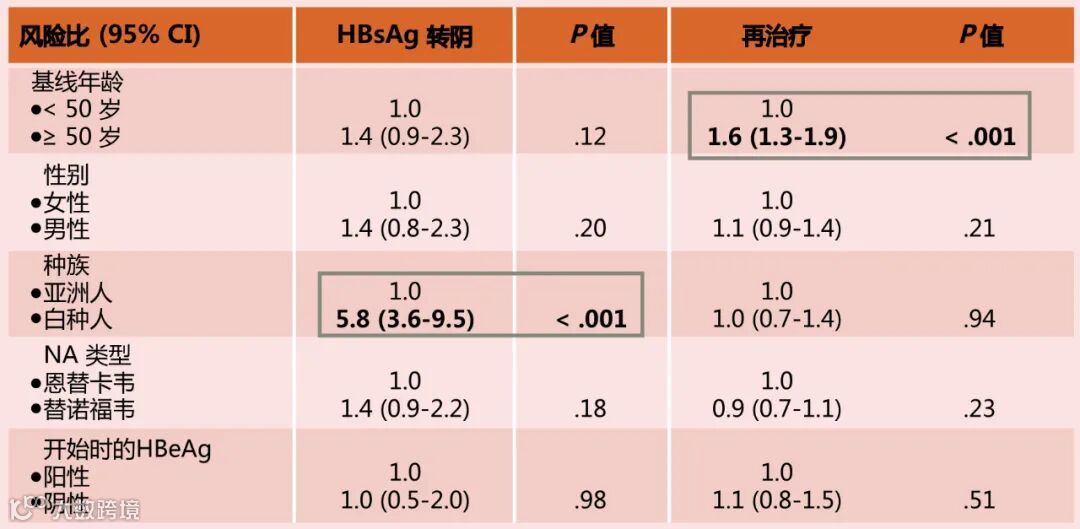
(引自报告幻灯)
●192周TDF联合24周Peg-IFN治疗,并按方案停用TDF,与TDF单药治疗相比并未增加HBsAg转阴率
另外一项来自美国国立卫生研究院(NIH)乙肝研究协作网的研究[2]纳入了201例HBeAg阳性/阴性患者,并将患者随机分为两组,一组单独使用富马酸替诺福韦酯(TDF),另一组前24周使用TDF联合Peg-IFN治疗,之后停用Peg-IFN,继续TDF治疗。该研究入组的HBeAg阳性和阴性患者在24周内都未接受抗病毒治疗。谷丙转氨酶(ALT)>1.5×ULN,HBV DNA≥1000IU/mL,且肝脏疾病都处于代偿期。研究的主要终点为HBsAg转阴(见图2,表2)。
这项研究的不同之处在于其规定了严格的停药和再治疗标准,即只有非肝硬化且HBV DNA<1000IU/mL持续24周,此外在第192周HBeAg阴性且乙肝e抗体(HBeAb)阳性的患者,才符合TDF停药的标准。而出现任何临床失代偿表现均需要重新进行TDF再治疗,包括胆红素升高,或HBV DNA≥10000IU/mL伴随ALT>1000U/L持续一周,≥300/200U/L持续≥4周或≥150U/L持续≥12周。但结果表明,192周TDF治疗+/-初始24周Peg-IFNα治疗,并按方案停用TDF,与TDF单药治疗相比并未增加HBsAg转阴率。

图2 两组患者240周累积HBsAg转阴率
(引自报告幻灯)
表2 意向性治疗人群(ITT)特征分析
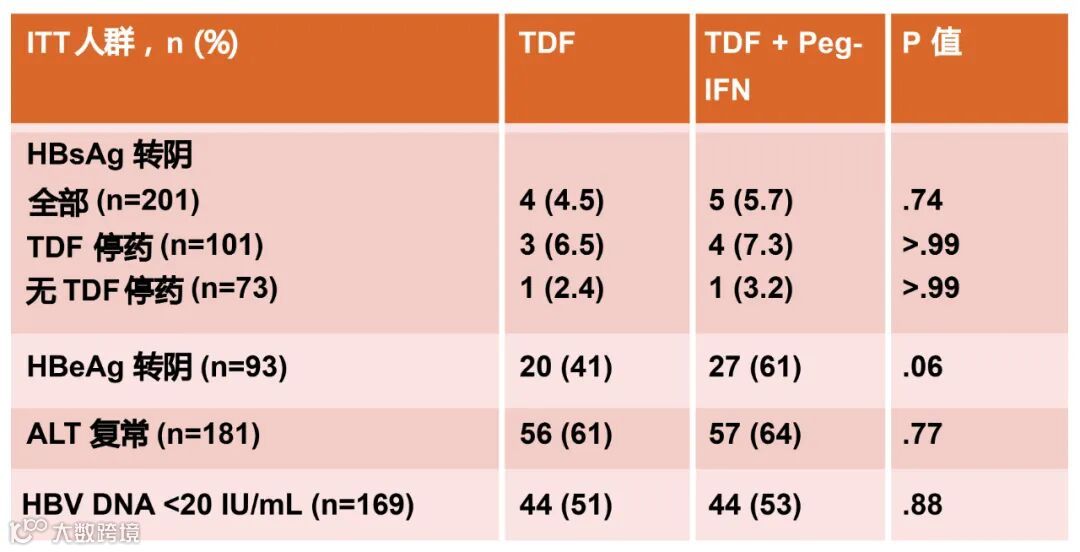
(引自报告幻灯)
目前一些新疗法正在开发研究中,但现在判断哪种疗法更有效还为时过早。

HBV新疗法
为最大限度地治疗HBV,临床上需要多个可同时抑制病毒复制和减少病毒抗原产生的靶点药物,同时需要识别出被感染的肝细胞,因此,在治疗研究方面既需要抗病毒的药物,也需要免疫调节的药物。
●JNJ-3989(RNAi)3次给药+NA治疗后可实现HBsAg水平持续抑制
通过RNA干扰剂或反义寡核苷酸,可减少病毒颗粒和HBsAg的生成,从而可能有助于恢复免疫反应。
一项研究纳入了40例NA初治或经治的HBeAg+/-患者,分别于第1、27、57天给药,并联用NA。这些患者中有73%为男性,85%为亚洲人;65%HBeAg-;80%NA经治。结果显示,98%患者的HBsAg最大降低幅度>1.0log10IU/mL,此外,17例患者(40%)在RNAi末次给药后的9个月仍维持持续的HBsAg抑制[3](见图3)。

图3 两组患者HBsAg的变化
(引自报告幻灯)
●JNJ-3989(siRNA)、JNJ-6379(CpAM)和NA三联疗法安全性良好
乙肝病毒核蛋白组装调节剂(CpAM)通过多种不同机制发挥作用,但最主要的机制是阻止核心颗粒正确组装,从而导致其组装错误或形成空心颗粒,进而降低HBV DNA复制、病毒颗粒分泌以及HBV蛋白的产生;并在高剂量下,减少核心颗粒的细胞内再循环,阻断cccDNA的补充;此外,还会阻止核心颗粒的分解和感染的建立。
一项关于siRNA、CpAM和NA的三联治疗研究[4],其耐受性良好,所有患者都实现了HBV DNA和RNA的显著降低;且都实现了HBsAg下降≥1.0log10(90%)的降低(-1.01~-2.26log10)。HBeAg+和HBeAg-患者HBsAg下降情况相似(见图4,图5)。
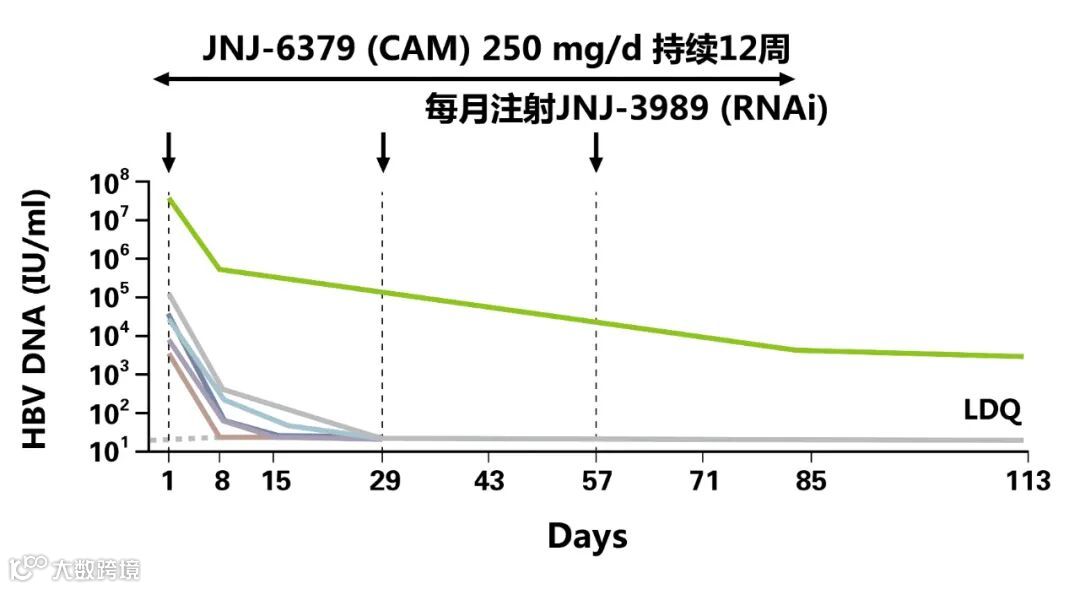
图4 每例患者HBV DNA的变化
(引自报告幻灯)

图5 第113天HBsAg变化(单位:log10IU/mL)
(引自报告幻灯)
●对HBV阳性患者进行TLR8激动剂SLGN联合TAF治疗,显示HBV DNA下降幅度类似
临床上可以通过加强免疫或阻断免疫抑制途径来尝试刺激先天免疫或恢复适应性免疫,但迄今为止,免疫调节疗法抗病毒效果并不明显,且其对HBsAg水平的作用非常有限。
一项关于在乙肝病毒阳性患者中进行的TLR8激动剂SLGN联合富马酸丙酚替诺福韦(TAF)治疗的研究[5],该研究纳入67例病毒阳性的乙肝患者,并将其随机分配到TAF单药组、1.5mgSLGN联合TAF治疗24周后继续TAF单药治疗组或3mgSLGN联合TAF治疗24周后继续TAF单药治疗组。比较患者在24周HBsAg的变化及不同治疗组间HBV DNA的对比情况。结果显示,在第24周,仅在接受SLGN治疗的患者中观察到HBsAg下降≥0.3log,此外,在第24周没有患者出现HBsAg或HBeAg转阴。另一方面,三组患者HBV DNA下降的幅度类似。
●对HBsAg和HBcAg(NASVAC)阳性的慢性乙肝患者治疗,显示大部分患者HBsAg下降幅度很小或者没有下降
该研究纳入NA初治或经治的HBsAg和HBcAg(NASVAC)阳性的慢性乙肝患者,并对患者进行治疗性疫苗的鼻腔给药,给药频次为每2周一次,共计10次。结果显示,患者在接受疫苗治疗期间,HBsAg有所下降,但大部分患者HBsAg下降幅度很小或者没有下降[6]。
●丁型肝炎(HDV)治疗
慢性乙肝患者合并感染HDV会导致更严重的肝病。目前在大部分国家尚无批准的HDV治疗药物。而2020年8月,EMA批准的Bulevirtide用于治疗HDV的III期临床试验也仅在进行当中。干扰素是唯一对HDV RNA有一定抑制作用的药物,但大多数患者在停药后复发;而一些研究表明,若患者耐受干扰素,则可持续接受数年的干扰素治疗,部分患者可实现持续的HDV RNA抑制,甚至HBsAg转阴。此外,NA单独使用没有抗病毒活性,与干扰素联合使用亦不增加抗病毒活性,因此,推荐将其与新的HDV治疗联合使用,以防止在HDV被抑制时HBV重新激活而继发肝炎。
今年的AASLD会议上展示了一项关于HDV的研究,即Peginterferon Lambda,Lonafarnib和Ritonavir治疗24周的II期研究:LIFT HDV研究[7](见图6)。该研究纳入26例HDV患者,并对其进行Peginterferon Lambda180mcg每周一次的皮下注射、Lonafarnib50mg及Ritonavir100mg每日2次口服的联合治疗。结果显示,经过24周治疗,77%的患者出现HDV RNA下降>2log,50%的患者在治疗结束时检测不到HDV RNA,但当停止治疗后,部分患者复发。而23%的患者在随访结束时检测不到HDV RNA。Lonafarnib具有明显的胃肠道副作用,即便在与Ritonavir联合治疗使用较低剂量时,副作用仍较明显。因此,仍需要开展长期的临床研究。

图6 HDV-RNA中位数随着时间的变化
(引自报告幻灯)
最后,综合2019~2020AASLD关于HBV和HDV的研究分析,在停用长期NA治疗后,亚洲人的HBsAg转阴率比白种人低;192周TDF治疗联合24周Peg-IFN治疗,并按方案停用TDF,与TDF单药治疗相比并未增加HBsAg转阴率。此外,目前关于该病的新疗法正在研究当中,但现在判断哪种疗法更有效还为时过早。RNAi3次给药联合NA治疗后可实现HBsAg水平持续抑制。SiRNA、CpAM和NA三联疗法耐受性良好;而免疫调节治疗的疗效一般;Peg-IFN、Lonafamib和Ritonavir三联疗法似乎是安全的,可增加对HDV RNA的抑制作用。
(来源:《国际肝病》编辑部)




