
各位专家同道好,本期CHESS月评(第四十三期)将分享上月PubMed发表的门静脉高压诊疗领域6篇文献(诊断监测3篇,多学科治疗3篇)。本期特邀月评专家:山东大学齐鲁医院消化内科高艳景教授、宁夏回族自治区人民医院肝胆外科田明国教授和安徽医科大学第二附属医院放射科宫希军教授。


Zhang Y, Xu BY, Wang XB, et al. Prevalence and Clinical Significance of Portal Vein Thrombosis in Patients with Cirrhosis and Acute Decompensation. Clin Gastroenterol Hepatol. 2021
门静脉血栓(PVT)是肝硬化患者常见的严重并发症。但是,目前对于肝硬化合并急性失代偿(AD)患者中的PVT知之甚少。近日,Zhang Y等人的研究分析了肝硬化和AD患者中PVT的患病率及临床意义,相关内容发表在Clinical Gastroenterology and Hepatology杂志上。
该回顾性研究分析了由中国慢加急性肝衰竭联盟建立的CATCH-LIFE研究的两组慢加急性患者(2015年1月至2016年12月,n=2600名患者;2018年7月至2019年1月,n=1370例患者)。研究团队共分析了2826例伴和不伴AD的肝硬化患者的PVT患病率、临床表现和危险因素。
结果发现,肝硬化合并AD患者的PVT患病率为9.36%,明显高于无合并AD的肝硬化患者(5.24%)(P=0.04)。在患有肝硬化和AD的患者中,有63.37%的患者出现了PVT(最初检出的PVT,无慢性PVT征兆)。与没有PVT的患者相比,PVT患者的静脉曲张破裂出血比例明显升高(47.33% vs. 19.63%;P<0.001),PVT患者的D-二聚体中位血清水平显著升高(2.07 vs. 1.25;P<0.001)。脾切除和内镜下硬化治疗是肝硬化合并AD患者PVT的独立危险因素。有或无PVT的患者的1年死亡率无显著差异。
因此,通过分析2826例肝硬化患者的数据,AD患者中有PVT的比例明显高于无AD的患者。PVT与静脉曲张出血增加相关,增加了AD的风险。需要通过定期筛查来预防肝硬化患者的PVT,降低门静脉高压。

(图源自文献)
简评丨祁小龙团队
兰州大学第一医院门静脉高压研究所(中心)
门静脉血栓(PVT)是指门静脉主干或门静脉左、右分支发生血栓,伴或不伴肠系膜静脉和脾静脉血栓形成(中华医学会消化病学分会肝胆疾病协作组,中华消化杂志 2020)。肝硬化是PVT发生最常见的危险因素,门静脉血栓也是肝硬化最常见的并发症之一(Qi X, et al. Nat Rev Gastroenterol Hepatol 2014)。近年来,肝硬化患者中的PVT受到了越来越多的关注和重视,在治疗方面也取得了一些进展。然而,对于急性失代偿期肝硬化与PVT的相关研究较少。
研究团队基于由中国慢加急性肝衰竭联盟建立的CATCH-LIFE研究的两组慢加急性患者中2826例伴和不伴急性失代偿的肝硬化患者,首次阐明了肝硬化合并急性失代偿人群的患病率与临床特征。研究分析发现:①急性失代偿期肝硬化患者PVT发生率显著高于非急性失代偿的患者;②脾脏切除术和内镜下硬化治疗是急性失代偿期肝硬化患者PVT发生的独立风险因素;③PVT可能加重门静脉高压,提高静脉曲张出血风险,从而增加肝硬化急性失代偿的风险。
本研究亮点包括:①研究结论基于大型的多中心队列,纳入了以乙型肝炎为主要病因的晚期肝硬化患者,数据充实;②本研究首次关注PVT与急性失代偿期肝硬化的关系,填补了肝硬化合并急性失代偿患者PVT研究的空白;③脾切除术和内镜下硬化治疗是PVT的独立风险因素,因此肝硬化不伴急性失代偿的患者在经历脾切除术或内镜下硬化治疗后,应密切监测PVT的发生。
Selicean S, Wang C, Guixé-Muntet S, et al. Regression of portal hypertension: underlying mechanisms and therapeutic strategies. Hepatol Int. 2021
门静脉高压是慢性肝病的主要非肿瘤性并发症,也是包括腹水或静脉曲张破裂出血在内的导致严重生命危险的重要原因。肝脏微循环功能障碍导致的病理性肝内血管阻力增加是门静脉高压发展的主要因素,随后肝外血管紊乱(包括门静脉血流的增加)加剧了该情况。一些临床前肝硬化模型的证据表明,当去除病因后,门静脉高压和慢性肝病可以逆转,并可以通过药物治疗进一步改善。这些重要的发现已在临床研究中得到了部分证明。近日,来自瑞士伯尔尼大学的Selicean S等人发表了综述文章,对目前有关门静脉高压自发性和药物促进性逆转的最新资料进行了总结归纳。除注重临床证据外,还考虑了病理生理学警示,强调在建立人类慢性肝病和门静脉高压是可逆的新观念时需要谨慎。详细内容发表在Hepatology International杂志上。

(图源自文献)
简评丨高艳景
山东大学齐鲁医院消化内科
门静脉高压是慢性肝病的主要并发症,是慢性肝病的热点关注问题。目前观点认为进展期肝纤维化除接受肝移植外不可逆转,而新近临床和动物研究显示去除病因后肝纤维化甚至肝硬化可能会逆转。该综述据最新研究阐述了门静脉高压的发生机制及未来治疗策略。
本综述从动物模型研究及临床数据资料阐述了肝纤维化和门静脉高压在去除病因后的可逆性。去除病因是逆转慢性肝病的首要步骤。多项研究显示,经去除病因治疗,部分患者的门静脉高压可被逆转,尤其是对于病毒性肝炎引起慢性肝病的患者。绝大多数对抗病毒治疗应答的进展期乙型肝炎肝硬化患者的坏死性炎症和纤维化评分逐步降低。多项研究结果表明,抗乙型肝炎病毒治疗可降低食管静脉曲张进展的风险。
与抗乙型肝炎病毒治疗类似,抗丙型肝炎病毒治疗也可以预防食管静脉曲张的发生或延缓进展至失代偿期。然而,研究显示,如果在治疗开始前已经存在食管静脉曲张,则上述效应似乎就有所减弱,说明一旦发生门静脉高压,抗丙型肝炎病毒治疗食管静脉曲张的效果则相对较差。此外,即便门静脉压力降低,也难以预防失代偿的发生,并难以将压力降低至临床显著性门静脉高压的阈值以下。
虽然有充足的证据表明肝硬化门静脉高压至少可被部分逆转,但是逆转的程度取决于疾病的分期。该综述归纳了限制门静脉高压逆转的细胞分子机制,包括肝脏纤维组织特性、肝星状细胞激活、血管表型转换以及衰老等因素。导致门静脉高压难以被逆转的重要因素包括纤维化组织的组成和硬度、特定细胞群的出现或消失以及明显的(微)血管变化,所有上述因素在早期和进展期慢性肝病中均有显著差异。
该综述进一步归纳了降低门静脉压力的治疗策略及改善炎症及纤维化的治疗策略。血管调节剂是一类可以有效降低肝血管阻力的药物,包括他汀类、肾素血管紧张素醛固酮系统抑制剂(血管紧张素转移酶抑制剂、血管紧张素受体拮抗剂和醛固酮拮抗剂)、PDE5抑制剂及Rho激酶抑制剂。研究显示,半乳糖凝集素3抑制剂Belapectin,可显著降低无明显食管静脉曲张患者的肝静脉压力梯度(HVPG)及食管静脉曲张的再发率。一项针对伴有临床显著性门静脉高压的肝硬化患者的临床研究显示,经牛磺酸治疗28天后,58%的受试者的HVPG下降超过10%。类似的,益生菌、抗生素、抗氧化剂、Simtuzumab等药物也显示出了通过减少炎症和纤维化从而不同程度地降低门静脉压力作用。
HVPG是监测门静脉压力的金标准,而学者们也正在尝试寻找相关血清标志物,以期更为便捷、无创地评估门静脉压力。有研究发现,反映纤维生成和纤维溶解的血清标志物与门静脉高压的程度具有相关性,但仍有待进一步研究。
该综述从分子机制到临床研究针对逆转门静脉高压机制及治疗策略进行了全面阐述,为今后的临床和基础研究提供了良好的参考。
Li Y, Liu Z, Liu C. Efficacy and safety of laparoscopic splenectomy for hypersplenism secondary to portal hypertension after transjugular intrahepatic portosystemic shunt. BMC Gastroenterol. 2021
患者经颈静脉肝内门体分流术(TIPS)后使用腹腔镜脾切除术(LS)的相关研究尚未见报道。近日,来自重庆医科大学的Li Y等人探讨了TIPS术后门静脉高压继发脾功能亢进的患者行LS的可行性、安全性和潜在疗效。
该研究回顾分析了2014年至2020年间门静脉高压继发脾功能亢进TIPS术后接受LS治疗的6例患者,记录患者围手术期数据及临床转归。
结果显示,所有患者均顺利完成LS手术。LS治疗后6例患者的脾功能亢进均得到了纠正。术后凝血酶原时间、凝血酶原活性、国际标准化比率和总胆红素均有改善趋势。术前和术后1个月的白蛋白和活化部分凝血活酶水平无明显差异。在两名有限记录的患者中,血浆氨水平和血栓弹性成像指标得到改善。在1个月的随访期内,未发生膈下脓肿、门静脉血栓形成、静脉曲张破裂出血、肝性脑病和肝功能衰竭等术后并发症。
因此,TIPS术后LS治疗门静脉高压继发性脾功能亢进的患者是可行、安全和有益的。LS不仅能纠正脾功能亢进,而且有可能改善肝功能。

(图源自文献)
简评丨田明国
宁夏回族自治区人民医院肝胆外科
近年来TIPS在门静脉高压的治疗中应用越来越多,对外科治疗后复发或内镜治疗失败的患者常采用TIPS治疗。TIPS治疗后也可发生肝性脑病,脾亢不能缓解,甚至胃食道静脉曲张复发的情况,多采取较为保守的药物、介入栓塞或内镜治疗。
本文回顾性分析了腹腔镜脾切除术(LS)治疗TIPS术后重度脾亢6例,通过观察术前及术后1个月患者血常规、肝功能、凝血功能及2例患者的血氨变化,以及术后并发症情况,研究认为LS可彻底消除脾亢并改善肝脏功能,是TIPS术后脾亢安全可行的治疗方法。尝试用LS 治疗TIPS术后脾亢是本文的亮点。
本文的缺陷在于:①病例过少、随访时间过短。②6例均有食道中、重度静脉曲张,且1例在TIPS后复发静脉曲张破裂出血,而LS后并没有复查胃镜。上述情况行脾切除联合贲门周围血管离断术已被广泛接受,而单纯脾切除术仅适合无胃食道静脉曲张的患者,否则易复发出血,LS也不例外。③本文2例患者术后的血氨下降并不足以说明单纯脾切除可预防肝性脑病,相反,单纯脾切除有可能诱发或加重肝性脑病。其一,在脾切除前TIPS分流的门静脉血含有来自脾静脉的血,而脾切除后TIPS引流的几乎全部是肠系膜静脉血,从而使血氨升高。其二,本文在讨论中认为脾切除可同时消除自发脾肾分流从而预防肝性脑病的论点很难成立。单纯LS在技术上很难彻底阻断脾肾静脉间的分流,当存在自发性脾肾分流时,脾切除后则使原本分流脾静脉血的分流通道全部分流肠系膜静脉血,成为近端脾肾分流,这是脾切除(包括联合断流)后肝性脑病发生的重要原因。
Singh R, Wilson MP, Katlariwala P, et al. Accuracy of liver and spleen stiffness on magnetic resonance elastography for detecting portal hypertension: a systematic review and meta-analysis. Eur J Gastroenterol Hepatol. 2021
近日,来自于加拿大阿尔伯塔大学的Singh R等人评估了磁共振弹性成像(MRE)对肝脾硬度的测量及诊断临床显著性门静脉高压(CSPH)的准确性。相关内容发表在European Journal of Gastroenterology & Hepatology杂志上。
该荟萃分析纳入了截止至2019年8月15日的MEDLINE、EMBASE、Scopus、Cochrane和Grey Literature数据库的文献并进行系统评价回顾。研究者分析了包括使用MRE评估10例以上患者肝脏和/或脾脏硬度的原始文章。门静脉高压参考标准定义为顽固性腹水、食管静脉曲张、脑病和/或死亡。由两名独立评审者分析患者临床情况、MRI和诊断性能。荟萃分析采用双变量混合效应回归模型。
结果显示,该项研究共纳入了14项研究,其中12项为评估肝脏硬度的研究,8项为评估脾脏硬度的研究。MRE肝脏硬度的合并加权敏感性、特异性和曲线下面积(AUC)值分别为83%[95%置信区间(CI)72%~90%],80%(95%CI:70%~88%),88%(95%CI:85%~91%)。MRE脾脏硬度的合并加权灵敏度、特异性和AUC值分别为79%(95%CI:61%~90%)、90%(95%CI:80%~95%)和92%(95%CI:89%~94%)。在评估食管静脉曲张时,肝脏和脾脏硬度敏感性和特异性值相当,肝脏硬度为80%(95%CI:66%~89%)和76%(95%CI:62%~86%),而脾脏硬度为75%(95%CI:52%~90%)和89%(95%CI:70%~96%)。
因此,通过MRE评估肝脏和脾脏硬度可以作为检测CSPH的一种补充性无创评估工具。在检测门静脉高压时脾脏硬度可能比肝脏硬度更具特异性及准确性。

(图源自文献)
简评丨宫希军
安徽医科大学第二附属医院放射科
本研究通过荟萃分析评估磁共振弹性成像(MRE)测量肝脏硬度和脾脏硬度对临床显著性门静脉高压(CSPH)的诊断准确性,采用综合/合并数据荟萃分析方法,对于原始的各效应指标数据进行汇总分析。同时,资料提取中考虑到多种因素避免偏倚风险,并采用受试者工作特征曲线分析,以减少变异性和不同临界值的影响,研究设计较为严谨。
MRE肝脏硬度和脾脏硬度诊断CSPH的曲线下面积分别为88%和92%。荟萃分析证实以往研究中通过瞬时弹性成像技术,与肝脏硬度相比,脾脏硬度的特异性更好(90% vs. 80%),因此,更重要的是得出了MRE脾脏硬度的诊断性能优于肝脏硬度的结论,并且也得到了MRE评估肝脾硬度值的支持,此为亮点。最终认为MRE测定的肝脏和脾脏的硬度值可以作为检测肝病患者CSPH的辅助无创性工具,并且有望在筛查中对门静脉高压及其相关疾病的肝病患者进行危险分层。
纳入的各项研究的MRE技术之间存在一定差异,如参数拟合模型、机器序列设置、刺激频率/强度、代表性弹性值以及不同感兴趣区选择等仍然是影响研究结果不可避免的因素。尽管这些在诊断准确性评价方面存在一定不足,未来在CSPH无创诊断中关注于脾脏硬度和基于脾脏病理生理改变的相关的影像学特征,以及MRE对于肝、脾硬度临界值的规范化研究值得进一步探索。

简评丨 高艳景
山东大学齐鲁医院消化内科
奥曲肽通过选择性收缩内脏血管来降低门静脉压力和调整门静脉血流,目前在临床上广泛应用于门静脉高压静脉曲张出血的治疗。临床上该类药物皮下注射或静脉给药生物利用度较高,同时,口服奥曲肽被认为是未来的一种可供选择的剂型。然而,奥曲肽受肠道首过消除作用的影响明显,这可能会较大地限制其疗效。该研究创新性地开展了口服奥曲肽的药代动力学及相关分子机制。
本研究基于胆管结扎造模的肝硬化门静脉高压大鼠模型和体外细胞实验探究了影响肠道奥曲肽吸收的药代动力学和分子机制。结果显示,对照和门静脉高压大鼠模型吸收奥曲肽的部位均为空肠,并受p-gp和MRP2调控。动物模型及细胞研究层面得出p-gp是参与肠道排泄奥曲肽的主要分子,MRP2及CYP3A4亦发挥作用。同时也验证了门静脉高压大鼠模型中p-gp及MRP2的上调表达。因此抑制p-gp、MRP2、CYP3A4可以减少口服奥曲肽的肠道首过效应,可发挥奥曲肽降低门静脉压力的生物学效应。然而,本研究没有阐明门静脉高压大鼠肠道p-gp、MRP2或CYP3A4表达和/或活性失调的机制。此外,如何通过抑制p-gp、MRP2、CYP3A4,减少口服奥曲肽的肠道首过效应仍需更多的研究。
口服奥曲肽使门静脉高压患者在院外用药成为了可能,这可能会为门静脉高压及相关并发症的治疗带来革命性的改变。近期,美国FDA批准了MYCAPSSA(奥曲肽,octreotide)胶囊用于肢端肥大症患者的长期维持治疗。本研究探索了口服奥曲肽在肠道中的首过效应的分子机制,发现了降低该药物在肠道吸收首过效应的干预靶点,为未来新一代的口服奥曲肽制剂的研制奠定了基础,意义重大。
(图源自文献)
简评丨 田明国
宁夏回族自治区人民医院肝胆外科
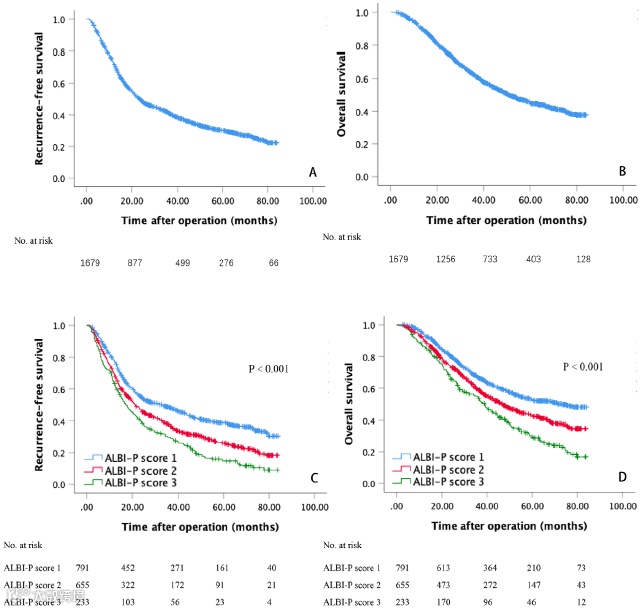
白蛋白-胆红素分级(ALBI)是一种对肝功能评分的方法,基于白蛋白和胆红素两个客观指标通过公式计算得出分值,因Child-Pugh评分牵涉肝性脑病及腹水评级的主观因素,因此有报道认为ALBI在评估肝功能及预测HCC治疗后复发优于Child-Pugh。本文对HCC术后的患者进行了随访研究,并将ALBI与临床显著性门静脉高压(CSPH)结合开发出新的分值(ALBI-P)对术后无复发生存率(RFS)及总生存率(OS)进行评估。通过对1679例患者的研究发现,ALBI-P是HCC术后复发的独立危险因素,且分值越高,RES和OS越短。当ALBI-P与BCLC分级结合后,其对复发预测的能力高于BCLC分级本身以及其他结合方式。本文结论是ALBI-P分值可作为评估HCC肝叶切除后预后的替代方法。
本文的局限性正如作者在讨论部分阐述的一样,其多因素分析资料仅来自单中心,且CSPH的确定仅凭有无胃食道静脉曲张或脾大及血小板降低,而未引入门静脉系统超声多普勒检查指标以及肝静脉压力梯度(HVPG)。另外,需进一步阐明CSPH本身对RFS的预测价值。


扫描二维码
浏览往期文章

(来源:《国际肝病》编辑部)



