

肝切除术(HR)是治疗极早期/早期肝细胞癌(HCC)的一种有效方法[1-3]。然而,肝切除术后肝衰竭(PHLF)是HCC患者HR后的主要并发症,严重影响患者的预后[4]。近期,韩国首尔国立大学医院Jae Seok Bae等发表了一项研究,旨在评估术前CT图像测量的脾脏体积(SV)是否与HCC患者HR后PHLF和总生存期(OS)的发展相关。结果显示,术前CT图像中获得的SVBSA越大,极早期/早期HCC患者HR后PHLF发生率越高,OS越差[5]。


研究方法
该研究纳入317例在2010年1月至2016年12月期间接受术前CT和HR检查的极早期/早期HCC患者。利用半自动体积测量软件从术前CT图像中提取SV值,并除以体表面积得到SVBSA。通过受试者工作特征(ROC)曲线和logistic回归分析确定影响PHLF发展的因素。Cox比例风险模型用于确定OS的预后因素。

研究结果
 PHLF相关因素
PHLF相关因素
317例患者中有72例(22.7%)观察到PHLF。PHLF分级为A级59例,B级12例,C级1例。C级PHLF患者的凝血酶原时间与国际标准化比值较高,为3.3。所有PHLF患者均得到成功治疗,出院时未发生院内死亡。
在单因素分析中,SVBSA与PHLF的发生相关。发生PHLF的患者的中位SVBSA明显大于未发生PHLF的患者(148 cm3 vs. 112 cm3,P<0.001)。脾脏平均直径BSA在伴或不伴PHLF的患者之间的差异无统计学意义(6.06 cm vs. 5.77 cm,P=0.023),而ICG-R15的差异则没有统计学意义(12.3% vs. 10.7%,P=0.076)。根据多因素分析结果,SVBSA、手术时间和手术范围与PHLF的发展独立相关。
ROC分析显示,SVBSA预测PHLF发展的AUC为0.663(95%CI:0.608~0.714,P<0.001),最佳临界值为107.5 cm3。SVBSA相应的灵敏度、特异性、阳性预测值和阴性预测值分别为70.8%(51/72)、58.4%(143/245)、33.3%(51/153)和87.2%(143/164)。同时,CT和ICG-R15预测PHLF发生的AUC分别为0.605(95%CI:0.549~0.660,P=0.006)和0.543(95%CI:0.486~0.600,P=0.286)。对于PHLF的预测,SVBSA的AUC显著高于脾脏直径BSA或ICG-R15的AUC(P分别为0.036或0.026)(图1)。

图1.ROC曲线预测PHLF能力的比较
(引自发表文章)
 OS相关因素
OS相关因素
肝切除术后平均随访62.7±25.4个月,中位值(范围)为63.0个月(2~113个月)。在随访期间,研究者记录了37例HCC相关或与肝脏相关的死亡,以及9例因其他原因(包括脑梗死和颅内出血)导致的死亡。根据生存分析,研究者将与HCC相关或与肝脏相关的死亡视为阳性。1年、3年和5年的OS率分别为98.1%、93.3%和90.6%。
SVBSA是与OS相关的重要因素(危险比HR为3.935;95%CI为1.520~10.184;P=0.005),利用最小P值方法确定最佳临界值为146 cm3。
研究者还获得了HCC大小、ICG-R15、脾脏直径BSA、总肝脏体积BSA和残余肝脏体积BSA的最佳临界值。
之后,研究者使用Cox比例风险模型进行了单因素和多因素生存分析(表1)。在单因素分析中,SVBSA>146 cm3是影响OS的显著因素之一。在多因素分析中,SVBSA>146 cm3与CT图像上的HCC大小>8.6 cm和病理上的微血管浸润是预测OS的独立因素。
表1.临床特征与脾脏大小和OS之间的关系
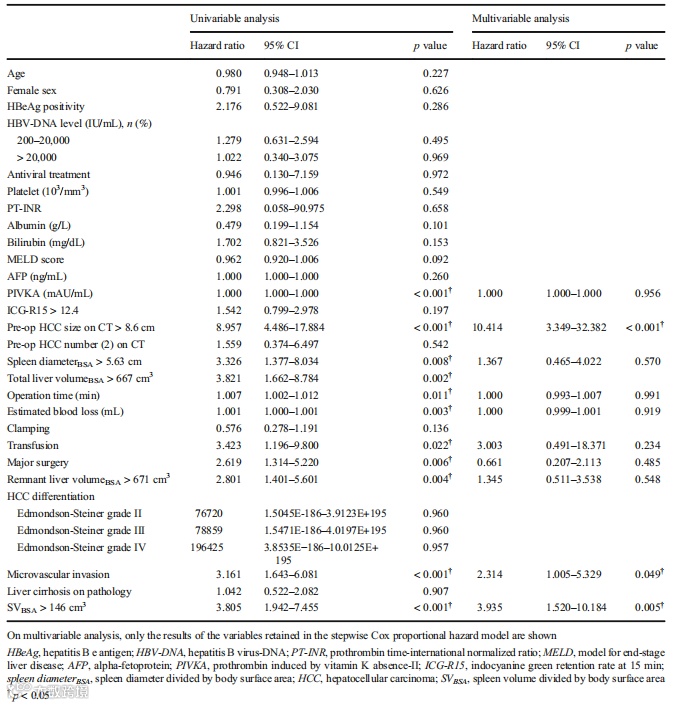
(引自发表文章)
245例SVBSA≤146 cm3患者的1年、3年和5年OS率显著高于72例SVBSA>146 cm3的患者(分别为99.2% vs. 94.4%、96.3% vs. 83.0%以及95.0% vs. 78.7%,P<0.001,图2)。
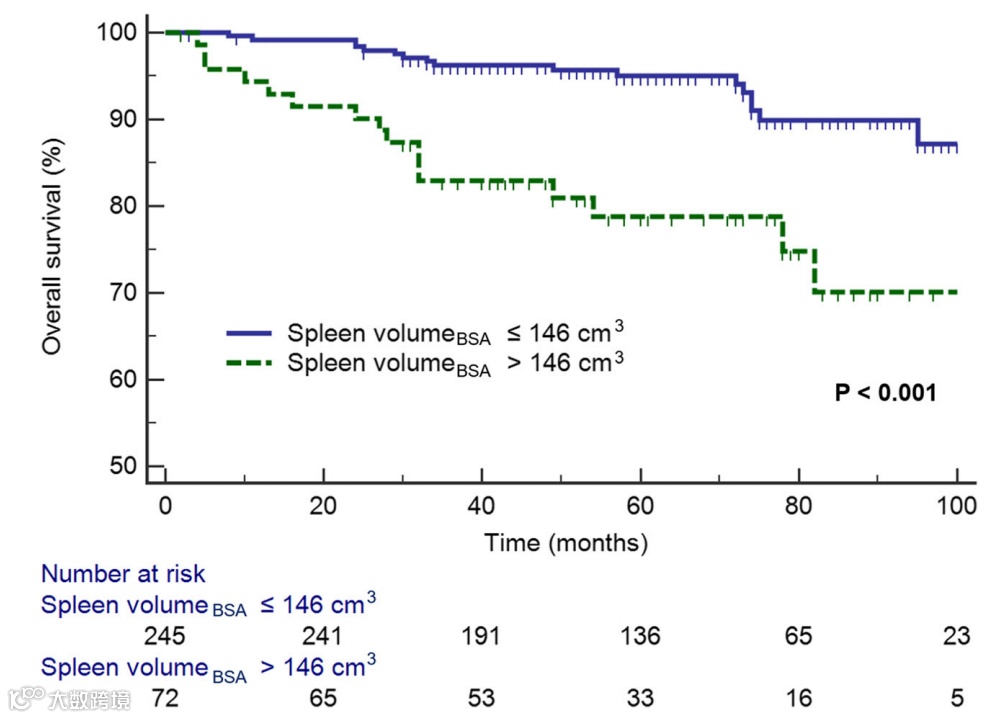
图2.计算Kaplan-Meier曲线,以确定根据术前CT图像获得的SVBSA分层患者的生存差异
(引自发表文章)

研究结论
在HCC患者中,SVBSA越大,HR后PHLF发生率越高,OS越差。因此,SVBSA在临床上有助于选择合适的手术方案。
●PHLF患者的SVBSA明显高于未发生肝衰竭的患者(148 cm3 vs. 112 cm3,P<0.001);
●SVBSA预测PHLF发生的ROC曲线下面积为0.663(P<0.001);
●SVBSA是影响OS的重要因素(危险比为3.935;95%CI为1.520~10.184;P<0.001),最佳临界值为146 cm3。
(来源:《国际肝病》编辑部)




