
作者:王晓雨 李一凡 孙明宇
审校:孙超
天津医科大学总医院消化内科

编者按:肝硬化的主要特征包含营养不良,而内脏脂肪是评估营养不良的重要指标之一。2021年11月,天津医科大学总医院消化内科王晓雨医师、孙超副主任医师在Frontiers in Nutrition(IF 6.576)上发表文章“Visceral Adiposity Associates With Malnutrition Risk Determined by Royal Free Hospital-Nutritional Prioritizing Tool in cirrhosis”。该项研究结果表明,肝硬化患者中内脏脂肪与营养不良相关,提示人们要加强关于内脏型肥胖的认识,积极进行针对性的干预策略。本刊特邀请孙超教授团队撰文介绍该项研究成果。

Frontiers in Nutrition网站文章页截图
研究背景
营养不良在肝硬化患者中非常普遍,且会增加人群并发症的发生率和死亡率。因此,筛查出营养不良的患者并对其进行营养治疗,对于降低死亡率、全身炎症反应和感染是非常必要的。英国皇家自由医院营养优先工具(RFH-NPT)是一种专门针对肝硬化的营养筛查工具,可以预测疾病恶化和不良结局[1]。本团队既往的研究也表明,在肝硬化患者中,通过RFH-NPT评估的营养不良风险与免疫功能紊乱显著相关。
体成分包括肌肉和脂肪组织,对于客观评估患者的代谢和营养状况是非常重要的。本团队前期的研究已经充分阐明了几种体成分异常对肝硬化患者预后的影响,最近国外的研究也聚焦于肌少症与营养不良的关系。然而,在肝硬化患者中,脂肪成分异常和营养不良的关系仍不清楚。内脏脂肪过度蓄积可能会促进炎症反应和代谢失调。同样地,皮下脂肪消耗会导致内脏脂肪蓄积和胰岛素抵抗。有趣的是,一些研究表明,脂肪组织的分布而非含量是决定各种肝病预后的主要因素。
基于上述问题,本课题组于2021年11月在Frontiers in Nutrition上发表文章“Visceral Adiposity Associates With Malnutrition Risk Determined by Royal Free Hospital-Nutritional Prioritizing Tool in cirrhosis”,旨在研究住院肝硬化患者内脏型肥胖与营养不良风险之间的关系。
研究方法
本研究纳入了176例住院的肝硬化患者,通过患者的CT图像,得到了总脂肪指数(TATI)、内脏脂肪指数(VATI)、皮下脂肪指数(SATI)、内脏脂肪/皮下脂肪组织比率(VSR)等评估指标,以上部分指标的截断值在我们前期的研究中已经得出:VSR(男性1.47,女性1.29)、SATI(男性:29.10 cm2/m2,女性:26.75 cm2/m2)、VATI(男性:28.42 cm2/m2,女:44.02 cm2/m2)。最后通过RFH-NPT将肝硬化患者的营养不良风险分为三组,即低危(0分)、中危(1分)和高危(2~7分)。
研究结果
◆基线特征
根据RFH-NPT危险度分级:低/中危组79例(44.89%),高危组97例(55.11%)。两组患者的性别、CTP分级、病因、有无腹水、BMI、有无肌少症、内脏型肥胖、白蛋白、肌酐、PT-INR有显著差异。营养不良高风险的患者呈现出的特点包含:男性为主,多为CTP-B/C级,酗酒,大多出现腹水,较低的BMI,大多合并肌少症和内脏型肥胖,血清白蛋白较低,肌酐和PT-INR较高。
◆营养不良的独立危险因素
单因素分析表明:年龄(P=0.041),男性(P=0.005),酗酒(P<0.001),CTP分级(P=0.011),腹水(P<0.001),BMI(P=0.001),肌少症(P= 0.007),内脏型肥胖(P<0.001)和白蛋白(P=0.008)与营养不良高风险显著相关。考虑到酒精性肝病在原始RFH-NPT评分中权重较大,我们决定构建2个多因素logistic回归模型。在模型1中,我们发现:内脏型肥胖具有临界意义(OR=2.705,95% CI:0.968~7.557,P=0.058)。在排除病因的模型2中,男性(OR=2.884,95% CI:1.336~6.115,P=0.006)、BMI(OR=0.879,95% CI:0.812~0.951,P=0.001)、白蛋白(OR=0.934,95% CI:0.882~0.989,P=0.019)和内脏型肥胖(OR=3.413,95% CI:1.344~8.670,P=0.010)为住院肝硬化患者营养不良风险的独立危险因素。
◆脂肪组织和RFH-NPT的性别分层分析
既往研究表明,脂肪组织的分布具有性别差异。在肝硬化患者中,男性的VATI水平较高,而女性则是SATI水平较高。因此,基于RFH-NPT,我们进一步探讨了不同性别的脂肪成分与营养不良风险之间的关系(图1)。
结果显示:不同营养不良风险患者的TATI(男性:100.80 ± 43.54 vs. 92.19 ± 37.94 cm2/m2,P=0.355;女性:111.70 ± 54.65 vs. 98.19 ± 49.92 cm2/m2,P=0.219)、SATI(男性:49.50 ± 25.16 vs. 36.39 ± 15.96 cm2/m2,P=0.058;女性:62.23 ± 34.50 vs. 50.91 ± 27.35 cm2/m2,P=0.122)和VATI(男性:51.09 ± 23.60 vs. 55.80 ± 25.88 cm2/m2,P=0.422;女性:49.42 ± 24.48 vs. 47.28 ± 26.05 cm2/m2,P=0.684)无显著差异。相反地,男性患者营养不良高危组发生内脏型肥胖的比例高于低/中危组(47.27% vs. 17.86%,P=0.009),在女性中,这一差异具有临界意义(19.05% vs. 5.88%,P=0.061)。
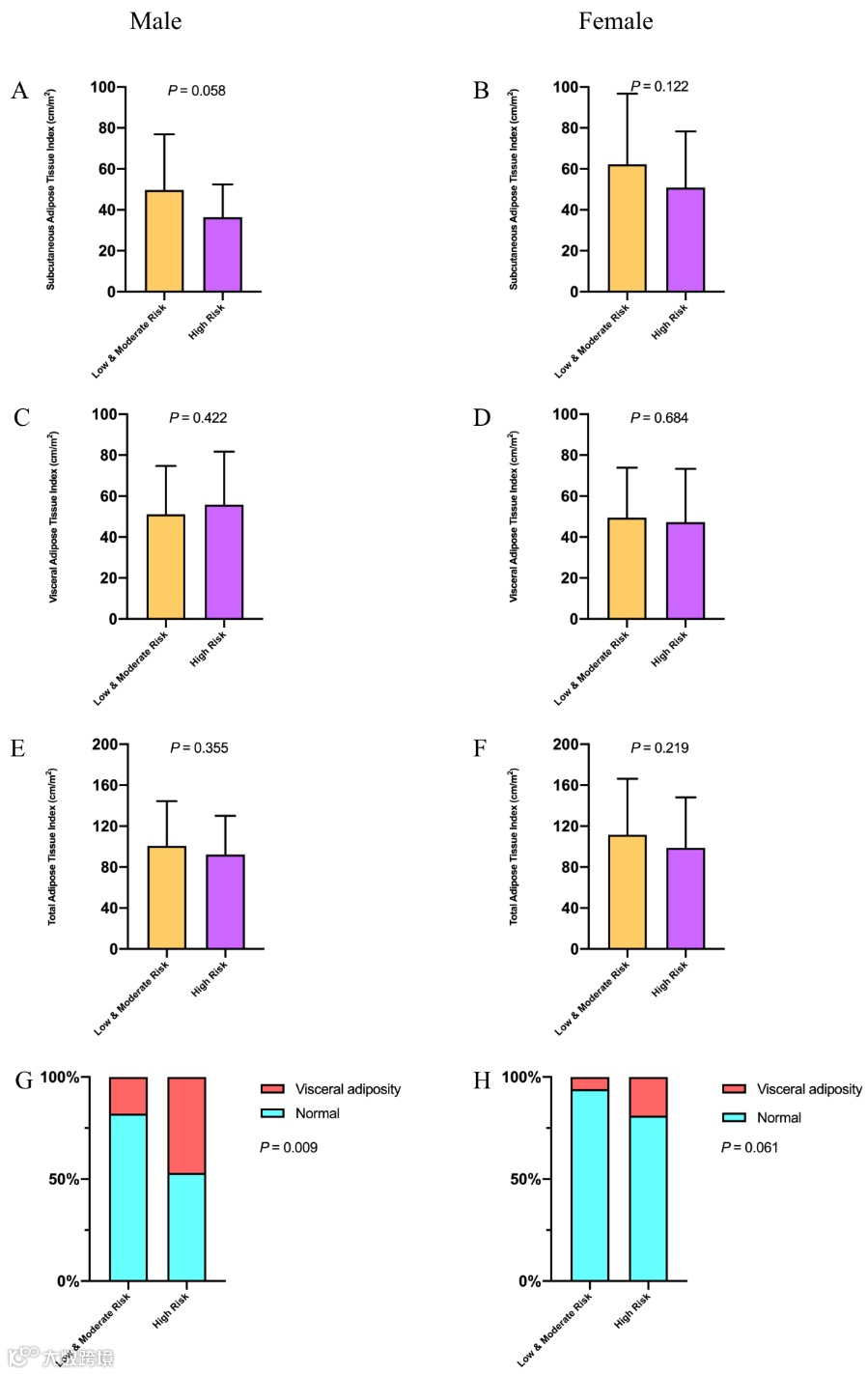
图1.按照性别分组的脂肪成分和RFH-NPT不同危险度组间比较
小结
越来越多的证据表明,营养不良是肝硬化患者出现并发症和死亡的一个预测因子,采取针对性的干预措施以改善营养不良状态和相关并发症具有重要临床意义。鉴于目前还没有关于营养不良风险筛查的通用方法,基于数个肝病中心和学会的推荐,并结合本团队前期的研究,我们采用RFH-NPT识别高营养不良风险的患者。
本研究发现,住院的肝硬化营养不良高危患者BMI水平较低,内脏型肥胖比例较高。尽管在大多数评估肝硬化预后的研究中,BMI一直备受关注,但它并不是一个准确的体成分评估指标,因其不能区分肌肉和脂肪组织,并且不能排除肝硬化患者液体潴留带来的混杂影响[2]。换言之,液体潴留(如大量腹水)可能会掩盖营养不良造成的体重减轻。因此,我们建议使用横断面CT或MRI图像,而不是BMI,作为评估体成分的非侵入性工具。
我们的研究证实,与内脏型肥胖相对应的高VSR与较高的营养不良风险相关,在对性别进行分层研究时发现脂肪组织的分布而非单一部位脂肪指数(VATI、SATI)具有统计学意义。我们的前期研究也表明,脂肪分布异常是肝硬化患者预后不良的危险因素[3]。内脏脂肪与皮下脂肪在解剖部位、脂肪细胞大小、胰岛素敏感性、释放的脂肪细胞因子和脂解能力方面存在显著差异[4]。内脏脂肪主要负责分泌各种促炎细胞因子,如IL-1、TNF-α和有毒的游离脂肪酸(FFAs)。这些FFAs通过门静脉直接运输到肝脏,导致氧化应激、脂质过氧化和肝细胞炎症。相反,皮下脂肪已被证实可摄取和贮存甘油三酯和血浆FFAs,并可产生瘦素,调控免疫反应和脂质代谢。我们近期的研究表明通过中性粒细胞/淋巴细胞比率(NLR)测定的免疫功能紊乱与肝硬化患者RFH-NPT评估的营养不良风险有关,而IL-6、IL-8与NLR呈正相关。综合以上,我们推测VSR可能与肝硬化患者体内的慢性炎症状态更密切相关,而慢性炎症则促进了营养不良的进展。
综上所述,应用CT评估脂肪组织分布有助于对肝硬化患者进行营养不良评估,对准确识别内脏型肥胖并制定针对性的治疗策略具有重要意义。
通讯作者
孙超,副主任医师,本科毕业于北京大学医学部,天津医科大学医学/理学博士,日本兵库医科大学研究员。2020年度天津医科大学总医院“十佳科技工作者”。全国疑难及重症肝病攻关协作组成员。主持完成国家自然科学基金一项。担任SCI期刊Journal of Clinical and Translational Hepatology编委,Frontiers in Pharmacology/Mediators of Inflammation客座编辑。2020年在欧洲肝脏研究学会(EASL)年会做口头发言,2021年在美国肝病研究学会(AASLD)年会做壁板展示。获得EASL的“Full Bursary”和APDW的“Travel Grant”奖励。以通讯作者在Clinical Nutrition, Liver International, Cell Death & Disease, Hepatology Communications等杂志发表SCI文章40篇,他引451次,h指数12,研究成果被美国胃肠内镜学会(ASGE)和EASL发布的临床实践指南引用。目前研究方向为调节性细胞死亡在急慢性肝损伤中的作用机制,体成分异常、营养不良、衰弱、睡眠障碍以及微量元素对肝硬化预后的影响及干预措施。
第一作者
王晓雨,天津医科大学总医院消化内科医师、讲师,毕业于天津医科大学,获医学博士学位。入选2021年天津医科大学总医院“卓越新星”培育项目。多次在AASLD等国内外学术会议上做口头发言和壁报展示,并获得iGES的Young Investigator’s Award。以第一/共同第一作者身份在Clinical Nutrition, Frontiers in Nutrition, Journal of Parenteral and Enteral Nutrition等SCI期刊发表论文9篇,单篇最高影响因子7.66,累计影响因子40余分。目前研究方向为慢性肝病与营养不良、衰弱、体成分异常之间的关系。

2021-09-02

2021-08-06

2021-06-10

2021-05-28

2021-03-30

2021-10-03

(来源:《国际肝病》编辑部)






