
慢性丙型肝炎病毒(HCV)感染是肝细胞癌(HCC)的重要风险因素。当前已经认识到,尽管清除HCV能降低丙型肝炎患者整体的HCC风险,但并不等于清除这一风险,尤其是在肝硬化人群中。但目前并没有很好的手段能够区分这部分获得了持续病毒学应答(SVR)但仍具有HCC高风险的患者。近期在Gastroenterology杂志上在线发表的日本学者的一项研究对这个问题进行了探索。
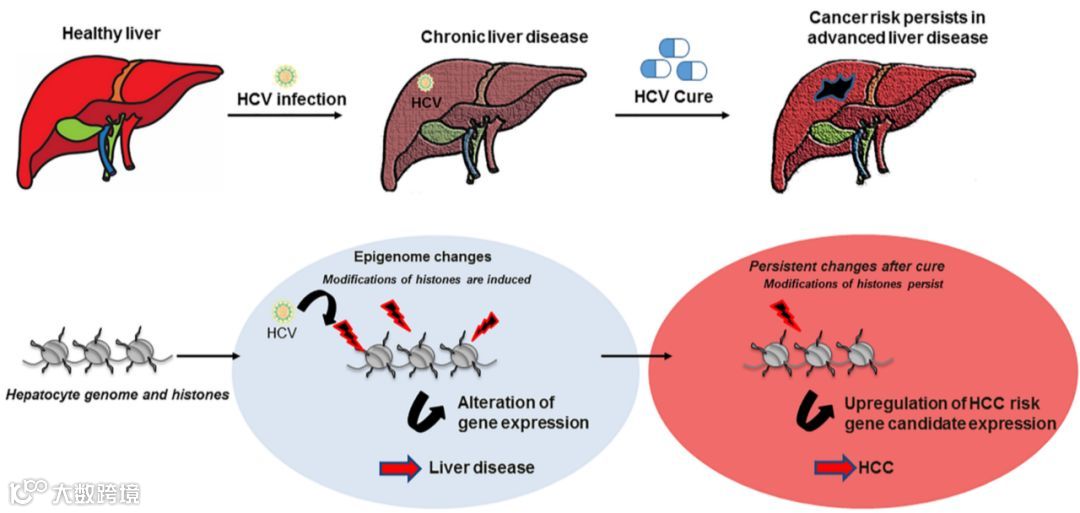
(图源自公开发表的原文献)
研究对象包括6例没有感染HCV感染的患者(对照)、18例慢性HCV感染患者、8例经DAA治疗后获得治愈的慢性HCV感染患者、13例经干扰素治疗后获得治愈的慢性HCV感染患者、4例慢性HBV感染患者和7例非酒精性脂肪性肝炎患者。
研究者使用基于ChiPmentation的染色质免疫共沉淀测序(ChiP-Seq)和转录组测序(RNA-Seq)方法对上述受试者的肝组织样本进行了基因组分析。比较HCV和其他肝病病因各自诱导的表观遗传学修饰差异。
另一方面,研究者将人类肝细胞移植到uPA/SCID小鼠,获得有人源化肝脏的小鼠,给小鼠注射来自丙型肝炎患者的血清,使其感染HCV,随后再给予小鼠DAA以根除病毒。通过综合通路分析来鉴定与HCC风险相关的通路,并在前述8例经DAA治疗后获得SVR的丙型肝炎患者的配对HCC组织中进行验证。
研究者发现,慢性HCV感染可特异性地诱导H3K27ac(一种组蛋白修饰)全基因组变化,H3K27ac修饰与活化的启动子和增强子有关,与转录激活也有关。这些变化在DAA或干扰素治疗获得SVR后持续存在。
对患者肝脏组织以及人源化肝脏小鼠的肝组织进行的综合通路分析显示,HCV诱导的表观遗传学改变与肝癌风险相关。计算分析显示SPHK1基因的表达增加与HCC风险相关,SPHK1为一种脂质激酶,能够介导鞘氨醇磷酸化而形成SP1,是细胞凋亡抑制和增殖促进的主要调节因子。
上述结果在一个独立的HCV相关肝硬化患者队列中(216例,其中21例清除了病毒)得到了验证。
作者总结认为,HCV诱导的一些表观遗传改变和基因表达改变与HCC风险有关,在病毒清除后仍持续存在,也许有必要针对这些变化采取措施,以预防丙型肝炎患者发生肝癌。
原文链接:Hamdane N, Jühling F, Crouchet E, et al. HCV-induced Epigenetic Changes Associated With Liver Cancer Risk Persist After Sustained Virologic Response. Gastroenterol. 2019 Feb. https://doi.org/10.1053/j.gastro.2019.02.038
(来源:《国际肝病》编辑部)




