



简评丨祁小龙
兰州大学第一医院门静脉高压研究所(中心)

简评 | 尉文新
Brusilovskaya K, Königshofer P, Schwabl P, et al. Vascular Targets for the Treatment of Portal Hypertension. Semin Liver Dis 2019
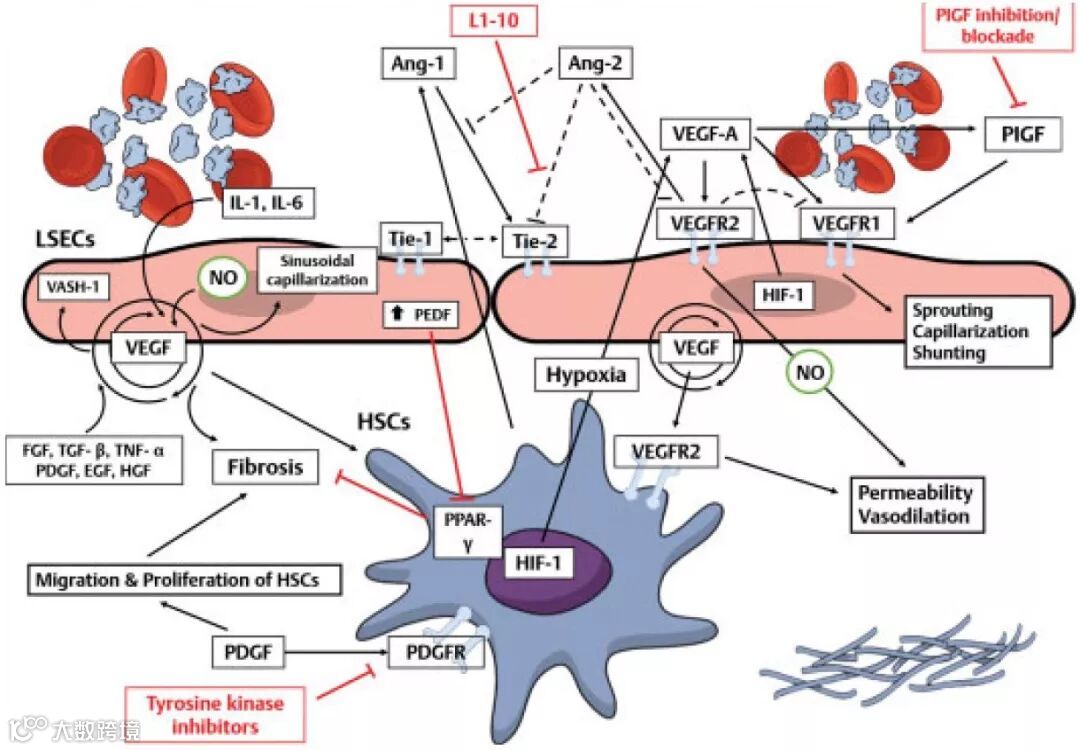
简评 | 赵颖
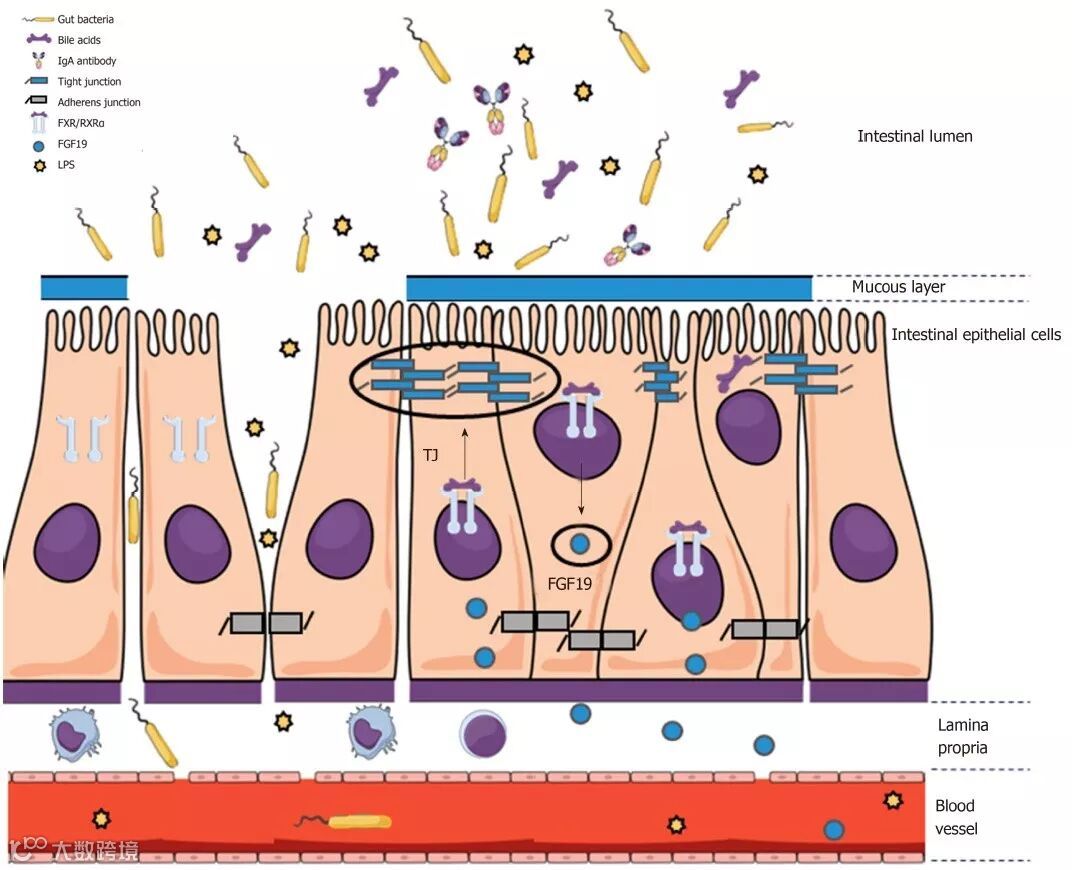
简评丨向慧玲
天津市第三中心医院消化科

简评 | 朱贺
Semmler G, Scheiner B, Schwabl P, et al. The impact of hepatic steatosis on portal hypertension. PLoS One 2019

简评丨向慧玲
天津市第三中心医院消化科



扫描二维码
浏览往期文章
(来源:《国际肝病》编辑部)




