

识别上方二维码
进入《中华肝脏病杂志》小程序
注册后即可下载观看全文PDF

引用本文

中华医学会肝病学分会. 经颈静脉肝活检专家共识[J]. 中华肝脏病杂志, 2022, 30(11):1144-1150.DOI:10.3760/cma.j.cn501113-20221027-00523.
通信作者:
刘福全,首都医科大学附属北京世纪坛医院介入治疗科 首都医科大学肝硬 化及门脉高压临床诊疗与研究中心,北京 100038,Email:lfuquan@aliyun.com;
贾继东, 首都医科大学附属北京友谊医院肝病中心 首都医科大学肝硬化及门脉高压临床诊疗 与研究中心,北京 100050,Email:jia_jd@ccmu.edu.cn;
徐小元,北京大学第一医院感染 疾病科,北京 100034,Email:xiaoyuanxu6@163.com

摘要
肝活检病理学检查是临床肝脏病学中最常用及最重要的诊断手段之一。经颈静脉肝活检(TJLB)目前在临床应用于有明显凝血功能障碍和/或肝前腹水的患者,拓宽了肝活检的适应证。国内目前尚无专门的TJLB操作规范,病理取材及组织标本处理也无统一的标准流程。中华医学会肝病学分会邀请国内相关领域的专家,就TJLB的适应证、禁忌证、操作方法、病理标本取材、处理等问题,进行文献归纳总结并编写本共识,以利于其在临床上的更规范、更合理应用。

肝脏穿刺病理学检查(简称肝活检)是临床肝脏病学中最常用、也是最重要的诊断手段之一[1],经常用于急/慢性肝病患者的病因诊断、疾病分期、疗效评估和预后判断[2-4]。其主要目的包括:第一是病因诊断,包括不明原因的肝功能异常(临床怀疑非酒精性脂肪性、药物性、自身免疫性、遗传代谢性肝病或血管性肝病等),不明原因黄疸/肝内胆汁淤积、发热以及全身性疾病累及肝脏等,影像学发现肝脾肿大、肝脏肿块、局灶性或弥漫性结节增生等。第二是判断预后,包括慢性肝病/肝炎的分期和分级,供体肝移植前评估以及移植后受体肝功能异常状态诊断及评估等。第三是疗效评估,主要用于决定停药时机或进一步治疗方案,以及在临床研究中确定组织学疗效。
肝活检技术主要包括经皮肝穿刺活检、手术或操作中肝活检(包括外科开腹手术、腔镜及内镜术中肝活检)以及颈静脉肝活检(transjugular liver biopsy,TJLB)。在临床上最常用的经皮肝脏穿刺活检,在大部分情况下是安全的。但是,当患者有重度凝血功能异常、血小板数量过低或者有大量腹水时,经皮肝穿刺活检有较大风险。外科手术或操作中肝活检的优势是穿刺路径短、甚至可以直视下穿刺,但仅适用于有相应手术或操作适应证的患者[5]。1964年Dotter等[6]在犬身上首次尝试了TJLB;1967年Hanafe等在研究经颈静脉肝静脉插管行胆道造影时,探讨了经颈静脉取肝活检的可能性,并于1970年报道了首例在人体实施的TJLB[6]。与经皮肝穿刺活检相比,TJLB对于有明显凝血功能障碍和/或肝前腹水的患者更为安全,因此拓宽了肝活检的适应证[2-4,7-11]。
近年来,国内对TJLB应用逐渐增多,但尚无专门的TJLB操作规范,病理取材及组织标本处理也无统一的标准流程[12]。因此,中华医学会肝病学分会邀请国内肝病、消化、影像、介入及病理等相关领域的专家,就TJLB的适应证、禁忌证、操作方法、病理标本取材、处理等问题,进行文献归纳总结并结合我国的临床实际情况,编写了本共识,以利于TJLB在临床上的更合理应用。

一、TJLB适应证[3-4,7-11]
1.需要肝活检但存在经皮穿刺活检绝对或相对的禁忌证:(1)凝血功能障碍或低血小板血症:国际标准化比值(international normalized ratio,INR)>1.5和/或凝血酶原时间(prothrombin time,PT)延长>4 s,或血小板计数(platelet count,PLT)<50×109/L时;(2)肝前腹水。
2. 需要同时行肝静脉压力梯度(hepatic venous pressure gradient,HVPG)或右心导管检查者,或者需要进行经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt,TIPS)或直接肝内门体静脉分流术(direct intrahepatic portosystemic shunt, DIPS)者。
3.其他适应证包括:(1)肝脏萎缩;(2)病态肥胖难以行经皮肝穿刺;(3)经皮肝活检失败或拒绝经皮肝活检;(4)不能中断抗凝或抗血小板治疗;(5)患有肝紫癜病及其他严重凝血疾病等。

二、TJLB禁忌证
一般来说,没有TJLB的绝对禁忌证。严重凝血功能障碍时,如INR>3.5或凝凝血酶原活动度(prothrombin activity,PTA)<30%,或PLT<10×109/L,建议先补充血液制品纠正凝血功能障碍,或应用升血小板药物[13]。
相对禁忌证包括:(1)未能控制的脓毒症/败血症;(2)显著胆道梗阻或急性胆管炎;(3)缺乏静脉穿刺通路(颈内静脉血栓、上下腔静脉阻塞、肝静脉闭塞等);(4)多囊性肝病;(5)肝包虫病;(6)肾功能衰竭;(7)严重心肺功能障碍;(8)对碘造影剂过敏;(9)患者不能或不愿配合操作。

三、TJLB术前检查及患者准备
(一)知情同意和术前检查
1.签署同意书:仔细询问患者病史,明确肝脏穿刺适应证,在患方充分了解操作的必要性、有无其他替代检查及潜在风险的基础上,由患者或家属签署知情同意书。
2.实验室检查:血常规、生化、凝血功能指标,及心肌酶、B型钠尿肽检查,及常规传染病抗原或抗体筛查等。
3.其他辅助检查:(1)心电图,既往有心脏基础疾病者还应行心脏超声检查;(2)腹部增强CT或者增强核磁共振,以明确下腔静脉及肝静脉通畅程度、肝静脉走行及肝静脉与肝实质的解剖关系;(3)若不能行增强CT或核磁共振,可行肝脏血管超声检查;(4)颈部血管超声明确颈静脉通畅情况。
4.抗凝及抗血小板药物的管理:若患者正在服用维生素K拮抗剂等抗凝药物,术前3 d改用低分子肝素,TJLB操作当日改为半量低分子肝素注射,操作后确认无腹腔出血等并发症,术后当日恢复使用抗凝药物[6]。若患者正在服用抗血小板药物,需停用抗血小板药物3~7 d,并使用低分子肝素代替[2]。
(二)术前患者准备
1.询问麻醉药品和碘剂过敏史。
2.若在局部麻醉下操作,术前可不禁食水;若需镇静麻醉,术前禁食水2 h;若需全麻下操作,术前禁食水6~8 h。
3.术前留置静脉通路(前臂静脉留置针或者深静脉置管等)。

四、器械准备和操作过程
(一)术前器械准备(图1)

1.血管穿刺针
2.9 F~10 F血管短鞘
3.40 cm-9~10F血管长鞘
4.0.35"超滑泥鳅导丝
5.0.35"加硬交换导丝
6.经颈静脉肝活检穿刺套件(包括经颈静脉穿刺导引器、经颈静脉活检针等)
7.C2导管或J头多功能导管
8.5F双腔测压导管(术中需测定HVPG时)
9.漂浮导管(术中需行右心导管检查时)
(二)术中操作
1.监护及麻醉:(1)予患者全程心电监护,包括心率、血压、血氧饱和度、呼吸频率,鼻导管氧气吸入(1~2 L/min);(2)TJLB一般可在局部麻醉下完成。若患者对疼痛敏感或配合度差,麻醉医师根据患者肝功能状态,予低剂量镇静麻醉,推荐咪达唑仑,可联合舒芬太尼。低剂量麻醉剂可减轻患者操作中不适,并且对血压影响较小。必要时在全身麻醉下进行操作。
2.建立静脉通路:首选右侧颈内静脉入路,置入10~15 cm/9~10 F短鞘。若右侧颈内静脉不可用,可选择左侧颈内静脉入路,并可在超声引导下操作。
3.HVPG测定:若需要行HVPG测定,可先行该检查,以避免活检造成的不适影响测压准确性。
4.肝静脉置管
(1)造影明确肝静脉情况:将5 F导管(Cobra导管、多功能导管或单弯导管)置于目标肝静脉,造影剂确认肝静脉通畅及明确肝静脉走行、与下腔静脉角度等。
(2)穿刺导引器置于肝静脉:根据肝静脉与肝实质的解剖关系,选择合适的肝静脉进行活检。若3只肝静脉均闭塞,可于肝后段下腔静脉进行穿刺活检。
(3)导引器置于肝静脉:通过导管及加硬导丝,将穿刺导引器置于目标肝静脉,通过造影剂确认,一般置于距离肝静脉开口1~3 cm处。
(4)长鞘辅助:肝静脉与下腔静脉角度过大,穿刺导引器不能固定于肝静脉的患者,可使用40 cm-9~10 F长鞘进行辅助:将长鞘置于肝静脉内,再置入导引器。
5.肝活检:活检方法包括Tru-Cut活检针法及Menghini法,我国常用Tru-Cut活检针法。
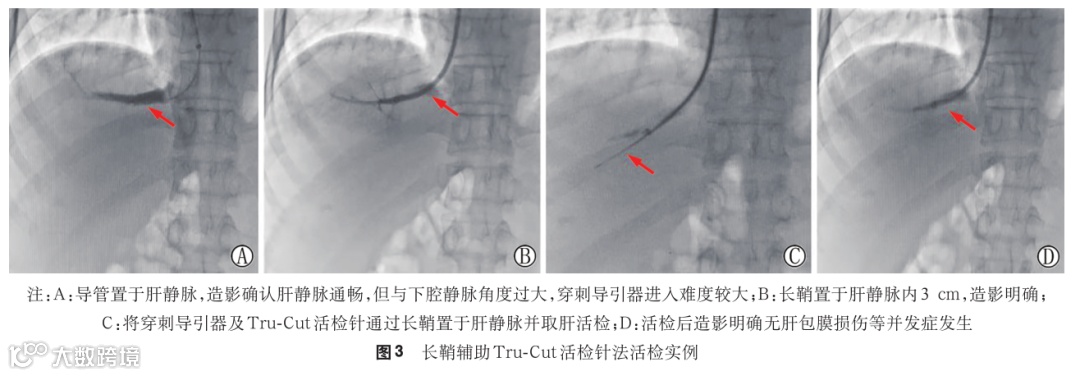
(1)Tru-Cut活检针法(图2、3):

a.活检针准备:Tru-Cut活检针为半自动活检针。使用前向后拉动尾部针柄,听到“咔哒”声音。
b.取活检:将Tru-Cut活检针送入导引器,在透视下,将导引器轻轻转向目标方向,柔和向前推顶住肝静脉壁,活检针尖刺入肝实质1~3 mm,按压针柄推出针芯,送入肝实质。加压针柄击发,等待5~10 s使活检针充分切割肝组织。拔出活检针,拉针柄上弦后推出针芯;将活检组织黏在滤纸条上,或将针芯在固定液或等渗盐水瓶内轻轻晃动,使肝组织完整脱离活检针。
c.再次注入造影剂,明确有无肝包膜损伤等并发症发生。
d.可重复上述步骤穿刺1~2次,保证取到足够的肝脏组织以利于做出病理诊断。
e.操作过程中,尤其是器械经过心脏时,随时关注患者有无不适主诉、生命体征、意识情况、心律、血压、呼吸、血氧情况。
(2)Menghini法:
a.沿弯头导引器,将穿刺针和配套外导管置于肝静脉内3~4 cm。
b.取活检:向目标方向轻推Menghini活检针,进入肝实质1~2 cm,将注射器连接穿刺针尾端,抽负压吸取肝组织并匀速将穿刺针退出肝实质,于体外向前推注射器取出肝组织。
c.取活检后需再次注入造影剂,明确有无穿出肝包膜外等并发症发生。
d.上述步骤可重复1~2次,保证取到足够的肝脏组织。
6.拔除血管鞘并加压包扎。

五、TJLB的并发症及处理
(一)并发症的分级方法
目前,有关TJLB并发症的分级多沿用2003年美国介入放射学会(Society of Interventional Radiology,SIR)的建议,将TJLB并发症分为轻微型和严重型[9],见表1。2017年,欧洲心血管和介入放射学会(Cardiovascular and Interventional Radiological Society of Europe,CIRSE)依据并发症造成的后果及后遗症的严重程度,制定了相应并发症的分级方法[10]。

(二)TJLB的常见并发症
TJLB术后并发症的总体发生率约为7.1%,其中轻微并发症6.5%,严重并发症0.6%,死亡发生风险为0.1%[11]。并发症主要发生在颈内静脉穿刺及肝组织穿刺活检过程中。
轻微并发症包括:发热、颈部血肿、出血、疼痛、穿刺到颈动脉、Horner综合征、发声困难、上肢麻木、室上性心动过速、轻度低血压、腹痛、无症状肝包膜穿孔、肝脏被膜下小血肿、肝内静脉门静脉漏、肝内静脉动脉漏、肝内胆管漏及胆道少量出血等。
严重并发症包括:肝脏被膜下较大血肿、腹腔内出血、下腔静脉穿孔、心房穿孔、心包填塞、肾静脉穿孔、肝外胆管漏、室性心律失常、气胸及呼吸暂停等,其中腹腔内大量出血和室性心率失常可导致死亡。
(三)发生并发症的相关因素
有研究结果显示,使用Tru-Cut法及细针穿刺可以减少肝穿刺相关并发症的发生[14]。肝穿刺的次数与并发症的发生是否有相关性尚存在争议。多数研究结果显示,穿刺3~4针时可以更好地满足病理诊断的需要,且并未明显增加并发症发生风险[15]。此外,儿童TJLB术后并发症及严重并发症的发生率高于成人,分别为6%~17%和1.5%~3.0%,死亡发生率为0.6%;严重并发症为肝脏被膜损伤导致的出血及室性心律失常[14,16-18]。
(四)TJLB并发症的处理
1.轻微并发症:对于轻微并发症,大多无需治疗或仅需要简单处理。对于无症状肝包膜穿孔、肝脏被膜下小血肿、胆道出血的情况,需要对患者生命体征进行监测,并于穿刺后24 h进行复查。
2.严重并发症
(1)出血:腹腔内出血和肝被膜下血肿形成与肝穿刺造成被膜损伤有关,多在穿刺后3 h内出现明显临床症状,但如有假性动脉瘤形成,这一时间可能延长。因此,每次穿刺后均应注射造影剂以早期发现被膜损伤及出血。若患者术中或术后发生血液动力学改变,如血压降低、心率加快,或发现活动性腹腔内出血,可行动脉栓塞止血治疗[11]。对于有明显血液动力学改变的患者,需进行严密监测并输注红细胞[19]。
(2)胆漏:穿刺损伤肝外胆管可造成腹腔内胆漏发生,患者可出现剧烈右上腹痛。胆管造影和CT等检查可及时诊断。对于胆漏,可行经内镜逆行性胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)十二指肠乳头括约肌切开或内镜下鼻胆管引流术(endoscopic nasobiliary drainage,ENBD)治疗以降低胆道内的压力,使胆汁进入十二指肠,损伤胆道得到恢复[20]。肝内动脉-胆道漏引起的胆道出血,可行动脉栓塞治疗[21]。为避免和减少以上穿刺相关并发症,活检针尖与肝包膜之间应留有足够的距离;此外,选择肝右静脉穿刺可降低上述风险。
(3)心脏相关并发症:室性心律失常可发生于经颈静脉穿刺置管及置入导丝时,导丝进入右心室可引起心律异常。有报道左束支传导阻滞的患者,导丝置入时出现心脏停搏,可能与导丝损伤右束支有关[21]。发生心脏停搏后,应立即予患者心肺复苏,必要时可置入临时起搏器。身高170 cm以下、女性,及既往有左束支传导阻滞是发生上述并发症的危险因素。为避免其发生,在进行右侧颈内静脉置管时,放置导丝的长度应<20 cm,且全程在心电监护及X线透视或超声引导下进行[21]。

六、TJLB术后监测
患者返回病房后,常规卧床休息,并给予心电监护,重点监测患者的脉搏、血压,有无腹痛症状及腹部体征,建议术后至少监测6 h[22-24]。有凝血功能障碍和/或血小板减少的患者,应特别注意早期发现和及时处理可能出现的腹腔或胆道等部位的出血。
对于没有发热、腹痛、心悸、低血压的患者,不推荐常规进行血常规及腹部超声的监测[23]。术后6 h后可正常进食。
目前,尚无证据证明术后需要常规使用抗生素。建议患者术后48 h内避免进行跑步、抬举重物等剧烈活动。

七、病理标本要求
肝脏病理标本的大小和完整性对于肝脏疾病诊断至关重要。为有助于肝脏疾病的病理诊断,肝脏标本应超过15 mm并至少含有6个汇管区(图4,5)[25] ;若需要进行疾病严重程度分级分期,需要至少20 mm长度以及11个汇管区,较小的样本可能低估或者高估疾病严重程度[4,26]。由于经颈静脉肝脏穿刺所使用的18~19G穿刺针内径较小,建议至少采取2次活检以获取足够的标本[27-29]。

肝活检标本应立即置于10%中性甲醛溶液(pH=7)中固定后送检。若需要行特殊检查则置于相应特殊固定液中:如需要进行电子显微镜观察,应采用戊二醛固定;如观察脂肪变,应采用新鲜组织做冰冻切片;如考虑存在病原体感染,则应进行组织培养。因相对于经皮肝活检来说,TJLB取得肝组织更小、更易碎,故后续包埋、脱水、切片及染色过程均需要精心优化专门的相关技术流程,以保障病理诊断结果的可靠性。
综上所述,TJLB是相对安全的肝活检方式,尤其适用于凝血功能异常或有腹水的危重患者。临床医师应根据明确的适应证并除外禁忌证,在取得患方的知情同意后,方可进行本操作。同时,应注意规范化操作,以预防和减少并发症,并尽可能取得足够的高质量肝组织标本,以提高病理诊断的准确性,从而更好地服务于患者诊疗。




声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
(来源:中华肝脏病杂志)


