


非酒精性脂肪肝病(Nonalcoholic Fatty Liver Disease, NAFLD)是代谢综合征的一种典型形式,全球超过25%的人口受到影响。NAFLD包括从单纯的肝脂肪变性(Simple Steatosis,SS)到不同程度纤维化伴随炎症细胞浸润的非酒精性脂肪性肝炎(Nonalcoholic Steatohepatitis,NASH)在内的广泛组织学变化。如果不加以有效干预,一些NAFLD患者将进一步发展为不可逆的肝硬化、肝细胞癌,最终导致肝衰竭。目前治疗NAFLD的主要方法仍然是以生活方式的改变为主,尽管有一些药物正处于II或III期临床试验当中,但目前尚没有用于专门治疗NAFLD的有效干预方案。
酒精性肝病(Alcoholic Liver Disease,ALD)与NAFLD有许多共同的病理特征,包括脂滴积累、广泛的免疫浸润和肝细胞膨胀。事实上,除了长期过量饮酒外,ALD的诊断标准与NAFLD相似。ALD作为最常见的酒精使用障碍性疾病(Alcohol Use Disorder,AUD),占肝硬化和肝细胞癌等慢性肝病死亡人数的四分之一以上,且超过30%的肝功能衰竭患者与ALD有关。尽管戒酒被认为是ALD的最佳治疗策略,但对于晚期或不可逆肝损伤患者的干预治疗在过去几十年中尚无进展,这表明我们对ALD发病机制的理解存在重大差距。
基于此,南京大学医学院附属鼓楼医院病理科樊智文博士、感染性疾病科李婕教授、消化内科邹晓平教授,联合中国药科大学药学院徐涌教授和李子龙教授,在JHEP Reports(中科院一区,IF:8.3)和EMBO Molecular Medicine(中科院一区,IF:11.1)对以上两大类肝脏疾病的发生发展机制进行了深入研究,希望寻找参与疾病进展的关键分子以用于药物靶向干预。
ALD的潜在干预靶点:Brg1-CXCL14轴
在肝硬化和肝癌患者中酒精性脂肪肝(ALD)病患者占据了很大一部分,在之前的研究中发现,小鼠肝细胞限制性Brg1缺失与一系列肝脏病变的改善有关,因此,在该研究中作者进一步对Brg1在ALD发生发展中的具体作用机制进行了探究[1]。

首先作者构建了多种ALD模型来确定Brg1的响应情况,通过WB、qPCR以及HE发现Brg1在肝脏中表达增高,同样,在ALD患者的肝脏标本中也发现Brg1升高的情况。为了解肝脏中Brg1在ALD期间发挥的作用,作者通过构建肝脏特异性缺失(Brg1LKO)和过表达Brg1(Brg1LKI)小鼠,测定肝脏相关指标发现敲除Brg1后缓解了ALD的症状并且相关的炎症指标,如IL-1β,TNF-α等表达都得到了显著下调。
接着,作者进一步探究了Brg1是否调节ALD进程中免疫细胞的浸润情况。通过流式分析发现Brg1缺乏会导致Ly6G+中性粒细胞的浸润减少,体外实验也证实了肝脏中Brg1的减少会影响中性粒细胞的迁移(图1)。

图1. Brg1在ALD模型中表达增加
为了解影响中性粒细胞迁移的分子机制,作者对WT和Brg1LKO小鼠在模拟ALD条件下进行了测序,发现趋化因子CXCL14在Brg1缺失后表达显著下调。因此,作者研究了Brg1是如何调节CXCL14来影响中性粒细胞的浸润,通过测定CXCL14启动子的转录活性以及通过ChIP实验发现在酒精处理条件下,Brg1将招募至CXCL14启动子区域,增强CXCL14的转录活性。
当注射外源或者沉默内源的CXCL14则会加重或缓解ALD的进程;同样,在患者肝脏样本中发现Brg1与CXCL14、中性粒细浸润存在相关性,以上结果均表明Brg1-CXCL14轴在ALD进程中发挥重要作用。最后,当作者给予ALD小鼠Brg1抑制剂(PFI-3)或者CXCL14受体的拮抗剂(AMD3100)来治疗,结果发现该两种药物均能缓解ALD的症状并抑制中性粒细胞的迁移,该研究为ALD的治疗提供了新的靶点(图2)。
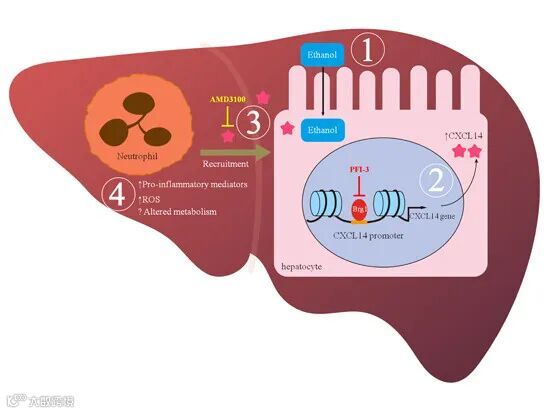
图2. Brg1影响ALD的机制图
NAFLD潜在治疗靶点:趋化因子CCL11
除了ALD外,因饮食和生活方式的改变,非酒精性脂肪性肝病(NAFLD)已成为世界范围内肝硬化和肝细胞癌的最重要原因。NAFLD的特征是肝内脂质沉积加速、异常炎症和大量细胞外基质积聚。CCL趋化因子在维持和破坏肝脏稳态中发挥重要作用。几种不同的CCL蛋白对NAFLD发病机制的贡献已被证实,在本研究中,CCL11也被称作Eotaxin,最初发现作为嗜酸性粒细胞的诱导剂,在各种肝病患者中增加,该研究探究了CCL11在NAFLD发生发展中的作用机制[2]。

首先构建NAFLD小鼠模型,结果发现CCL11在肝细胞中表达增加最为显著,接着,分离原代肝细胞后给予NAFLD刺激因子棕榈酸(PA)后发现CCL11的上调主要是由于NF-κB介导。接下来,作者探究了CCL11在NAFLD进程中的具体作用,结果发现在CCL11 KO小鼠中给予PA后,促炎因子和促进脂肪生成因子表达显著降低,并且在NAFLD模型中,CCL11 KO小鼠肝损伤减少,血清甘油三脂和胆固醇含量降低、胰岛素敏感性增强,这些结果表明CCL11促进了NAFLD的进程(图3)。

图3. CCL11在NAFLD模型中表达增加
接下来作者探究了CCL11如何影响NAFLD进展。通过RNA测序以及富集分析发现,在CCL11处理后,下游分子干扰素调节因子IRF1的出现高表达。体内外实验均证明CCL11可调节IRF1表达并且ChIP实验证明了CCL11刺激后NF-κB可与IRF1启动子结合并增加IRF1转录活性。CCL11通常与CCR3结合发挥功能,因此,作者给予NAFLD小鼠CCR3的阻断剂SB297006,结果发现NAFLD小鼠的症状缓解,肝损伤减少。
为进一步说明CCL11发挥的作用,作者同样使用了CCL11的抗体来进行治疗,结果同样发现CCL11抗体治疗提高了NAFLD小鼠的胰岛素敏感性,并减轻了脂肪变性损伤,这些结果表明CCL11在NAFLD小鼠中主要通过肝细胞炎症,脂质生成和纤维化发挥作用。最后,在临床NAFLD患者的肝组织标本中同样发现CCL11表达增加。
以上研究发现了CCL11在NAFLD发病机制中的调节作用,为NAFLD的干预提供了新的见解和转化潜力(图4)。

图4. CCL11影响NFALD的机制图
NAFLD潜在干预靶点:锌指转录因子Egf1
在NAFLD疾病进展过程中,转录重编程被认为是NAFLD相关病理的关键。例如,与健康个体相比,NAFLD患者肝脏中脂肪酸转运蛋白,包括脂肪酸转运蛋白FATP家族成员和CD36的表达水平升高,因此,当靶向某些转录因子将有助于NAFLD发病过程中肝脏转录组的改变。Egr1(Early Growth Response 1)是一种锌指转录因子,在多种病理生理过程中发挥作用,包括宿主防御反应、癌变和器官纤维化。之前的研究报道Erg1可介导ALD的发生,该研究探索了Erg1在NAFLD中发挥的作用[3]。

作者首先构建了四种不同的NAFLD模型,Erg1在这四种模型中表达均增加,同样在NAFLD患者的肝组织标本中检测到Erg1表达显著增加。为探究介导Erg1高表达的原因,作者构建了Erg1报告基因启动子,通过荧光酶素报告基因实验以及ChIP实验发现,棕榈酸(PA)刺激后可显著增加SRF的核定位和Egr1的结合能力;当干扰SRF后,Egr1对果糖的响应减弱,这些结果表明SRF可以介导Egr1在肝细胞中的转录(图5)。

图5. Egr1在NAFLD模型中表达增加
接下来通过给db/db小鼠尾静脉注射shEgr1以观察Erg1发挥的作用,结果发现Erg1敲除后肝脏脂质累积,免疫细胞浸润以及细胞外基质沉积均减少,表明Erg1参与了促炎和促纤维化的过程。为探究Erg1是如何影响这些过程的,作者通过RNA测序并进行富集分析,发现Egr1可通过调节转录因子NF-κB来影响炎症相关因子表达,同时,调节PPARα来影响脂质代谢相关酶的活性。
因此,作者接下来探究Erg1是如何影响PPARα的表达,通过Co-IP和ChIP实验,作者发现Egr1和PPARα在小鼠肝脏中相互作用,不仅如此,Egr1与PPARα也存在相互作用,通过敲除Egr1发现FAO表达上调,Egr1可以与Nab1相互作用抑制FAO的转录水平。
接下来,作者探究了Egr1是如何抑制FAO的转录水平,通过ChIP实验发现,Egr1缺失显著增强了FAO基因启动子上组蛋白H3K9、H3K18和H3K27的乙酰化水平,这些结果表明,Erg1可能通过Nab1向FAO启动子募集组蛋白去乙酰化酶(HDAC)来抑制FAO转录。
该研究描述了一种新的机制,即早期生长反应1(Egr1)通过调节脂肪酸代谢参与NAFLD的发病进程,从而为NAFLD干预提供了新的见解和转化可能(图6)。

图6. Egr1影响NFALD的机制图
参考文献:
[1] Li N, Liu H, Xue Y, et al. Targetable Brg1-CXCL14 axis contributes to alcoholic liver injury by driving neutrophil trafficking. EMBO Mol Med. 2023;15(3):e16592.
[2] Fan Z, Sun X, Chen X, et al. C-C motif chemokine CCL11 is a novel regulator and a potential therapeutic target in non-alcoholic fatty liver disease. JHEP Rep. 2023 May 26;5(9):100805.
[3] Guo Y, Miao X, Sun X, et al. Zinc finger transcription factor Egf1 promotes non-alcoholic fatty liver disease. JHEP Rep. 2023;5(6):100724.

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
(来源:《国际肝病》编辑部)


