

编者按:随着生活条件改善,肥胖已成为我国严重的公共卫生问题。面对数量日益攀升的超重和肥胖人群,临床用药需求远未得到满足,相关药物研发开展得如火如荼。近期,本刊邀请北京医院·国家老年医学中心、中国医学科学院老年医学研究院潘琦教授和中国医学科学院、北京协和医学院研究生院费思佳博士从中国肥胖严峻现状出发,分享了减重药物的研究进展。
肥胖
——日益严重的公共卫生问题
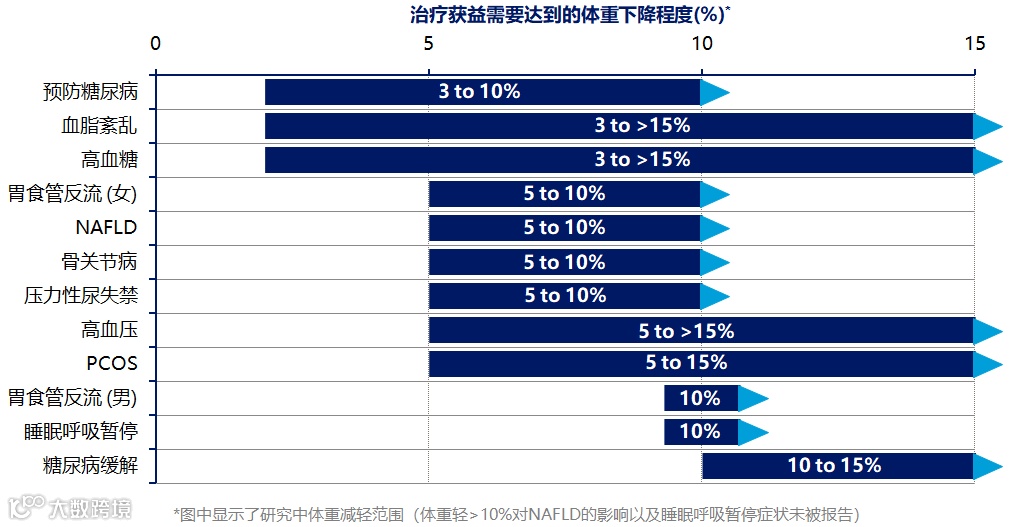
图1. 适当减重可改善肥胖相关疾病

减重方法
——肥胖是一种需要终生治疗和随访的慢性病,下一代减重药物需安全实现大幅度和持续减重
2016 AACE肥胖指南[1]建议安全减重≥10%~20%以预防和改善肥胖相关并发症。一项系统性回顾分析[2]纳入8项采用生活方式管理的减重前瞻性研究,在干预期间达到减重5%,干预完成后至少随访3年。结果显示,成人肥胖患者单纯生活方式管理无法长期维持体重减轻。这可能是由于减重后出现激素水平(饱腹感激素↓、饥饿感激素↑)和代谢水平(静息能量消耗↓)的适应性改变,限制了体重减轻,进而导致体重回升所致[3,4]。代谢手术是目前最有效的减重方法,但其为有创治疗且需长期随访。辅助药物治疗提供了介于生活方式管理和代谢手术之间的减重治疗方案(图2),达到代谢手术减重效果是减重药物的研发愿景。

图2. 辅助药物治疗提供了介于生活方式管理和代谢手术之间的减重治疗方案

机遇与挑战
——对体重调节机制的不断深入了解推动了减重药物研发进程,但也需克服种种障碍
大脑通过稳态途径和享乐途径两个互补驱动力调节食物摄入[3,5,6]。在稳态进食途径,通过胰高血糖素样肽-1(GLP-1)、胰高血糖素(GCG)、肽YY(PYY)、胃泌酸调节肽(OXM)、胰多肽(PP)、缩胆囊素(CCK)、瘦素、胰淀素等增加饱腹感,通过饥饿素增加饥饿感。在享乐进食途径,“想吃”即进食的动力,由多巴胺调控;“喜欢吃”即进食带来的愉悦感,由阿片和大麻素调控。
神经内分泌系统在调节食欲和能量代谢平衡中发挥重要作用(图3)[3]。阿片黑皮质素系统是调节稳态进食的总开关[5]。享乐进食主要核团位于伏隔核、腹侧苍白球和脑干臂旁核,通过阿片类、大麻素、多巴胺、食欲素、γ-氨基丁酸(GABA)神经化学信号形成皮层下网络;饥饿信号可能会增强伏隔核内的内源性阿片类信号,从而放大对美味食物的享乐进食;肥胖个体享乐进食系统对高能食物的反应增强,导致异常的高能食物进食冲动[6,7]。除调节能量摄入,神经内分泌系统还介导能量消耗的调节[8]。

图3. 神经内分泌系统在调节食欲和能量代谢平衡中发挥重要作用
对食欲平衡调节机制的理解为减重药物研发提供了潜在靶点,推动了药物研发进程。但是,从临床前模型到临床研究、从潜在靶点到减重药物的实现还面临如下诸多挑战[9]。
01
肥胖人群异质性
个体对药物治疗的反应需要更深入的代谢和遗传特征分析。在遗传方面,肥胖罕见单基因病因,更常见多基因病因,相关危险基因几乎存在于每条染色体上。在表观遗传方面,表观遗传过程可能是导致肥胖的其他因素。在环境风险因素方面,肥胖与神经行为、内分泌和代谢原因有关。
02
神经内分泌因素
外周内分泌因子和中枢的食欲控制系统成为持续减重的主要障碍,还需权衡营养不良和体重增加之间的平衡。减重时,外周脂肪信号(瘦素、胰岛素)减少。长期禁食导致下丘脑和后脑中促食欲神经肽的表达和敏感性增强,抑食欲神经肽的表达和敏感性降低。室旁核神经元的激活增加导致神经肽Y/刺鼠相关肽(NPY/AgRP)神经元纤维密度和强度增加。肥胖所致脂肪信号(瘦素、胰岛素)持续高水平导致胰岛素敏感性减退,食欲平衡系统反应性受损。
03
药理学转化
动物模型不能完全预测靶点药物在人体中的治疗反应。减重靶点药物在啮齿动物中的药效学与人体中不尽相同。此外,抑制食欲摄入药物对啮齿动物的减重具有更大影响。
04
安全性
肥胖的药物治疗历史漫长而曲折,上世纪多种药物如甲基苯丙胺(安非他明)、去甲麻黄碱等因安全问题退出市场。超重/肥胖患者心血管疾病风险很高,因此对心血管安全性的评估已成为减重药物越来越重要的医学和监管考虑因素。2012年,美国FDA内分泌和代谢药物咨询委员会召开会议,指出新型减重药物的获批需考虑心血管安全性要求[10]。目前,在没有长期安全性数据的情况下,进入市场的任何新药的使用应限于与关键试验中研究患者相似的患者。
既往获批可用的减重药物如纳曲酮/安非他酮、芬特明/托吡酯、芬特明、奥利司他不能明确心血管安全性或存在潜在风险。在LEADER研究中,1.8 mg利拉鲁肽可降低T2DM患者的心血管事件风险,被监管机构作为证据支持3.0 mg利拉鲁肽的心血管安全性[11](注:利拉鲁肽在中国无减重适应证)。正在进行的3b期心血管结局试验SELECT是一项事件驱动、估计为期59个月的多国、随机、双盲、平行组、安慰剂对照试验,将评估司美格鲁肽2.4 mg与安慰剂相比,在标准治疗基础上,对17 500例患有心血管疾病的超重或肥胖且无糖尿病的参与者的心血管结局的影响,研究预计于2023年9月完成[12](注:司美格鲁肽2.4 mg尚未在中国上市)。

新靶点,新未来
——食欲稳态分子机制提供了减重治疗新靶点,未来减重药物可能达到与代谢手术相当的疗效
01
胰淀素
一项随机、双盲、安慰剂对照、2期临床研究[13]纳入706例年龄≥18岁的超重/肥胖受试者,BMI≥30.0 kg/m2或BMI≥27.0 kg/m2合并肥胖相关并发症,HbA1c<6.5%,随机接受安慰剂、不同剂量人胰淀素类似物Cagrilintide OW、利拉鲁肽3.0 mg治疗。主要观察终点是26周时体重较基线的变化。结果表明,Cagrilintide不仅降低血糖,且最大减重幅度>10%。
02
肠促胰素
基于GLP-1的减重药物研发源于其多方面的作用机制(图4)[9],是目前最有前景的热点方向。多种基于肠促胰素的单受体/多受体激动剂进入研发阶段(表1)[9,14,15]。
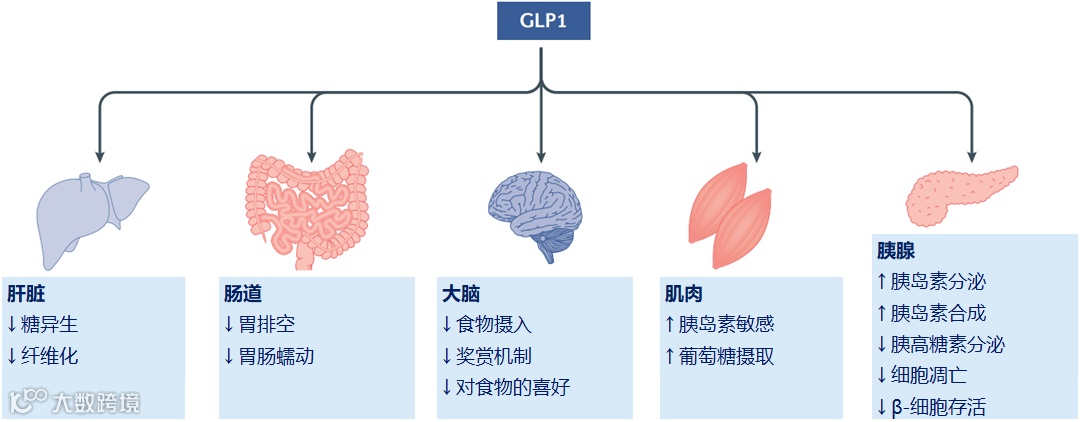
图4. 基于GLP-1的减重药物研发源于其多方面的作用机制
表1. 多种基于肠促胰素的单受体/多受体激动剂进入研发阶段

目前,基于相关研究证据[16-20],利拉鲁肽3.0 mg成为首个获批用于治疗肥胖的GLP-1受体激动剂(注:利拉鲁肽在中国无减重适应证)。在STEP系列研究[21-24]中,司美格鲁肽2.4 mg的体重降幅最高达18%(注:司美格鲁肽2.4 mg尚未在中国上市)。除司美格鲁肽2.4 mg外,目前FDA获批减重药治疗至少12个月后,安慰剂校正后平均体重降幅为2.9%~6.8%[25]。GLP-1/胰淀素复合制剂CagriSema最大体重降幅达17.1%[26]。司美格鲁肽片剂正在进行减重疗效及安全性的临床研究——东亚3a期OASIS 2研究(注:司美格鲁肽片剂尚未在中国上市),GLP-1/GIP双受体激动剂Tirzepatide也正在进行肥胖治疗临床研究。
03
瘦素
补充瘦素对先天性瘦素缺乏症患者有效,但对常见的多基因肥胖患者给予外源性瘦素治疗,则疗效甚微[5]。临床研究显示,瘦素与普兰林肽联合使用体重下降显著优于二者单独使用[27]。对饮食诱导的肥胖小鼠,瘦素与exendin 4、FGF21、GLP-1/GCG联合使用时,瘦素反应性得到改善[28,29]。第一代MC4R激动剂减重疗效有限,且伴有血压和心率升高不良反应。Setmelanotide是第一个针对基因缺陷进行个体化治疗的减重药物,可选择性激活黑皮质素4受体(MC4R)及MC3R、MC1R,无明显心血管不良反应[30,31]。FDA于2020年11月批准Setmelanotide用于治疗遗传性阿片黑皮素原(POMC)、前蛋白转化酶枯草杆菌素/kexin 1型(PCSK1)或瘦素受体缺陷所致肥胖。其主要不良反应包括注射部位反应、皮肤和毛发色素沉着,以及恶心、呕吐和腹泻。
04
其他
其他潜在减重治疗靶点药物尚需进一步研究以探索其在人体中的作用(表2)。此外,潘琦教授团队研究观察了FGF21-GLP-1融合蛋白对糖尿病小鼠糖脂代谢的影响[32]。对Fc-FGF21融合蛋白进行突变改造,可增强该蛋白和受体间的互作关系及稳定性。GLP-1和FGF21双靶点融合蛋白比单靶点类似物具有更好的血糖和体重控制效果。在脂肪肝改善方面,双靶蛋白可降低ALT水平70%以上,显著改善肝脏损伤状态,降低肝总甘油三酯和肝总胆固醇水平,将NAS评分降低3分以上,效果显著优于Fc-FGF21-H和Dulaglutide单靶点类似物。另外,双靶向纳米颗粒的透皮光热-药物疗法也处于研发之中。
表2. 其他潜在减重治疗靶点药物机制及前景


总结
中国不同年龄段、性别和地域的超重和肥胖患病率均显著增加。肥胖是一种多因素相互作用的慢性疾病,更大幅度的安全减重能带来更大获益。单纯生活方式干预减重疗效有限且不持久,代谢手术不能满足全部医疗需求,达到代谢手术减重疗效是减重药物的研发愿景。对体重调节机制的认识加深,推动了减重药物的研发进程,但药物研发仍面临种种挑战。目前,减重药物研发聚焦在基于肠促胰素的单受体和多受体激动剂,胰淀素、瘦素、PYY3-36类似物、GDF15、线粒体解偶联剂等治疗靶点也正在进行临床或临床前研究。

作者简介

费思佳 博士
中国医学科学院 北京协和医学院研究生院


潘琦 教授
主任医师,博士研究生导师,北京医院内分泌科副主任,北京医院全科医师培训基地副主任
中华医学会糖尿病学分会糖尿病监测与治疗技术学组副组长,中华医学会糖尿病学分会基层管理学组副组长,中国老年保健研究会老年骨质疏松分会秘书长,中华医学会老年医学分会内分泌学组副组长,北京医学会糖尿病分会常委兼秘书
主持国家省部级课题6项,参与多项国家重大攻关课题、国家自然科学基金、卫生部行业基金等项目,国内外核心期刊发表论文100余篇,担任《Diabetes Care中文版》《中华老年医学杂志》《中国糖尿病杂志》《中国心血管病杂志》《北京医学》编委

参考文献
1. Mechanick JI, et al. Endocr Pract. 2017; 23(3): 372-378.
2. Nordmo M, et al. Obes Rev. 2020; 21(1): e12949.
3. Theilade S, et al. Diabetes Obes Metab. 2021; 23 Suppl 1: 17-35.
4. Sumithran P, et al. N Engl J Med. 2011; 365(17): 1597-1604.
5. Andermann ML, et al. Neuron. 2017; 95(4): 757-778.
6. Lutter M, Nestler EJ. J Nutr. 2009; 139(3): 629-632.
7. Berridge KC, et al. Brain Res. 2010; 1350: 43-64.
8. Liu J, et al. Acta Pharm Sin B. 2019; 9(2): 220-236.
9. Müller TD, et al. Nat Rev Drug Discov. 2022; 21(3): 201-223.
10. Hiatt WR, et al. JAMA. 2012; 308(11): 1099-1100.
11. Wilding JPH, Jacob S. Obes Rev. 2021; 22(1): e13112.
12. Semaglutide Effects on Heart Disease and Stroke in Patients with Overweight or Obesity - Full Text View - ClinicalTrials.gov
13. Lau DCW, et al. Lancet. 2021; 398(10317): 2160-2172.
14. Neary NM, et al. Endocrinology. 2005; 146(12): 5120-5127.
15. Trevaskis JL, et al. Diabetes Obes Metab. 2015; 17(1): 61-73.
16. Pi-Sunyer X, et al. N Engl J Med. 2015; 373(1): 11-22.
17. le Roux CW, et al. Lancet. 2017; 389(10077): 1399-1409.
18. Davies MJ, et al. JAMA. 2015; 314(7): 687-699.
19. Wadden TA, et al. Obesity (Silver Spring). 2020; 28(3): 529-536.
20. Wadden TA, et al. Int J Obes (Lond). 2013; 37(11): 1443-1451.
21. Wilding JPH, et al. N Engl J Med. 2021; 384(11): 989-1002.
22. Davies M, et al. Lancet. 2021; 397(10278): 971-984.
23. Wadden TA, et al. JAMA. 2021; 325(14): 1403-1413.
24. Rubino D, et al. JAMA. 2021; 325(14): 1414-1425.
25. Tak YJ, Lee SY. World J Mens Health. 2021; 39(2): 208-221.
26. Enebo LB, et al. Lancet. 2021; 397(10286): 1736-1748.
27. Ravussin E, et al. Obesity (Silver Spring). 2009; 17(9): 1736-1743.
28. Müller TD, et al. J Pept Sci. 2012; 18(6): 383-393.
29. Clemmensen C, et al. Diabetes. 2014; 63(4): 1422-1427.
30. Sharma S, et al. Molecules. 2019; 24(10): 1892.
31. Clément K, et al. Nat Med. 2018; 24(5): 551-555.
32. Pan Q, et al. EBioMedicine. 2021; 63: 103202.

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
(来源:《国际糖尿病》编辑部)




