
编者按
在2025年亚太肝脏研究学会年会(APASL 2025)上,广西医科大学附属肿瘤医院钟鉴宏副教授团队展示了肝细胞癌(HCC)新辅助治疗、HCC术后辅助治疗、中晚期HCC免疫再挑战等领域的研究成果。其中,4项研究入选大会口头报告,8项为壁报交流,为HCC的临床诊疗实践提供了宝贵的科学依据和思路。


口头报告

研究一
三级淋巴结构对HCC术后辅助PD-1抑制剂疗效的影响
第一作者:苏家勇;通讯作者:钟鉴宏

研究背景
HCC术后辅助免疫治疗的最佳获益人群仍不清楚。三级淋巴结构(TLS)可能促进对HCC的适应性和体液免疫反应,从而增强免疫检查点抑制剂治疗的疗效。然而TLS是否与根治性肝切除术后接受辅助PD-1抑制剂的患者预后较好有关尚不清楚。
研究方法
该研究纳入TCGA队列304例HCC患者,广西队列312例HCC患者,195例HCC术后接受了辅助PD-1抑制剂治疗的患者。研究分析了肿瘤中TLS的存在率和成熟度,TLS与切除后辅助PD-1抑制剂治疗疗效的关系,以及TLS与免疫细胞浸润程度和特征的关系。同时通过肝癌动物模型进行了验证。
研究结果
TLS的存在与HCC患者预后较好显著相关。在使用辅助治疗的患者中TLS表达患者的无复发生存率和总生存率明显优于TLS不表达的患者。纳入TLS的复发预测模型对使用辅助治疗的患者HCC术后复发具有良好的预测作用。同时,具有TLS的肿瘤中CD3+ CD8+ PD-1+ T细胞、PD-1+自然杀伤T细胞、B细胞和granzyme B+细胞的水平都显著高于无TLS的肿瘤,而调节性T细胞和巨噬细胞的水平显著低于无TLS的肿瘤。在小鼠HCC模型中也观察到类似的结果。
研究结论
这些现象可能反映了TLS与辅助PD-1抑制剂治疗之间的协同作用。未来进一步明确存在瘤内TLS的患者是否是辅助PD-1抑制剂治疗的最佳获益人群具有十分重要的价值。


研究二
研究背景
近年来,在国内外的乙型肝炎防治指南中,推荐扩大抗病毒治疗适应证的呼声越来越大。以往关于抗病毒疗效的证据大多集中于慢性乙型肝炎患者,而缺乏基于乙型肝炎相关肝细胞癌(hepatitis B-related hepatocellular carcinoma,HBV-HCC)患者的临床证据。这一项回顾性研究旨在阐明不同核苷类似物(Nucleoside analogues,NAs)治疗持续时间对HBV-HCC患者肝纤维化的影响,为扩大慢性乙型肝炎抗病毒治疗适应证提供理论依据。
研究方法
对131例在广西医科大学附属肿瘤医院接受两次肝切除术并规范使用NAs治疗的HBV-HCC患者开展回顾性研究(2015年7月-2024年3月),并通过接受两次肝切除术的不同时间间隔分为三组:少于12个月治疗组,12至24个月治疗组和超过24个月治疗组。采用Ishak、Scheuer评分系统评估两次肝切除术后肝脏病理样本的纤维化程度。
研究结果
接受NAs治疗后,不同治疗时间段的HBV-HCC患者肝纤维化程度都获得了缓解(Ishak评分减少≥1分),其中治疗时间为12到24个月的HBV-HCC患者获得肝纤维化缓解的比例更高。12到24个月治疗组获得肝纤维化缓解的患者比例高于超过24个月治疗组(52.5% vs 28.0%,P=0.019),稍高于少于12个月治疗组(52.5% vs 44.1%,P=0.494)。Scheuer评分也表现出了相似的结果。


研究三
免疫检查点抑制剂在不可切除的肝细胞癌中的有效性和安全性:一项回顾性、多中心队列研究
第一作者:陈景坤;通讯作者:钟鉴宏

研究背景
免疫检查点抑制剂(ICI)是不可切除肝细胞癌(HCC)的标准治疗药物之一。在ICI的应用中存在许多挑战,如原发性和继发性耐药、免疫相关不良事件(irAE)等。这项大样本回顾性临床研究旨在探讨不可切除HCC患者在ICI耐药或irAE后ICI再挑战的疗效和安全性,并探索最佳获益人群。
研究方法
通过回顾性分析了近3000例接受ICI治疗的不可切除HCC病例,最终纳入272例接受了ICI再挑战且随访资料比较完整的病例。
研究结果
接受ICI再挑战患者的中位总生存时间为28.0个月。ICI初治(ICI-1)的中位无进展生存(mPFS)为5.3个月,ICI再挑战(ICI-2)的mPFS为4.4个月。基于肝内病灶、肝外病灶、PD-1抑制剂、ICI耐药等亚组分析结果均显示,与ICI-1相比,ICI-2与较低的ORR和较短的mPFS相关。在初始ICI治疗期间出现原发性耐药的患者,ICI再挑战的ORR最低,mPFS最短。安全性分析方面未观察到新的安全性信号。


研究四
新辅助TACE联合ICI和TKI对比直接肝切除术治疗初治可切除中晚期HCC的疗效与安全性比较:一项多中心回顾性研究
第一作者:杨大龙;通讯作者:钟鉴宏
研究背景
肝细胞癌(HCC)确诊时约70%已处于中晚期,部分患者虽可行肝切除术,但术后复发率高。传统新辅助治疗(如单纯TACE)未能显著改善预后,而今年公布的LEAP-012和EMERALD-1研究提示,在不可切除HCC中,TACE联合免疫检查点抑制剂及酪氨酸激酶抑制剂(三联疗法)可能提升疗效,但其在中晚期可切除HCC患者中的安全性及有效性尚未明确。本研究旨在评估新辅助三联疗法的生存获益与风险。
研究方法
多中心回顾性研究,纳入中国广西20家医院2019-2023年接受新辅助三联疗法(TACE+免疫+靶向,n=205)或直接肝切除术(n=378)的中晚期可切除HCC患者。比较两组总生存期(OS)、无事件生存期(EFS)、病理反应率及安全性,采用倾向评分匹配(PSM)减少基线差异影响。
研究结果
在整体人群中,在倾向评分匹配前后,新辅助三联治疗均可显著改善OS和EFS。在接受肝切除术的病例中,新辅助三联治疗序贯肝切除术的OS和EFS显著优于直接行肝切除术。基于mRECIST评估,新辅助三联治疗的ORR为67.3%,DCR为84.9%。新辅助组35.2%患者发生3-4级不良事件,16例患者因肿瘤进展失去手术机会。
研究结论
新辅助三联疗法(TACE+免疫+靶向)可显著提升中晚期可切除HCC患者的总生存期和无事件生存期,并诱导高病理缓解率,但其伴随较高的严重不良事件和术后并发症风险。临床决策需权衡生存获益与安全性,建议在经验丰富的多学科团队指导下个体化应用。未来需前瞻性研究进一步验证其长期疗效。
壁报交流

研究一

研究背景
肝细胞癌(HCC)多数确诊时已不可切除,转化治疗可使部分患者获得缓解并转为可切除状态。然而,转化治疗后是否应进行肝切除术以改善预后仍存争议。本研究旨在比较肝切除术与继续局部/全身治疗或主动监测对缓解患者的生存影响,并评估完全缓解(CR)与部分缓解(PR)的预后差异。
研究方法
多中心回顾性研究,纳入中国广西20家医院2019-2023年转化治疗后获得CR/PR的初始不可切除HCC患者565例。分为手术组:300例接受肝切除术,和非手术组:265例(215例继续局部/全身治疗,50例主动监测)。比较两组总生存期(OS)、无事件生存期(EFS)、无复发生存期(RFS)及病理缓解率,采用倾向评分匹配减少基线差异影响。
研究结果
手术组3年OS率显著高于非手术组(79.9% vs. 58.5%,P<0.001),但EFS无显著差异(中位40.6 vs. 33.4个月,P=0.403)。CR患者术后OS(HR=0.40)和EFS(HR=0.45)均优于PR患者;完全病理缓解(pCR)患者OS(HR=0.34)和RFS(HR=0.38)显著改善。非手术组中,继续局部/全身治疗患者OS(HR=0.51)和EFS(HR=0.47)优于主动监测。此外,在转化治疗后疾病稳定(SD)并且符合可切除HCC标准的病例中,行肝切除术的OS和EFS显著优于非手术组。38.7%手术患者达到pCR,显著关联长期生存。手术组术后并发症发生率较高(48.0%),但围手术期死亡率低(0.3%)。
研究结论
肝切除术可显著提升转化治疗后CR/PR患者的总生存期,但需权衡术后并发症风险。CR和pCR是预后良好的关键指标。对于未选择行手术的患者,继续局部/全身治疗优于主动监测。临床决策应基于多学科评估,结合患者个体特征及肿瘤生物学行为,未来需前瞻性研究验证长期疗效。


研究二
在不可切除肝细胞癌转化治疗中,无进展生存期可作为总生存期的潜在替代预后指标
第一作者:杨大龙;通讯作者:钟鉴宏
研究背景
肝细胞癌(HCC)确诊时约70%已不可切除,转化治疗可缩小肿瘤以提高手术机会。总生存期(OS)是评估疗效的金标准,但其需长期随访和大样本量,限制了临床应用。无进展生存期(PFS)作为替代终点可缩短研究周期,但此前缺乏真实世界数据验证其与OS的关联。本研究旨在探讨不可切除HCC患者接受转化治疗后,PFS能否作为OS的可靠替代终点,并分析不同治疗方案及肿瘤反应对PFS的影响。
研究方法
多中心回顾性研究,纳入中国广西20家医院2019-2023年接受转化治疗的不可切除HCC患者1909例。使用秩相关方法结合迭代多重插补(处理数据截尾),分析PFS与OS的相关性;亚组分析不同治疗方案(介入+全身治疗、单独全身治疗、单独介入治疗)及肿瘤反应(完全缓解CR、部分缓解PR、疾病稳定SD)对结果的影响。统计方法:Kaplan-Meier生存曲线、Cox回归模型、敏感性分析(随机分组重复1000次以验证相关性稳定性)。
研究结果
整体患者中,PFS与OS呈中等强度相关(Spearman’s ρ=0.74,95%CI:0.72-0.76)。不同治疗方案下相关性一致(介入+全身治疗ρ=0.75,全身治疗ρ=0.73,介入治疗ρ=0.74)。24个月PFS与48个月OS的成对相关性系数为0.74(SD=0.08)。肿瘤反应与PFS:CR患者(HR=0.24)和PR患者(HR=0.23)的PFS显著优于未缓解者(PD/SD),且缓解程度越高,PFS改善越明显。
研究结论
不可切除HCC患者接受转化治疗后,PFS与OS存在中等强度相关性,且不受治疗方案影响,支持PFS作为OS的潜在替代终点。肿瘤缓解程度(CR/PR)是PFS改善的重要预测指标,可指导临床分层管理。研究局限性包括缺乏试验层面验证、治疗方案异质性及术后治疗差异的影响,未来需前瞻性研究进一步确认结果。

研究三

研究背景
我国的肝细胞癌(HCC)指南强推荐对根治性切除后复发风险高的HCC患者进行辅助经肝动脉化疗栓塞(TACE)。然而,现有的一些临床研究可能纳入了较多接受姑息性切除的患者。
研究方法
通过研究设计目标试验模拟框架,采用处理加权逆概率(IPTW)和倾向评分匹配(PSM)减少偏移。定义了根治性切除为术后数字减影血管造影(DSA)中未见肿瘤染色;其余为R1切除。对比两组之间的无复发生存期(RFS)和总生存期(OS)。
研究结果
在最终分析的1390例患者中,433例(31.2%)接受了术后TACE治疗,其余患者接受了积极监测。中位随访时间为35.7个月。接受TACE治疗的患者RFS和OS均显著提高。然而,在接受TACE治疗的患者中,315例(72.7%)切除属于真正根治性,其余的可能属于R1切除。与主动监测相比,真正根治性切除后辅助TACE并无显著提高RFS和OS。PSM和IPTW后得出了相似的结果。
研究结论
辅助TACE可能并不能改善复发风险高的HCC患者的RFS和OS。本研究强调了术后DSA在合并高危复发因素HCC切除术后检测微小残留病灶的价值。

研究四

研究背景
越来越多的证据表明,辅助PD-1抑制剂可能可改善合并高危复发风险肝细胞癌(HCC)患者的预后。然而,尚不清楚不同类型的PD-1抑制剂是否表现出相同的临床疗效。
研究方法
这项研究对来自8个中心接受辅助PD-1抑制剂患者的无复发生存期(RFS)和总生存期(OS)与接受主动监测的患者进行了比较。根据不同类型的PD-1抑制剂进一步进行亚组分析。
研究结果
在最终分析的1534例患者中,378例(24.6%)接受了PD-1抑制剂联合或不联合分子靶向药物治疗。中位随访30.5个月之后,接受PD-1抑制剂辅助治疗的患者的RFS 和OS 显著高于接受主动监测的患者。接受替雷利珠单抗、信迪利单抗、卡瑞利珠单抗、特瑞普利单抗和派安普利单抗治疗的患者相应的中位RFS和OS并无显著差异。
研究结论
辅助PD-1抑制剂可改善合并高复发风险HCC患者的RFS和OS。不同类型PD-1抑制剂的疗效无显著差异。

研究五

研究背景
IMbrave050研究虽然失败,但仍有少部分肝细胞癌(HCC)患者可以从中获益。确定从辅助免疫治疗中获益的最佳人群至关重要。本研究旨在利用接受PD-1抑制剂治疗的HCC患者建立复发预测模型。
研究方法
本研究纳入了389例合并高危复发因素的患者,且根治性术后接受了PD-1抑制剂辅助治疗。这些患者被分为发展队列(中心1)和外部验证队列(中心2-8)。
研究结果
通过多因素COX回归分析发现,男性、肿瘤大、多结节肿瘤、血清甲胎蛋白高、白蛋白-胆红素分级高、微血管侵犯、肿瘤分化差是HCC早期复发的关键参数。本研究构建了术前和术后使用辅助PD-1抑制剂患者复发预测模型。通过ROC曲线、临床影响曲线、决策曲线分析和校准曲线进行验证模型具有良好的预测效能,可以有效地将患者分为两个不同的风险层和预后亚组。
研究结论
这项研究为寻找术后辅助免疫治疗的最佳获益人群开发了有前景的预测模型,但仍需要更多的数据进行验证。

研究六

研究背景
大血管侵犯,特别是门脉主干或下腔静脉癌栓严重限制了患者的长期生存。目前的RCT研究多不纳入癌栓分期晚、预后差的患者,故有必要探索这部分患者的治疗疗效。
研究方法
本研究回顾性分析了2019年至2024年109例合并门脉主干或下腔静脉癌栓HCC患者,其中74例接受放疗联合靶向和免疫治疗,35例接受单一放疗。
研究结果
接受三联治疗的患者有更长的中位总生存时间(18.0 vs 11.0月,P=0.002)和中位无进展生存时间(10.0 vs 7.5月,P<0.001)。三联治疗组的癌栓反应率高于放疗组。癌栓缩退率≥30%患者的中位总生存时间(20.0 vs 10.0月,P<0.001)和中位无进展生存时间(12.0 vs 6.7月,P<0.001)明显长于未达到癌栓缩退率≥30%患者。
研究结论
放疗联合靶向和免疫治疗可能是治疗合并门脉主干或下腔静脉癌栓HCC患者的有效方案。目前样本量仍较小,需要更多大样本的研究进行探索。

研究七
ICIs单药或联合TKIs在存在肝外转移HCC的疗效和安全性:多中心、回顾性研究
第一作者:邓柱鉴;通讯作者:钟鉴宏
研究背景
免疫检查点抑制剂(ICI)和酪氨酸激酶抑制剂(TKIs)是国内外指南推荐的治疗晚期肝细胞癌(HCC)的标准治疗方案。在临床实际中,晚期患者除了接受靶免治疗之外,还会接受TACE、HAIC等局部治疗。因此在评估肝内病灶的时候,无法得知靶免治疗的真实疗效。而肝外病灶几乎不受肝内局部治疗的影响。因此本研究通过肝外病灶了解靶免治疗的真实疗效。
研究方法
本研究纳入了8个中心的240例合并肝外转移的HCC患者,其中178例患者接受ICIs联合TKIs,62例患者接受ICIs单药治疗。
研究结果
联合治疗组和ICIs单一治疗组患者的中位OS无显著差异。相比于ICIs单一治疗,联合治疗显著延长了患者的中位PFS(8.0 vs 5.0个月,P=0.012)。当单独评估EHS时,接受联合治疗的患者也有更长的中位PFS(9.9 vs 5.4个月,P=0.012)和更高的DCR,但两组的ORR无显著差异。
研究结论
HCC患者在接受ICIs联合TKIs或接受单一ICIs治疗后,肝外病灶的PFS和局部控制率与既往文献报道的肝内病灶的结果相似。但仍需要更多大样本的研究进一步探索。

研究八
建立与非酒精性脂肪性肝病的病程及肝纤维化进展相关的转录组特征基因集
第一作者:潘立鑫;通讯作者:钟鉴宏
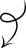
研究背景
肝纤维化是非酒精性脂肪性肝病(NAFLD)患者长期肝损伤的结果,肝纤维化进展与患者的长期预后密切相关。该研究旨在建立一个转录组特征基因集以在分子水平上监测NAFLD相关肝纤维化的进展。
研究方法
本研究基于整合的NAFLD相关批量转录组测序数据,通过联合差异表达基因分析和最小绝对收缩和选择算子回归分析的策略,建立了由11个关键基因组成的基因集。本研究尚且检测了人源肝星状细胞(HSCs)——LX-2细胞中的11个关键基因的表达水平。
研究结果
该研究所建立的基因集能较准确地区分伴有非进展期肝纤维化和进展期肝纤维化的NAFLD患者,由基因集区分的高危组患者尚且具有更高的肝细胞癌发生风险。此外,基因集在批量转录组水平及单细胞转录组水平上可分别提示负责调控肝纤维化进展的HSCs的浸润及活化。基于LX-2细胞建立的体外高脂培养体系能够模拟HSCs在NAFLD患者肝脏的高脂环境中活化的进程。通过检测11个关键基因的表达水平,发现IL6在具有脂质累积的活化LX-2细胞中表达上调。
研究结论
由11个关键基因组成的基因集有助于识别NAFLD患者的肝纤维化分期及NAFLD的病程进展。在NAFLD的背景下,IL6在肝星状细胞活化中的作用值得进一步探究。


会场花絮





专家简介

往期推荐
APASL名家访谈丨侯金林教授:中国以卓越之力推动乙型肝炎母婴传播消除事业
APASL前沿情报丨打破边界 多元共治——构建肝脏健康新社区
APASL 2025丨杨松教授团队:酒精性肝病不良结局预测及相关致癌机制
APASL 2025丨天津大学中心医院梁静教授团队在肝病领域收获5项研究成果
(来源:《国际肝病》编辑部)

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。








