脓毒症(sepsis)是指由于微生物或其他病原体侵入而诱发的全身炎症反应综合征(systemic inflammatory response syndrome,SIRS),是创伤、烧伤、休克、感染和大手术等临床急危重症患者的严重并发症之一,进一步发展为严重脓毒症、脓毒症休克、多器官功能障碍综合征,是急危重症患者死亡的主要原因之一。据美国疾病控制中心的统计调查结果显示,美国每年约有20万人死于脓毒症,每年用于治疗脓毒症的医疗费用高达160亿美元。中国虽然缺乏详细的流行病学资料,但据推算,每年仍可有超过300万例患者发生脓毒症。脓毒症一直都是国际医学界的研究热点和重点。2002年,旨在降低脓毒症患者死亡率的"拯救脓毒症战役",呼吁并动员全社会力量,提高对脓毒症发病率、高病死率、早期诊断、早期治疗以及护理重要性的认识。
研究发现,脓毒症的核心机制是炎症反应,SIRS是机体修复和生存而出现应激反应的一种临床过程,然据目前研究,单纯抑制促炎细胞因子如肿瘤坏死因子(tumour necrosis factor,TNF)-α和白介素(interleukin,IL)-1尚不能改善严重脓毒症患者的预后。因此,过度的炎症反应并非造成脓毒症不良后果的基础,基于此,美国学者Bone提出了著名的代偿性抗炎症反应综合征(compensatory anti-inflammatory response syndrome,CARS)假说,提出脓毒症的发生和发展是机体促炎与抗炎机制失衡所致,在脓毒症发生的后续阶段,CARS逐渐占据主导地位,进一步激发免疫抑制以及"炎症的二次打击",决定脓毒症患者的死亡风险。尽管随着对脓毒症发病机制认识的改变,脓毒症与免疫、脓毒症与炎症反应等研究逐渐成为现今脓毒症基础研究的热点。如何实现脓毒症的早期诊断,预测分析其疾病发生发展的阶段,现有评价脓毒症疾病严重程度的指标往往都是等待脓毒症发生发展进而出现器官、系统功能障碍之后而表现出的临床症状,存在较大的滞后性,那么如何评价及预测疾病发展的严重程度同样是困惑临床医师治疗的难题。
Toll样受体(Toll-like receptor,TLR)是炎症信号转导的门户蛋白,介导天然免疫反应的首要受体,可识别大量不同病原体相关分子模式并快速激发机体免疫应答,现有研究发现其与脓毒症的发生发展关系密切。TLR是识别病原体和产生持续性全身炎症瀑布效应的中间环节,通过抑制TLR的功能,可以调控脓毒症发病过程中的促炎反应,缓解脓毒症发病的严重程度。因此,TLR目前被认为是控制脓毒症的一个新的靶点。TLR4是人类发现的第一个Toll样相关蛋白,主要识别革兰阴性细菌表面的脂多糖(lipopolysaccharide,LPS),通过经典MyD88及TRIF信号转导通路,是革兰阴性细菌感染、内毒素血症及由此引起的中毒性休克、SIRS和脓毒症的主要识别受体。
高迁移率族蛋白(high mobility group protein,HMG)是20年代中期发现的一类新的典型的非组蛋白,参与细胞核内诸如转录、复制、重组等多个复杂有序的功能过程。高迁移率族蛋白B1(high mobility group box-1 protein,HMGB1)与TNF-α、IL-1等早期炎症因子相比,HMGB1具有明显的延迟释放的特点,同期及近年来大量研究已经明确在感染性休克,如脓毒症中,HMGB1是一种重要的炎症介质,一方面起到触发炎症的作用,诱导其他炎症因子的产生和释放,导致血管内皮损伤;另一方面亦能被多种早期释放的炎症因子活化而主动释放,形成级联反应,参与多器官损害的病理生理过程,动物实验亦证明HMGB1升高与脓毒症小鼠死亡率增加相关。
因此,本研究通过构建脓毒症大鼠模型,检测不同时间点HMGB1及TLR4的表达变化规律,初步探索脓症大鼠模型不同时间血清HMGB1及TLR4浓度变化关系,为脓毒症炎症机制探索及脓毒症早期识别与诊断提供新思路。
材料与方法
一、实验动物
SD大鼠,清洁级,体重(300±50)g,周龄(8±1)周,雄性。
二、主要仪器及试剂
Rat-HMGB1酶联免疫吸附测定(enzyme-linked immuno sorbent assay,ELISA)试剂盒,Rat-TLR4 ELISA试剂盒(武汉伊莱瑞特生物科技有限公司);TAK-242 TLR4 signaling inhibitor(Glycyrrhizin,美国);HMGB1 inhibitor(Glycyrrhizin,美国)
三、脓毒症大鼠模型制备
术前禁食12 h,自由饮水。称重、编号、按随机数字表进行分组。腹腔注射0.5%戊巴比妥钠(30 mg/kg),待麻醉满意后,将大鼠固定于手术台,常规消毒胸腹部皮肤,在剑突下约2 cm处沿腹正中线剪开腹壁约2 cm,暴露盲肠,结扎其近端,避免结扎供应盲肠的血管,用国产25号针头均匀贯通盲肠2次,造成2个漏口,使2个漏口的距离为1 cm。挤压结扎的盲肠,挤出少量粪便内容物,并放置2条引流条(0.5 cm×2.0 cm)。确认无明显出血后将盲肠还纳腹腔,避免肠管扭转,缝合腹壁切口。术毕,颈后皮肤常规消毒后皮下注射20 ml/kg 0.9%NaCl进行液体复苏,麻醉苏醒后单笼饲养。
四、实验分组
将模型大鼠分为脓毒症大鼠组[盲肠结扎穿孔(cecal ligation and puncture,CLP)组],HMGB1干预组、TLR4干预组,其中HMGB1干预组使用CLP法造模,术后即刻经尾静脉注射HMGB1抑制剂5000 U/kg体重(溶于2.0 ml/kg体重0.9%NaCl中),TLR4干预组使用CLP法造模,术后即刻经尾静脉注射TLR抑制剂1000 U/kg体重(溶于2.0 ml/kg体重0.9%NaCl中);另选择假手术组(麻醉后开腹翻动盲肠后关腹)、空白组(不做任何处理的正常大鼠)作为对照。
五、HMGB1及TLR4表达曲线构建
CLP组、HMGB1干预组、TLR4干预组、假手术组、空白组分别于CLP术后/正常饲养状态下4、12、24、36、48 h采取尾静脉取血法,分别采集静脉血1 ml留存备用。以ELISA法分别检测静脉血清HMGB1、TLR4浓度,构建浓度曲线。
六、统计学分析
采用统计软件SPSS 17.0对实验数据进行分析,计量资料以 ±s表示,组间两两比较采用配对t检验,多组间不接采用单因素方差分析。以P<0.05为差异有统计学意义。
±s表示,组间两两比较采用配对t检验,多组间不接采用单因素方差分析。以P<0.05为差异有统计学意义。
结果
一、HMGB1表达曲线构建
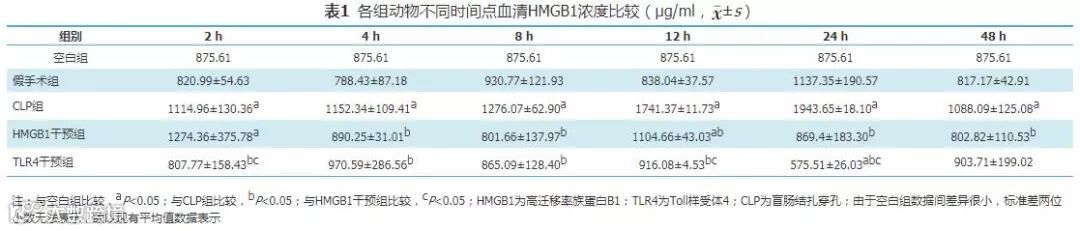
不同时间点实验动物血清HMGB1浓度检测结果表明,假手术组术后8 h较空白组稍有升高,但差异无统计学意义(P>0.05)。与空白组相比,CLP大鼠造模2 h后,血清HMGB1浓度开始升高,至术后48 h达到高峰,后逐渐开始下降(各时间点P<0.05)。术后即刻予以HMGB1干预的HMGB1干预组数据表明,2 h后血清HMGB1浓度较CLP组异常升高,但差异无统计学意义(P>0.05);予以HMGB1干预4 h后,血清HMGB1浓度较CLP组明显下降,HMGB1干预作用一直可持续至术后48 h,且在24 h其抑制作用达到高峰。予以TLR4干预的TLR4干预组,术后2 h开始,其血清HMGB1浓度较CLP亦有明显下降,抑制作用可持续至术后48 h;与HMGB1干预组相比,予以TLR4干预2 h后,血清HMGB1浓度明显低于CLP组及HMGB1干预组;TLR4干预4 h开始至术后24 h,TLR4干预组HMGB1浓度均低于CLP组(各时间点P<0.05),但与HMGB1干预组相比,差异无统计学意义(P>0.05);术后12 h检测数据表明,TLR4干预组血清HMGB1浓度明显低于CLP组及HMGB1干预组(P<0.05),至术后24 hTLR4干预作用达到高峰(图1,表1);术后48 h,TLR4干预组HMGB1浓度较CLP组,HMGB1组相比差异无统计学意义(P>0.05)。

注:HMGB1为高迁移率族蛋白B1;TLR4为Toll样受体4;CLP为盲肠结扎穿孔
图1 各组动物不同时间点血清HMGB1浓度比较
二、TLR4表达曲线构建
不同时间点实验动物血清TLR4浓度检测结果表明,假手术与空白组相比,差异无统计学意义(P>0.05),且几乎数值为零。相比空白组,脓毒症术后大鼠血清TLR4浓度变化呈现双峰状,术后8 h,TLR4浓度第一次达到峰值,随后稍有下降(12 h),至术后24 h,其数值再次达峰(各时间点数值较空白组P<0.05)。CLP术后予以HMGB1干预的HMGB1干预组,各检测时间点TLR4数值均较空白组明显升高(P<0.05);与CLP组相比,HMGB1干预处理8 h后,血清TLR4浓度明显升高,高于CLP组血清TLR4浓度(P<0.05),随后血清TLR4浓度明显降低,甚至低于CLP组血清TLR4浓度(P<0.05)。CLP术后予以TLR4干预的TLR4干预组,各检测时间点血清TLR4浓度均较空白组明显升高(P<0.05);与CLP组相比,予以TLR4干预后,实验动物血清TLR4浓度同样表现出双峰特点,但达峰时间提前(4、12 h,P<0.05),且峰值增加(P<0.05)(图2,表2)。

注:HMGB1为高迁移率族蛋白B1;TLR4为Toll样受体4;CLP为盲肠结扎穿孔
图2 各组动物不同时间点血清TLR4浓度比较

讨论
HMGB1从被发现至今已有30余年的历史,其家族蛋白具有多种生物学功能,包括维持核小体结构、调节基因转录、稳定染色质和参与DNA重组等。近年来研究发现HMGB1是致炎细胞因子网络中的一个中心环节,为临床上治疗脓毒症等炎症疾病提供了治疗时机。HMGB1作为致炎细胞因子在病理状态下分泌,并与其他细胞因子相互作用形成复杂的细胞因子网络。HMGB1在这个网络中与其他致炎细胞因子的具体关系有待深入研究,因为这关系到以HMGB1为靶向的抗炎治疗效果。因此进一步深入研究HMGB1诱导细胞活化的机制及其胞内信号转导通路,这将有助于从全新的视角认识脓毒症的发病本质与临床意义,并为探索其防治方法提供新思路。现有信号转导机制研究证实:HMGB1可与其受体TLR4相互作用,通过激活核转录因子(nuclear transcription factor,NF)-κB,引起下游炎症介质释放,形成多米诺骨牌效应,炎症持续放大,本研究旨在探讨HMGB1、TLR4、NF-kB信号通路在脓毒症中的可能作用,明确其信号通路在脓毒症中作用机制,可能为临床治疗脓毒症新方法提供理论依据。
本课题初步探讨脓毒症大鼠模型造模成功后不同时间点血清HMGB1及TLR4蛋白浓度变化趋势,分析其与脓毒症炎症级联反应诱发-发展-恶化的潜在可能关系。现有研究已经明确HMGB1与脓毒症发生发展以及进展恶化与多脏器功能衰竭综合征有直接密切关系。本研究的检测结果表明,作为一类晚期炎症因子,HMGB1在脓毒症4 h左右开始升高,至24 h达到高峰,较其他基于人类的研究结果提示HMGB1多于48 h达到高峰,其峰值稍有提前,考虑与实验动物本身寿命因素可能相关。通过研究结果表明,CLP脓毒症大鼠模型于术后即刻予以HMGB1抑制剂干扰后,其血清HMGB1浓度较单纯CLP组呈明显下降趋势,同样在HMGB1表达最高峰(24 h)抑制作用最强,这一结果与本课题预期研究结果一致,亦再次证实减少脓毒症后血清HMGB1浓度对于改善脓毒症预后具有积极重要的作用,且对于炎症细胞受刺激后释放晚期炎症因子HMGB1的抑制/干扰,需在HMGB1发挥作用达到高峰之前,通过本研究认为该时间点为严重感染后2~4 h内。为了进一步探索晚期炎症因子HMGB1在炎症级联反应中的作用通路,笔者进一步予以TLR4抑制剂于CLP后即刻干预实验大鼠,随后在不同时间点检测血清HMGB1浓度,初步研究结果表明,TLR4抑制剂干预后,从重症感染后2 h开始,其血清HMGB1浓度即呈下降趋势,并且其对于HMGB1释放的抑制作用于术后12 h起优于予以HMGB1抑制剂,并在24 h达到作用高峰。基于该研究结果,抑制TLR4对于抑制/减少晚期炎症因子HMGB1的释放,其发挥作用更早,作用效果更强,提示在炎症因子释放的信号转导通路中,HMGB1可能通过TLR4信号通路发挥作用。
此外,本研究还关注近年来的研究热点之一TLR4。现有研究表明,抑制TLR可调节脓毒症发生发展过程中的促炎反应。TLR4主要识别革兰阴性细菌表面的LPS,多项关于ICU常见感染病原菌的调查亦明确,革兰阴性细菌仍然是目前绝大多数ICU单位内的常见严重致病菌。因此本研究首先以TLR4为研究靶点,检测CLP模型大鼠不同时间点血清TLR4蛋白浓度。结果表明,CLP大鼠血清TLR4浓度呈现双峰趋势,术后8 h明显升高后稍有下降,再次于术后24 h达到第2次峰值,通过查阅国内相关文献,笔者并未发现相关研究结果,推测认为可能与重症感染后早期炎症因子及晚期炎症因子释放不同时效相关。现有研究亦明确,重症感染后免疫抑制,促炎/抑炎反应不平衡,SIRS,CARS"二重打击"学说,似乎可以从本研究结果血清TLR4浓度二次达峰中得到体现。另发现,分别于CLP术后即刻予以HMGB1干预和TLR4干预,随后检测不同时间点实验动物血清TLR4浓度,其结果亦有明显差异。重症感染予以HMGB1干扰2~8 h内,血清TLR4浓度较空白组明显升高,较单纯CLP组呈上升趋势,至8 h左右血清TLR4浓度达到高峰,远高于单纯CLP组,后其数值明显降低。结合重症感染后血清HMGB1表达变化曲线,TLR4作为HMGB1发挥作用的关键因子之一,一旦予以HMGB1抑制,导致机体内HMGB1蛋白含量减少,因而初期被炎症刺激/调动而释放的TLR4则呈现出高表达趋势,且重症感染后8 h左右亦不是HMGB1表达高峰,因而体内HMGB1本身含量偏少加之予以HMGB1抑制,因此HMGB1蛋白含量低,而当重症感染12 h后,即使予以HMGB1抑制,机体体内仍有较高HMGB1蛋白浓度,与TLR4相结合而发挥作用,故血清TLR4含量急剧下降。然而,重症感染后即刻予以TLR4干预后,实验动物血清TLR4表达变化亦更加复杂。与单纯CLP组相似,予以TLR4干预后,血清TLR4蛋白浓度亦呈现双峰趋势,且高峰值提前及数值明显高于单纯CLP组,该研究结果提示,重症感染后单纯予以TLR4干预是无法抑制TLR介导的炎症反应通路的,同样亦证实炎症级联反应,炎性细胞因子释放等信号转导通路是复杂的、相互交织的"cross-link"系统,单一改变某个/某些个信号转录调节因子,可能作用极其有限。
与既往较多数研究以免疫组织化学技术,如Western blot,聚合酶链反应(polymerase chain reaction,PCR)等技术检测特定组织TLR4蛋白浓度不同,本研究采用以ELISA法检测血清TLR4蛋白浓度,基于如下考虑:(1)本研究中以全血溶媒物的血液标本形式检测TLR4,该标本包括血细胞膜,巨噬细胞以及血小板细胞膜,而TLR4作为膜受体蛋白,存在于细胞膜上,因此该检测方法在一定程度上亦代表实验动物体内TLR4变化程度,且本研究数据采用组间比较,各组基线水平一致;此外,本研究所采用的ELISA检测方法亦被Singh等证实合理有效。(2)脓毒症是严重危及危重患者生命的疾病,其疾病发生发展快,死亡率高,且早期诊断困难,TLR4作为一种炎症因子调控通路上的重要蛋白,寻找可用于早期诊断的生物标志物具有重要意义,而ELISA是可用于临床患者检测且方便易掌握的检测技术,可在临床诊疗过程中顺利开展,且ELISA法检测临床患者血清TLR4浓度已被用于临床研究。本研究结果证实脓毒症实验动物体内TLR4蛋白浓度明显升高,进一步证实炎症刺激机体炎症信号通路激活,TLR4表达增高。亦有研究证实LPS可通过激活TLR4介导的炎症通路刺激单核巨噬细胞及其他炎性细胞,而Singh团队的研究结果明确证实LPS可导致TLR4表达增加。反之,亦有研究证实TLR4表达下调与降低的炎症反应相关。因此,本研究结果也为本研究团队继续深入开展脓毒症炎症因子调控系统研究,探究脓毒症发生发展过程中的关键因子,寻找脓毒症诊疗的早期分子标志物开辟新思路。
脓毒症是创伤、烧伤、休克、感染等临床急危重症患者常见的并发症之一,尽管近年来针对脓毒症做了大量的基础研究工作,并进行了有效的临床干预措施的研发及推广,但遗憾的是,无论在发达国家还是发展中国家,脓毒症仍以其高发病率和高死亡率严重威胁人类的健康与生命安全,消耗着大量的医疗资源。据不完全统计,全球每年有2~3千万患者患脓毒症,每天约有1400人死于脓毒症。在脓毒症患者中,约9%的脓毒症患者进展为重症脓毒症,3%发展为脓毒症休克,超过28%的脓毒症患者走向死亡结局。因此,提高对脓毒症的认识,正确面对脓毒症所带来的巨大挑战,对改善脓毒症患者症状及预后具有极其重大的意义。
【引用本文】: 任珊, 张远, 于明基, 等. 脓毒症大鼠血清高迁移率族蛋白B1、Toll样受体4时间-浓度变化关系研究 [J/CD] . 中华重症医学电子杂志,2018,4( 2 ): 164-169. DOI: 10.3877/cma.j.issn.2096-1537.2018.02.012


